“分类”的思想在化学学习及化学学科发展中起着重要作用。现有下列物质:
① 固体②熔融
固体②熔融 ③淀粉溶液④液态氯化氢⑤NaCl溶液⑥
③淀粉溶液④液态氯化氢⑤NaCl溶液⑥ ⑦金属铜⑧
⑦金属铜⑧ ⑨酒精⑩
⑨酒精⑩
回答下列问题:
(1)以上物质中属于电解质的是_____ (填序号,下同),属于非电解质的是_____ 。
(2)②熔融 能导电,其电离方程式为
能导电,其电离方程式为_____ 。
(3)③淀粉溶液所属分散系为_____ ,⑤NaCl溶液所属分散系为_____ ,二者如果混合,可采用_____ 方法分离。
(4)⑧ 与水的反应属于氧化还原反应,化学方程式为
与水的反应属于氧化还原反应,化学方程式为_____ ,该反应中 是
是_____ (“氧化剂”“还原剂”或“既是氧化剂又是还原剂”),每当有1mol 参与反应,转移电子数为
参与反应,转移电子数为_____ (设 为阿伏伽德罗常数的值)。
为阿伏伽德罗常数的值)。
(5)已知⑨ (次磷酸)与足量KOH溶液反应的化学方程式为
(次磷酸)与足量KOH溶液反应的化学方程式为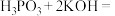
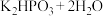 ,
, 属于
属于_____ (填“正盐”或“酸式盐”)。
①
 固体②熔融
固体②熔融 ③淀粉溶液④液态氯化氢⑤NaCl溶液⑥
③淀粉溶液④液态氯化氢⑤NaCl溶液⑥ ⑦金属铜⑧
⑦金属铜⑧ ⑨酒精⑩
⑨酒精⑩
回答下列问题:
(1)以上物质中属于电解质的是
(2)②熔融
 能导电,其电离方程式为
能导电,其电离方程式为(3)③淀粉溶液所属分散系为
(4)⑧
 与水的反应属于氧化还原反应,化学方程式为
与水的反应属于氧化还原反应,化学方程式为 是
是 参与反应,转移电子数为
参与反应,转移电子数为 为阿伏伽德罗常数的值)。
为阿伏伽德罗常数的值)。(5)已知⑨
 (次磷酸)与足量KOH溶液反应的化学方程式为
(次磷酸)与足量KOH溶液反应的化学方程式为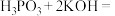
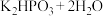 ,
, 属于
属于
更新时间:2024-01-04 19:39:14
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】酸的主要化学性质
[思考] 从微观角度来看,不同的酸溶液中都含有___________ ,故酸的化学通性都由___________ 体现。
| 酸的主要化学性质 | 反应实例(以盐酸为例,写出化学方程式) |
| (1)与活泼金属反应 | |
| (2)与碱性氧化物反应 | |
| (3)与碱反应 | |
| (4)与某些盐反应 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)从H、O、S、K四种元素中选择合适的元素,组成属于表中第一栏类型的物质,将其化学式填在表中相应的空格内(只要求举一例)。
(2)用你在上表中所填的物质,写出符合下列要求的化学方程式:
①酸性氧化物+碱性氧化物:__________________________ 。
②酸性氧化物+足量的碱:_____________________________ 。
③碱性氧化物+酸:____________________________ 。
| 类型 | 酸性 氧化物 | 碱性 氧化物 | 含氧酸 | 碱 | 含氧酸盐 |
| 化学式 |
(2)用你在上表中所填的物质,写出符合下列要求的化学方程式:
①酸性氧化物+碱性氧化物:
②酸性氧化物+足量的碱:
③碱性氧化物+酸:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】①石墨②氯化钠③蔗糖④稀硫酸⑤NH4HSO4溶液⑥碳酸氢钠⑦氢氧化钡溶液⑧冰醋酸⑨氯化氢⑩铜
(1)其中能导电的是___________ (填写序号,下同);属于电解质的是___________ ;属于非电解质的是___________ 。
(2)写出物质⑤在水中的电离方程式:___________ 。
(3)写出物质④和⑦反应的离子方程式:___________ 。
(4)写出物质⑥和⑨在水中发生反应的离子方程式:___________ 。
(5)写出氧化铜与④发生反应的离子方程式:___________ 。
(1)其中能导电的是
(2)写出物质⑤在水中的电离方程式:
(3)写出物质④和⑦反应的离子方程式:
(4)写出物质⑥和⑨在水中发生反应的离子方程式:
(5)写出氧化铜与④发生反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下列是中学常见的物质:①铜②液氯③稀盐酸④氯化银⑤NaHSO4⑥乙醇⑦冰醋酸⑧氟化氢⑨氢氧化钡溶液⑩氨水回答下列问题:
(1)上述物质中能导电的是___________ (填写序号,下同),属于电解质的是___________ ,属于非电解质的是___________ ,属于强电解质的是___________ ,属于弱电解质的是___________ 。
(2)写出下列物质在水溶液中的电离方程式:⑤___________ ;⑩___________ 。
(1)上述物质中能导电的是
(2)写出下列物质在水溶液中的电离方程式:⑤
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】现有9种物质:①Na;②盐酸;③ ;④
;④ ;⑤空气;⑥
;⑤空气;⑥ ;⑦
;⑦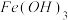 胶体;⑧NaOH;⑨
胶体;⑧NaOH;⑨
(1)属于电解质的是_______ (用序号填空,下同);属于非电解质的是_______ ;属于碱性氧化物的是_______ 。
(2)实验室中少量①通常保存在_______ 中;④在工业上大量用于_______ (写出一种用途即可)。
(3)⑧物质的水溶液常常用来吸收④,请写出此反应的化学方程式_______ 。
(4)③是一种白色晶体,因受热易分解并产生气体适宜作膨松剂,请写出此物质受热分解的化学方程式_______ 。
(5)向⑦中逐滴滴入过量的②,会出现一系列变化:先出现红褐色沉淀,原因是胶体发生_______ ,随后沉淀溶解,得到黄色溶液,原因_______ (用离子方程式表示)。
 ;④
;④ ;⑤空气;⑥
;⑤空气;⑥ ;⑦
;⑦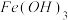 胶体;⑧NaOH;⑨
胶体;⑧NaOH;⑨
(1)属于电解质的是
(2)实验室中少量①通常保存在
(3)⑧物质的水溶液常常用来吸收④,请写出此反应的化学方程式
(4)③是一种白色晶体,因受热易分解并产生气体适宜作膨松剂,请写出此物质受热分解的化学方程式
(5)向⑦中逐滴滴入过量的②,会出现一系列变化:先出现红褐色沉淀,原因是胶体发生
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】用KMnO4和浓盐酸制备氯气反应方程式如下: 2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,反应中氧化剂与还原剂物质的量之比为_____ ;若在标准状况下得到11.2L氯气,则参加反应的KMnO4质量是___________ g,被氧化HCl的物质的量是______
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】硫酸是一种重要的工业原料,可用于制造肥料、药物、洗涤剂、蓄电池等。工业上生产硫酸常以硫磺或黄铁矿为原料,制备硫酸的尾气中含有硫的氧化物等。
(1)除去试管壁上沾有的硫磺,可用的化学试剂是___________ (填名称)。
(2)二氧化硫可以用氯化铁溶液吸收,生成氯化亚铁和两种强酸,该反应的离子方程式为___________ 。
(3)二氧化硫与硝酸钠溶液的反应为3SO2+2NaNO3+2H2O=Na2SO4+2NO+2H2SO4。
①该反应体现SO2的性质是___________ 。
②SO2经催化氧化可转化为SO3,该转化的化学方程式是___________ 。
(4)黄铁矿主要成分是FeS2,写出用黄铁矿制备硫酸的第一步反应的化学方程式:_______ 。
(1)除去试管壁上沾有的硫磺,可用的化学试剂是
(2)二氧化硫可以用氯化铁溶液吸收,生成氯化亚铁和两种强酸,该反应的离子方程式为
(3)二氧化硫与硝酸钠溶液的反应为3SO2+2NaNO3+2H2O=Na2SO4+2NO+2H2SO4。
①该反应体现SO2的性质是
②SO2经催化氧化可转化为SO3,该转化的化学方程式是
(4)黄铁矿主要成分是FeS2,写出用黄铁矿制备硫酸的第一步反应的化学方程式:
您最近一年使用:0次

 4NH3 + 3O2
4NH3 + 3O2

