有A、B、C、D四种元素,A元素是地壳中含量最多的金属元素;B元素的原子其M层电子数比L层少1个电子;C元素的原子得到2个电子,D元素的原子失去1个电子,所得到的微粒都具有与氖原子相同的电子层结构。回答下列问题:
(1)元素A的名称为___________ ,元素A的单质与 溶液反应的离子方程式为
溶液反应的离子方程式为___________ 。
(2)元素B在周期表中的位置:___________ ,画出B的离子结构示意图:___________ 。
(3)C和D形成的化合物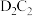 可作供氧剂,写出
可作供氧剂,写出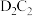 与
与 反应的化学方程式:
反应的化学方程式:___________ 。消耗 生成的氧气在标准状况下的体积为
生成的氧气在标准状况下的体积为___________ 。
(4)设计实验证明D的金属性强于A:___________ 。
(1)元素A的名称为
 溶液反应的离子方程式为
溶液反应的离子方程式为(2)元素B在周期表中的位置:
(3)C和D形成的化合物
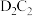 可作供氧剂,写出
可作供氧剂,写出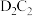 与
与 反应的化学方程式:
反应的化学方程式: 生成的氧气在标准状况下的体积为
生成的氧气在标准状况下的体积为(4)设计实验证明D的金属性强于A:
更新时间:2023-12-30 19:28:25
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】现有部分前四周期元素的性质或原子结构如下表:
(1)T在周期表中的位置为___________ ,基态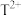 的核外电子排布式为
的核外电子排布式为_____________ ;T的单质在高温下与X的氢化物反应,其化学方程式为____________________________________________ 。
(2)基态Z原子中,核外电子占据的最高能级的符号是______________ ,占据最高能级的电子的电子云形状为______________ 。
(3)W、X、Y三种元素的离子半径由大到小的顺序是______________ (用离子符号表示)。
(4)在W、X的气态氢化物中,较稳定的是__________________________________________ 。
元素编号 | 元素性质或原子结构 |
W | 单质能与水剧烈反应,所得溶液呈弱酸性 |
X | 基态原子的s轨道与p轨道电子数相等 |
Y | 第三周期元素的简单离子中半径最小 |
Z | L层有三个未成对电子 |
T | 该元素的正三价离子的3d能级为半充满 |
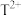 的核外电子排布式为
的核外电子排布式为(2)基态Z原子中,核外电子占据的最高能级的符号是
(3)W、X、Y三种元素的离子半径由大到小的顺序是
(4)在W、X的气态氢化物中,较稳定的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】A.B.C是短周期的三种相邻元素。A.B同主族,B.C同周期;这三种元素的质子数之和为38,最外层电子数之和为16。
(1)则它们的元素符号分别为A______ ,B______ ,C______ 。
(2)A元素在周期表中的位置,第____ 周期,第_____ 族,A单质的电子式为_______ 。
(1)则它们的元素符号分别为A
(2)A元素在周期表中的位置,第
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号:
A___________ ,B ___________ ,C __________ ,D __________ ,E ____________
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:___________________________ 。
(3)写出A、B两元素的最高价氧化物的水化物相互反应的化学方程式:_______________________ 。
(4)写出B、E两元素的最高价氧化物的水化物相互反应的离子方程式:_____________________ 。
(5)C、D、E的氢化物稳定性由强到弱依次为:(用化学式表示)__________________________ 。
(1)写出下列元素符号:
A
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:
(3)写出A、B两元素的最高价氧化物的水化物相互反应的化学方程式:
(4)写出B、E两元素的最高价氧化物的水化物相互反应的离子方程式:
(5)C、D、E的氢化物稳定性由强到弱依次为:(用化学式表示)
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】现有四种短周期元素A、B、C、D,已知:①C、D在同一周期,A、B在同一主族;②它们可以组成化合物A2C、B2C2、DC2、D2A4等;③B的简单阳离子与C的简单阴离子的核外电子排布相同;④B2C2与A2C或DC2反应都生成气体C2,单质B与A2C反应生成气体A2,A2与气体C2按体积比2:1混合后点燃发生爆炸,其产物是一种常温下常见的无色无味的液体。请回答下列问题:
(1)写出元素符号:A__ 、B__ 、C__ 、D__ 。
(2)在A2C、B2C2、DC2和D2A4中,同时含有离子键和非极性共价键的化合物的电子式为__ ,按原子轨道重叠方式,其非极性键的类型是__ 。化合物DC2的结构式为__ 。
(3)A2C分子的电子式为__ ,按原子轨道重叠方式,其共价键的类型是__ 。D2A4是平面形分子,其分子中含有__ 个σ键,__ 个π键。
(1)写出元素符号:A
(2)在A2C、B2C2、DC2和D2A4中,同时含有离子键和非极性共价键的化合物的电子式为
(3)A2C分子的电子式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】有7种短周期元素,其原子半径及主要化合价如下:完成下列填空:
(1)A在元素周期表中的位置是_______ ,当配制150mL实验所需的0.1 mol∙L−1 A最高价氧化物的水合物的溶液,用到的玻璃仪器有_______ ,下列操作可能造成此次配制溶液浓度偏低的有_______ 。
A.用蒸馏水洗净容量瓶未干燥,直接配制新溶液
B.量筒未干燥
C.溶解后将溶液未冷却直接进行后续操作
D.溶解后洗涤烧杯和玻璃棒的洗涤液未全部转移至容量瓶中
E.定容时俯视液面
F.定容时不小心加蒸馏水超过刻度线,用胶头滴管迅速吸出多余的水
(2)上述7种元素形成的简单离子中,离子半径最大是_______ (用离子符号表示)
(3)写出B单质与烧碱溶液反应的离子方程式,并用单线桥法表示出电子转移_______ 。
(4)甲是由G、H两种元素组成的18e-分子,甲中滴入E单质的水溶液,有无色气体产生,写出反应离子方程式:_______ 。
(5)用一个化学方程式表示E元素的非金属性比D强_______ 。
| 元素代号 | A | B | D | E | F | G | H |
| 原子半径/nm | 0.186 | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 | 0.032 |
| 主要化合价 | +1 | +3 | +6,−2 | +7,−1 | +5,−3 | −2 | +1 |
A.用蒸馏水洗净容量瓶未干燥,直接配制新溶液
B.量筒未干燥
C.溶解后将溶液未冷却直接进行后续操作
D.溶解后洗涤烧杯和玻璃棒的洗涤液未全部转移至容量瓶中
E.定容时俯视液面
F.定容时不小心加蒸馏水超过刻度线,用胶头滴管迅速吸出多余的水
(2)上述7种元素形成的简单离子中,离子半径最大是
(3)写出B单质与烧碱溶液反应的离子方程式,并用单线桥法表示出电子转移
(4)甲是由G、H两种元素组成的18e-分子,甲中滴入E单质的水溶液,有无色气体产生,写出反应离子方程式:
(5)用一个化学方程式表示E元素的非金属性比D强
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】现有A、B、C、D四种元素,A元素形成的-2价阴离子比氦原子的核外电子数多8个,B元素与A元素形成的一种化合物为淡黄色固体,该固体遇到空气能生成A的单质;C为原子核内有12个中子的金属元素,当2.4克C与足量热水反应时,在标准状况下放出气体2.24L,C形成正二价阳离子;D元素原子的M层上有7个电子。
(1)写出B、C两种元素的元素符号:B________ ,C_________ ;
(2)画出A2-的离子结构示意图:__________________________ ,
指出D在周期表的位置:_____________________________ ;
(3)写出B的呈淡黄色的化合物与CO2反应的化学方程式:________________ ;
(4)比较D的气态氢化物与H2S和HF的稳定性:___________ (用化学式表示);
(5)用电子式表示C与D形成化合物的过程:_____________________________ 。
(1)写出B、C两种元素的元素符号:B
(2)画出A2-的离子结构示意图:
指出D在周期表的位置:
(3)写出B的呈淡黄色的化合物与CO2反应的化学方程式:
(4)比较D的气态氢化物与H2S和HF的稳定性:
(5)用电子式表示C与D形成化合物的过程:
您最近一年使用:0次



