乙醇在能源、生产及日常生活等许多方面都有十分广泛的应用。请计算:
(1)将足量乙醇与9.2 g金属钠充分反应,则标准状况下生成气体的体积是_______ L
(2)若一定量的乙醇和O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。产物依次经过浓硫酸和碱石灰使其被充分吸收,浓硫酸增重10.8 g,碱石灰增重13.2 g。则氧气的物质的量是_______________ mol,燃烧产物的平均摩尔质量是____________ g/mol。
(1)将足量乙醇与9.2 g金属钠充分反应,则标准状况下生成气体的体积是
(2)若一定量的乙醇和O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。产物依次经过浓硫酸和碱石灰使其被充分吸收,浓硫酸增重10.8 g,碱石灰增重13.2 g。则氧气的物质的量是
13-14高一下·江西抚州·期末 查看更多[5]
(已下线)2013-2014江西省临川一中高一下学期期末考试化学试卷(已下线)2013-2014学年江西省临川一中高一(下)期末考试化学试卷7.3.1 乙醇——2020年春高一新人教版第二册化学一课一练2020年春高一化学新人教版第二册课后同步:7.3.1 乙醇浙江省横店高级中学2021-2022学年高一下学期期中考试化学试题
更新时间:2014-10-10 14:28:39
|
相似题推荐
【推荐1】乙醇分子中有5种化学键,如图所示 ,在不同的反应中会有不同形式的化学键断裂,根据下列不同反应,按要求回答相关问题。
,在不同的反应中会有不同形式的化学键断裂,根据下列不同反应,按要求回答相关问题。
(1)和金属钠反应,断裂的化学键为_______ (填断键序号,下同),化学方程式为_________ 。
1mol乙醇和足量的金属钠反应,生成标准状况下的氢气为_________ L。
(2)乙醇在空气中充分燃烧,反应时断裂的化学键为_____ ,反应的化学方程式为_____ 。
(3)①将弯成螺旋状的铜丝灼烧,铜丝变黑,反应原理为_______ (用化学方程式表示)。然后将灼热的铜丝插入乙醇中,铜丝表面由黑变红,在此过程中,乙醇分子中断裂的化学键为________ ,反应方程式为______ ,整个过程反应总方程式为_______ ,铜在反应中起到________ 作用。
②如果将乙醇改为 ,试写出在该条件下的化学反应方程式:
,试写出在该条件下的化学反应方程式:________ 。
③如果醇为 ,在该条件下,醇还能被催化氧化吗
,在该条件下,醇还能被催化氧化吗____ ?为什么______ ?
 ,在不同的反应中会有不同形式的化学键断裂,根据下列不同反应,按要求回答相关问题。
,在不同的反应中会有不同形式的化学键断裂,根据下列不同反应,按要求回答相关问题。(1)和金属钠反应,断裂的化学键为
1mol乙醇和足量的金属钠反应,生成标准状况下的氢气为
(2)乙醇在空气中充分燃烧,反应时断裂的化学键为
(3)①将弯成螺旋状的铜丝灼烧,铜丝变黑,反应原理为
②如果将乙醇改为
 ,试写出在该条件下的化学反应方程式:
,试写出在该条件下的化学反应方程式:③如果醇为
 ,在该条件下,醇还能被催化氧化吗
,在该条件下,醇还能被催化氧化吗
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某有机物的结构确定:
(1)测定实验式:某含C、H、O三种元素的有机物,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51%,则其实验式是_______ ;
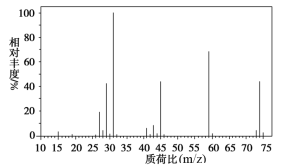
(2)确定分子式:如图是该有机物的质谱图,则其相对分子质量为_______ ;分子式为_______ ;
(3)结构式的确定:经测定,该有机物在核磁共振氢谱中出现四个峰,其氢原子个数比为6∶1∶2∶1;该有机物与金属钠反应产生氢气;则A的结构简式为_______ 。
(4)写出与A具有相同官能团的同分异构体_______ 。
(1)测定实验式:某含C、H、O三种元素的有机物,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51%,则其实验式是
(2)确定分子式:如图是该有机物的质谱图,则其相对分子质量为

(3)结构式的确定:经测定,该有机物在核磁共振氢谱中出现四个峰,其氢原子个数比为6∶1∶2∶1;该有机物与金属钠反应产生氢气;则A的结构简式为
(4)写出与A具有相同官能团的同分异构体
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】A是乙烯与水加成后的产物,它易溶于水并有特殊香味,并能进行如图所示的多种反应。
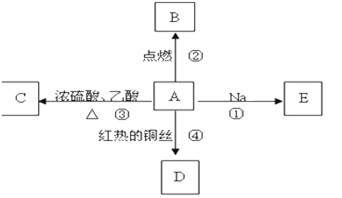
(1)写出A的化学式_____________________________ 。
(2)下列反应的化学方程式及反应类型
反应①______________________________ 反应类型:________________ ;
反应②______________________________ 反应类型:________________ ;
反应③______________________________ 反应类型:________________ ;
反应④______________________________ 反应类型:________________ ;
(3)比较反应①与钠和水反应的现象有什么相同和不同
相同点:_________________________ 。
不同点:_________________________ 。

(1)写出A的化学式
(2)下列反应的化学方程式及反应类型
反应①
反应②
反应③
反应④
(3)比较反应①与钠和水反应的现象有什么相同和不同
相同点:
不同点:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】生活中的有机物种类丰富,在衣食住行等多方面应用广泛,其中乙醇是比较常见的有机物。
(1)乙醇是无色有特殊香味的液体,密度比水_______ 。
(2)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为__________________ (不写反应条件),原子利用率是______________ 。
(3)属于乙醇的同分异构体的是_______ (选填编号)。
A.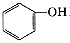 B.
B.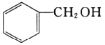 C.甲醇 D.CH3—O—CH3 E.HO—CH2CH2—OH
C.甲醇 D.CH3—O—CH3 E.HO—CH2CH2—OH
(4)乙醇能够发生氧化反应:
① 46 g乙醇完全燃烧消耗_______ mol氧气。
② 乙醇在铜作催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为____________________ 。
(1)乙醇是无色有特殊香味的液体,密度比水
(2)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为
(3)属于乙醇的同分异构体的是
A.
 B.
B. C.甲醇 D.CH3—O—CH3 E.HO—CH2CH2—OH
C.甲醇 D.CH3—O—CH3 E.HO—CH2CH2—OH(4)乙醇能够发生氧化反应:
① 46 g乙醇完全燃烧消耗
② 乙醇在铜作催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为
您最近一年使用:0次
【推荐2】生活中的有机物种类丰富,在衣食住行等多方面应用广泛,其中乙醇是比较常见的有机物。
(1)乙醇是无色有特殊香味的液体,密度比水的_______ 。
(2)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为_______ 。反应类型是_______ 。
(3)下列属于乙醇的同系物的是_______ ,属于乙醇的同分异构体的是_______ (填编号)。
A. B.
B.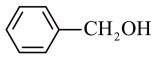 C.乙醚(CH3CH2OCH2CH3) D.甲醇 E. CH3—O—CH3 F. HO—CH2CH2—OH
C.乙醚(CH3CH2OCH2CH3) D.甲醇 E. CH3—O—CH3 F. HO—CH2CH2—OH
(4)乙醇能够发生氧化反应:
①46 g乙醇完全燃烧消耗_______ mol氧气。
②乙醇在铜作催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为_______ 。
(1)乙醇是无色有特殊香味的液体,密度比水的
(2)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为
(3)下列属于乙醇的同系物的是
A.
 B.
B. C.乙醚(CH3CH2OCH2CH3) D.甲醇 E. CH3—O—CH3 F. HO—CH2CH2—OH
C.乙醚(CH3CH2OCH2CH3) D.甲醇 E. CH3—O—CH3 F. HO—CH2CH2—OH(4)乙醇能够发生氧化反应:
①46 g乙醇完全燃烧消耗
②乙醇在铜作催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】生活中的有机物种类丰富,在衣食住行等多方面应用广泛,其中乙醇是比较常见的有机物。
(1)乙醇是无色有特殊香味的液体,密度比水的___________ 。
(2)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为___________ 。反应类型是___________ 。
(3)下列属于乙醇的同系物的是___________ ,属于乙醇的同分异构体的是___________ (填编号)。
A.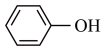 B.
B.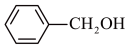 C.乙醚(CH3CH2OCH2CH3)D.甲醇E.CH3—O—CH3F.HO—CH2CH2—OH
C.乙醚(CH3CH2OCH2CH3)D.甲醇E.CH3—O—CH3F.HO—CH2CH2—OH
(4)乙醇能够发生氧化反应:46g乙醇完全燃烧消耗___________ mol氧气。
(1)乙醇是无色有特殊香味的液体,密度比水的
(2)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为
(3)下列属于乙醇的同系物的是
A.
 B.
B. C.乙醚(CH3CH2OCH2CH3)D.甲醇E.CH3—O—CH3F.HO—CH2CH2—OH
C.乙醚(CH3CH2OCH2CH3)D.甲醇E.CH3—O—CH3F.HO—CH2CH2—OH(4)乙醇能够发生氧化反应:46g乙醇完全燃烧消耗
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下面给出了四种烃A、B、C、D的相关信息:
①烃A在所有的烃中含碳的质量分数最低;
②烃B是一种植物生长调节剂,可用于催熟果实;
③烃C在氧气中燃烧产生的氧炔焰常用来切割或焊接金属;
④烃D的分子比例模型如图所示 。
。
据此回答有关问题:
(1)将A和Cl2混合充入一试管,密封后置于光亮处,一段时间后能看到试管内壁上出现的油状物不可能是________(填编号)。
(2)写出实验室制取B的反应类型________________________ 。
(3)实验室制取C的化学方程式为________________________ 。
(4)D分子中不存在碳碳单键和碳碳双键交替的结构,以下能证实这一事实的是__________________ 。
a.D的邻位二氯取代物不存在同分异构体
b.D的间位二氯取代物不存在同分异构体
c.D的对位二氯取代物不存在同分异构体
(5)a L体积比为1∶3的M、N两种链烃的混合气体,可与0.5aL(状态相同)氢气发生加成反应,则M、N两种链烃的通式可能是___________。
①烃A在所有的烃中含碳的质量分数最低;
②烃B是一种植物生长调节剂,可用于催熟果实;
③烃C在氧气中燃烧产生的氧炔焰常用来切割或焊接金属;
④烃D的分子比例模型如图所示
 。
。据此回答有关问题:
(1)将A和Cl2混合充入一试管,密封后置于光亮处,一段时间后能看到试管内壁上出现的油状物不可能是________(填编号)。
| A.CH3Cl | B.CH2Cl2 | C.CHCl3 | D.CCl4 |
(3)实验室制取C的化学方程式为
(4)D分子中不存在碳碳单键和碳碳双键交替的结构,以下能证实这一事实的是
a.D的邻位二氯取代物不存在同分异构体
b.D的间位二氯取代物不存在同分异构体
c.D的对位二氯取代物不存在同分异构体
(5)a L体积比为1∶3的M、N两种链烃的混合气体,可与0.5aL(状态相同)氢气发生加成反应,则M、N两种链烃的通式可能是___________。
| A.CnH2n和CnH2n+2 | B.CnH2n-2和CnH2n+2 |
| C.CnH2n和CnH2n | D.CnH2n和CnH2n-2 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】C1化学是指从一个碳原子的化合物(如CH4,CO,CO2 CH3OH,HCHO等)出发合成各种化学品的技术。从煤、天然气制合成气再进一步制备各种化工产品和洁净燃料,已成为当今化学工业发展的必然趋势。其中甲醇是C1化学的基础。
①CO与H2按一定比例可生成乙二醇,则n(CO)/n(H2)=_______________ 。(填数字)
②若汽油平均组成用CmHn表示,则合成汽油应控制n(CO)/n(H2)=_____________ 。(用m、n表示),
③甲醇在一定条件下与CO、H2作用生成有机物A,A发生加聚可生成高分子 写出生成A的化学方程式
写出生成A的化学方程式_____________ 。
①CO与H2按一定比例可生成乙二醇,则n(CO)/n(H2)=
②若汽油平均组成用CmHn表示,则合成汽油应控制n(CO)/n(H2)=
③甲醇在一定条件下与CO、H2作用生成有机物A,A发生加聚可生成高分子
 写出生成A的化学方程式
写出生成A的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】写出下列各有机物的结构简式或分子式:
(1)相对分子质量为84的烃的分子式为__________ 。
(2)某炔烃和H2充分加成生成2,5—二甲基己烷,则该炔烃的结构简式为________ 。
(3)0.2 mol烃A在氧气中完全燃烧后生成1.2 mol CO2和1.2 mol H2O,催化加氢后生成2,2—二甲基丁烷,则烃A的结构简式为__________ 。
(4)某烃1 mol和2 mol HCl完全加成,生成的氯代烷最多还可以与4 mol氯气反应,则该烃的结构简式为__________ 。
(1)相对分子质量为84的烃的分子式为
(2)某炔烃和H2充分加成生成2,5—二甲基己烷,则该炔烃的结构简式为
(3)0.2 mol烃A在氧气中完全燃烧后生成1.2 mol CO2和1.2 mol H2O,催化加氢后生成2,2—二甲基丁烷,则烃A的结构简式为
(4)某烃1 mol和2 mol HCl完全加成,生成的氯代烷最多还可以与4 mol氯气反应,则该烃的结构简式为
您最近一年使用:0次



