某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol· L-1 盐酸、0.55mol· L-1NaOH溶液,尚缺少的实验玻璃用品是________ 、________ 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?______ (填“能”或“否”),
(3)他们记录的实验数据如下:
已知:Q=Cm(t2 -t1),反应后溶液的比热容C为4.18KJ·℃-1· kg-1,各物质的密度均为1g·cm-3。
①根据实验数据计算并写出NaOH溶液与HCl溶液反应的热化学方程式:_______________
(4)若用KOH代替NaOH,对测定结果____ (填“有”或“无”)影响;若用醋酸代替HCl做实验,对测定结果_____ (填“有”或“无”)影响。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol· L-1 盐酸、0.55mol· L-1NaOH溶液,尚缺少的实验玻璃用品是
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?
(3)他们记录的实验数据如下:
| 实 验 用 品 | 溶 液 温 度 | 中和热△H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | |
已知:Q=Cm(t2 -t1),反应后溶液的比热容C为4.18KJ·℃-1· kg-1,各物质的密度均为1g·cm-3。
①根据实验数据计算并写出NaOH溶液与HCl溶液反应的热化学方程式:
(4)若用KOH代替NaOH,对测定结果
14-15高二上·云南玉溪·期中 查看更多[4]
河北省邯郸市2016-2017学年高二上学期期中考试化学试题2016-2017学年河北省邯郸市成安一中、永年二中高二上期中化学卷2015-2016学年江西省南昌二中高二上第一次月考化学试卷(已下线)2014-2015学年云南省玉溪市第一中学高二上学期期中考试化学试卷
更新时间:2016-12-09 06:43:11
|
【知识点】 反应热
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)已知1g的甲烷完全燃烧生成液态水放出akJ的热量,写出表示甲烷燃烧热的热化学方程式为___ 。
(2)某实验小组用100mL0.55mol·L-1NaOH溶液与100mL0.5mol·L-1盐酸进行中和热的测定。装置如图所示。
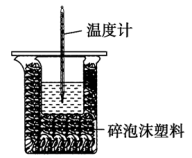
回答下列问题:
①图中装置缺少的仪器是____ 。
②碱稍过量的原因是____ 。
③若将盐酸改为相同体积、相同浓度的醋酸,测得中和热为ΔH1,NaOH溶液与盐酸反应中和热为ΔH,则ΔH1____ ΔH(填写<、>、=);若测得该反应放出的热量为2.865kJ,请写出盐酸与NaOH溶液反应的中和热的热化学方程式:__
(3)已知拆开1molH-H键、1molCl-Cl键、1molH—Cl键分别需要的能量是akJ、bkJ、ckJ,则反应H2(g)+Cl2(g)=2HCl(g)的∆H=____ 。
(4)①2O2(g)+N2(g)=N2O4(l) ∆H1
②N2(g)+2H2(g)=N2H4(l) ∆H2
③O2(g)+2H2(g)=2H2O(g) ∆H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ∆H4
上述反应热效应之间的关系式为∆H4=____ (用∆H1、∆H2、∆H3表示)。
(2)某实验小组用100mL0.55mol·L-1NaOH溶液与100mL0.5mol·L-1盐酸进行中和热的测定。装置如图所示。

回答下列问题:
①图中装置缺少的仪器是
②碱稍过量的原因是
③若将盐酸改为相同体积、相同浓度的醋酸,测得中和热为ΔH1,NaOH溶液与盐酸反应中和热为ΔH,则ΔH1
(3)已知拆开1molH-H键、1molCl-Cl键、1molH—Cl键分别需要的能量是akJ、bkJ、ckJ,则反应H2(g)+Cl2(g)=2HCl(g)的∆H=
(4)①2O2(g)+N2(g)=N2O4(l) ∆H1
②N2(g)+2H2(g)=N2H4(l) ∆H2
③O2(g)+2H2(g)=2H2O(g) ∆H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ∆H4
上述反应热效应之间的关系式为∆H4=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】碳是常见的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程:
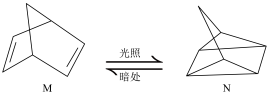
ΔH=+88.6kJ·mol-1。则M、N相比,较稳定的是_____ 。
(2)已知CH3OH(l)的燃烧热ΔH=-726.5kJ·mol-1,CH3OH(l)+ O2(g)===CO2(g)+2H2(g)ΔH=-akJ·mol-1,则a
O2(g)===CO2(g)+2H2(g)ΔH=-akJ·mol-1,则a________ 726.5(填“>”“<”或“=”)。
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)===2Al2O3(s)+3TiC(s) ΔH=-1176kJ·mol-1,则反应过程中,每转移1mol电子放出的热量为________ 。
(4)煤气化制合成气(CO和H2)
已知:①C(s)+H2O(g) CO(g)+H2(g)ΔH1=+131.3kJ·mol-1
CO(g)+H2(g)ΔH1=+131.3kJ·mol-1
②C(s)+2H2O(g) CO2(g)+2H2(g)ΔH2=+90kJ·mol-1
CO2(g)+2H2(g)ΔH2=+90kJ·mol-1
则一氧化碳与水蒸气反应生成二氧化碳和氢气的热化学方程式是________ 。
(1)有机物M经过太阳光光照可转化成N,转化过程:

ΔH=+88.6kJ·mol-1。则M、N相比,较稳定的是
(2)已知CH3OH(l)的燃烧热ΔH=-726.5kJ·mol-1,CH3OH(l)+
 O2(g)===CO2(g)+2H2(g)ΔH=-akJ·mol-1,则a
O2(g)===CO2(g)+2H2(g)ΔH=-akJ·mol-1,则a(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)===2Al2O3(s)+3TiC(s) ΔH=-1176kJ·mol-1,则反应过程中,每转移1mol电子放出的热量为
(4)煤气化制合成气(CO和H2)
已知:①C(s)+H2O(g)
 CO(g)+H2(g)ΔH1=+131.3kJ·mol-1
CO(g)+H2(g)ΔH1=+131.3kJ·mol-1②C(s)+2H2O(g)
 CO2(g)+2H2(g)ΔH2=+90kJ·mol-1
CO2(g)+2H2(g)ΔH2=+90kJ·mol-1则一氧化碳与水蒸气反应生成二氧化碳和氢气的热化学方程式是
您最近一年使用:0次

 和液态
和液态 ,放出890.3kJ的热量,
,放出890.3kJ的热量, 的燃烧热为
的燃烧热为

