实验室以一种工业废渣(主要成分为MgCO3、Mg2SiO4和少量Fe、Al的氧化物)为原料制备MgCO3·3H2O。实验过程如下。
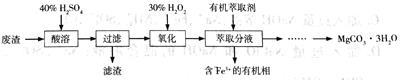
(1)酸溶过程中主要反应的热化学方程式为
MgCO3(s)+2H+(aq)=Mg2+(aq)+CO2(g)+H2O(l) ΔH=-50.4 kJ/mol
Mg2SiO4(s)+4H+(aq)= 2Mg2+(aq)+H2SiO3(s)+H2O(l) ΔH=-225.4 kJ/mol
酸溶需加热的目的是_________ ;所加H2SO4不宜过量太多的原因是__________ 。
(2)加入H2O2氧化时发生发应的离子方程式为___________ 。
(3)用如图所示的实验装置进行萃取分液,以除去溶液中的Fe3+。
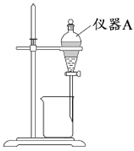
① 实验装置图中仪器A的名称为________________ 。
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有水溶液的仪器A中加入一定量的有机萃取剂,______________ 、静置、分液,并重复多次。
(4)请补充完整由萃取后得到的水溶液制备MgCO3·3H2O的实验方案:边搅拌边向溶液中滴加氨水至______________ ,过滤,____________ ,静置,___________ ,若无沉淀生成,过滤、用水洗涤固体2-3次,在50℃下干燥,得到MgCO3·3H2O。[已知该溶液中pH=8.5时Mg(OH)2开始沉淀;pH=5.0时Al(OH)3沉淀完全]。

(1)酸溶过程中主要反应的热化学方程式为
MgCO3(s)+2H+(aq)=Mg2+(aq)+CO2(g)+H2O(l) ΔH=-50.4 kJ/mol
Mg2SiO4(s)+4H+(aq)= 2Mg2+(aq)+H2SiO3(s)+H2O(l) ΔH=-225.4 kJ/mol
酸溶需加热的目的是
(2)加入H2O2氧化时发生发应的离子方程式为
(3)用如图所示的实验装置进行萃取分液,以除去溶液中的Fe3+。

① 实验装置图中仪器A的名称为
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有水溶液的仪器A中加入一定量的有机萃取剂,
(4)请补充完整由萃取后得到的水溶液制备MgCO3·3H2O的实验方案:边搅拌边向溶液中滴加氨水至
更新时间:2019-01-30 18:14:09
|
【知识点】 反应热
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
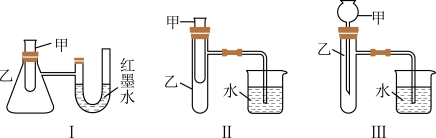
【推荐1】为了探究化学能与热能的转化,某实验小组设计了如下三套实验装置。
回答下列问题:
(1)上述三套装置中,不能证明“铜与浓硝酸的反应是吸热反应还是放热反应”的是装置______ 。
(2)某同学选用装置I进行实验(实验前U形管里液面相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,U形管中可观察到的现象是________________________ ,说明该反应属于______ (填“吸热”或“放热”)反应。
(3)为探究固体M投入水中的热效应,选择装置Ⅱ进行实验(反应在甲中进行)。
①若M为钠,则实验过程中烧杯中可观察到的现象是_________________ 。
②若观察到烧杯里导管口不产生气泡,但导管内形成一段水柱,则M可能是______ 。
(4)至少有两种实验方法能验证超氧化钾与水的反应( );是放热反应还是吸热反应。
);是放热反应还是吸热反应。
方法①:选择上述装置______ (填“I”“Ⅱ”或“Ⅲ”)进行实验。
方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到脱脂棉燃烧,则说明该反应是______ (填“吸热”或“放热”)反应。

回答下列问题:
(1)上述三套装置中,不能证明“铜与浓硝酸的反应是吸热反应还是放热反应”的是装置
(2)某同学选用装置I进行实验(实验前U形管里液面相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,U形管中可观察到的现象是
(3)为探究固体M投入水中的热效应,选择装置Ⅱ进行实验(反应在甲中进行)。
①若M为钠,则实验过程中烧杯中可观察到的现象是
②若观察到烧杯里导管口不产生气泡,但导管内形成一段水柱,则M可能是
(4)至少有两种实验方法能验证超氧化钾与水的反应(
 );是放热反应还是吸热反应。
);是放热反应还是吸热反应。方法①:选择上述装置
方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到脱脂棉燃烧,则说明该反应是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1。回答有关中和反应的问题。
(1)用0.1 mol Ba(OH)2配成稀溶液与足量稀硝酸反应,能放出_______ kJ热量。
(2)如图装置中仪器A的名称是____________ ,碎泡沫塑料的作用是_____________________________ ;要重复进行三次实验的目的是 ____________________ 。
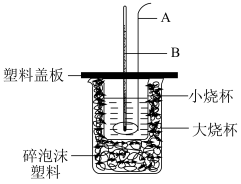
(3)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会__________ (填“偏大”、“偏小”、“无影响”)。
(4)将V1 mL 1.00 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。下列叙述正确的是_____ 。
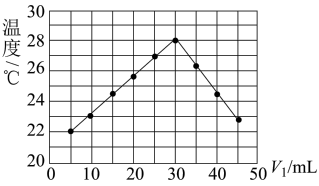
A.做该实验时环境温度为22 ℃
B.该实验表明化学能可以转化为热能
C.NaOH溶液的浓度约为1.00 mol·L-1
D.该实验表明有水生成的反应都是放热反应
(1)用0.1 mol Ba(OH)2配成稀溶液与足量稀硝酸反应,能放出
(2)如图装置中仪器A的名称是

(3)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会
(4)将V1 mL 1.00 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。下列叙述正确的是

A.做该实验时环境温度为22 ℃
B.该实验表明化学能可以转化为热能
C.NaOH溶液的浓度约为1.00 mol·L-1
D.该实验表明有水生成的反应都是放热反应
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种用品是______ ;
(2)用相同浓度和体积的醋酸代替稀盐酸溶液进行实验,求得的中和热数值__ (填“偏大”、“偏小”或“无影响”);
(3)实验中改用60mL 0.50mol/L 盐酸跟50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量_______ (填“相等”或“不相等”),所求中和热_______ (填“相等”或“不相等”)
(4)若上述实验中测得放出热量为1.4325kJ,写出该反应的热化学方程式:_____

(1)从实验装置上看,图中尚缺少的一种用品是
(2)用相同浓度和体积的醋酸代替稀盐酸溶液进行实验,求得的中和热数值
(3)实验中改用60mL 0.50mol/L 盐酸跟50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量
(4)若上述实验中测得放出热量为1.4325kJ,写出该反应的热化学方程式:
您最近一年使用:0次



