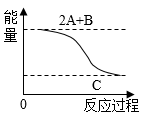
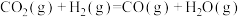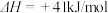已知反应:2A+B = C在一定条件下进行的能量变化如图所示,破坏1mol A中的化学键消耗的能量为Q1 kJ,破坏1mol B中的化学键消耗的能量为Q2 kJ,形成1mol C中的化学键释放的能量为Q3 kJ.请判断以下说法正确的是

| A.该反应中存在以下关系:2 Q1+ Q2< Q3 |
| B.该反应的能量转化形式只能以热能的形式进行 |
| C.当有1molB参加反应时,该反应放出的热量为:Q3 kJ |
| D.此反应为放热反应,所以在常温下一定能发生 |
更新时间:2017-06-13 21:37:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列对化学反应中能量变化的说法正确的是
| A.化学反应中一定伴有能量变化 |
| B.钠与水的反应是吸热反应 |
| C.放热反应发生时不必加热 |
| D.Ba(OH)2·8H2O 与NH4Cl的反应是放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知反应
①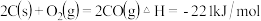
②稀溶液中,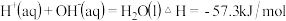 ,
,
下列结论正确的是
①
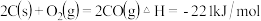
②稀溶液中,
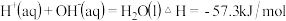 ,
,下列结论正确的是

A.碳的燃烧热为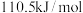 |
B.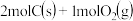 的能量比 的能量比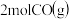 的能量高221kJ 的能量高221kJ |
C. 浓 浓 与1 molNaOH溶液混合,产生 与1 molNaOH溶液混合,产生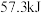 热量 热量 |
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出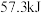 热量 热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法中正确的是
| A.甲烷燃烧时只有化学能转化为热能 |
| B.轮船在海水中发生的腐蚀主要是析氢腐蚀 |
C.反应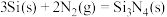 能自发进行,则该反应为放热反应 能自发进行,则该反应为放热反应 |
| D.常温下,pH=2的醋酸溶液与pH=12的NaOH溶液混合后溶液呈酸性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知Zn(s)+H2SO4(sq)===ZnSO4(aq)+H2(g) ΔH<0,则下列叙述不正确 的是( )
| A.该反应的化学能可以转化为电能 |
| B.该反应的ΔH值与反应方程式的化学计量数有关 |
| C.该反应的反应物的总能量高于生成物的总能量 |
| D.该反应中反应物的化学键断裂放出能量,生成物化学键形成吸收能量 |
您最近一年使用:0次

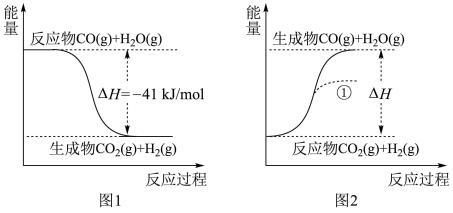
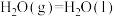
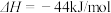
 的状态为液态,则能量变化曲线可能为①
的状态为液态,则能量变化曲线可能为①