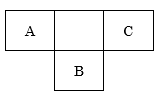
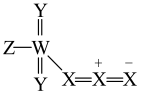短周期元素A、B、C,在周期表中所处的位置如图所示。A、B、C三种元素原子质子数之和为32。D元素原子的最外层电子数为其次外层电子数的2倍。则下列说法正确的是
| A.元素D形成的气态氢化物一定是正四面体型分子 |
| B.B、C两种元素可形成BC6型化合物,该化合物在空气中能燃烧 |
| C.四种元素形成的气态氢化物中,C元素形成的氢化物的稳定性最大 |
| D.A、B两种元素的气态氢化物均能与它们对应的最高价氧化物对应的水化物发生反应,且反应类型相同 |
更新时间:2018/03/21 12:05:56
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知X、Y、Z、W为短周期元素,X的一种核素的质子数为8;Y和Ne原子的核外电子数相差1;Z的单质是一种常见的半导体材料;W的非金属性在同周期元素中最强。其原子半径随原子序数变化如图所示。

下列说法正确的是

下列说法正确的是
| A.对应简单离子半径:W>Y>X |
| B.对应气态氢化物的稳定性:Z>W |
| C.化合物YWX中既含离子键,又含共价键 |
| D.Z的氧化物能与W的气态氢化物、Y的最高价氧化物对应水化物的溶液反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】运用元素周期律分析下面的推断,其中错误的是
| A.硝酸钫是离子化合物,易溶于水 | B.硫酸锶(SrSO4)是难溶于水晶体 |
| C.砹(At)为有色固体,HAt不稳定,AgAt感光性很强,且不溶于水也不溶于酸 | D.硒化氢(H2Se)是无色、有毒且比硫化氢稳定的气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下表中的实验操作能达到实验目的或能得出相应结论的是
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向淀粉KI溶液通入某有色气体,溶液变蓝 | 该气体一定为 |
| B | 若弱酸的酸性: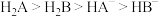 ,向0.1 mol·L-1 ,向0.1 mol·L-1  溶液中滴加少量等浓度的 溶液中滴加少量等浓度的 溶液 溶液 | 不会发生反应 |
| C | 向 溶液中通入少量氯气,然后再加入少量苯,振荡,静置,溶液分层,上层呈橙红色 溶液中通入少量氯气,然后再加入少量苯,振荡,静置,溶液分层,上层呈橙红色 | 氧化性: |
| D | 检验溴乙烷中溴元素 | 溴乙烷和NaOH溶液混合,振荡后加热,静置分层后,取少量上层清液,移入另一支试管中,加入2滴 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】化合物M是一种重要的化工原料,可作净水剂,化学式为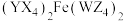 。其中,X、Y、Z、W是原子序数依次增大的短周期主族元素,
。其中,X、Y、Z、W是原子序数依次增大的短周期主族元素, 是含
是含 的微粒,Z的最外层电子数是次外层电子数的3倍,W形成的化合物是造成酸雨的主要原因之一。下列说法错误的是
的微粒,Z的最外层电子数是次外层电子数的3倍,W形成的化合物是造成酸雨的主要原因之一。下列说法错误的是
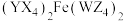 。其中,X、Y、Z、W是原子序数依次增大的短周期主族元素,
。其中,X、Y、Z、W是原子序数依次增大的短周期主族元素, 是含
是含 的微粒,Z的最外层电子数是次外层电子数的3倍,W形成的化合物是造成酸雨的主要原因之一。下列说法错误的是
的微粒,Z的最外层电子数是次外层电子数的3倍,W形成的化合物是造成酸雨的主要原因之一。下列说法错误的是| A.M具有还原性 | B.简单氢化物的沸点:Z>W |
| C.简单离子半径:W>Z>Y | D.M是含有共价键的离子化合物 |
您最近一年使用:0次


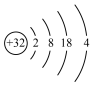
 、
、 、
、 、
、 的原子序数依次增大,Y和W位于同主族,一种化合物的结构如图所示。下列叙述正确的是
的原子序数依次增大,Y和W位于同主族,一种化合物的结构如图所示。下列叙述正确的是