化学科技工作者对含有碳杂质的金属铝的腐蚀与溶液酸碱性的关系进行了研究,在25℃时得出溶液pH值对铝的腐蚀影响关系如图所示,下列说法正确的是
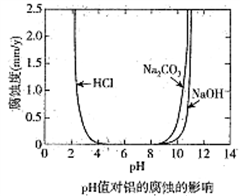

| A.金属铝在浓硫酸中的腐蚀速率大于盐酸中的腐蚀速率 |
| B.金属铝在中性环境中不易被腐蚀 |
| C.金属铝在pH=8.5的Na2CO3 溶液中会发生电化学腐蚀析出氧气 |
| D.不能用电解的方法在金属铝的表面生成致密的氧化物薄膜 |
2017·辽宁·一模 查看更多[5]
辽宁省百校联盟2018届高三TOP20十二月联考(Ⅱ卷)理综化学试题(已下线)黄金30题系列 高二化学(选修4) 小题好拿分【提升版】2017-2018学年第一学期期末复习备考之精准复习模拟题高三化学(单科)(C卷)(已下线)课时34 金属的腐蚀与防护-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第36练 金属的腐蚀与防护-2023年高考化学一轮复习小题多维练(全国通用)
更新时间:2017-12-24 12:49:58
|
【知识点】 金属的电化学腐蚀与防护
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】宝鸡被誉为“青铜器之乡”,出土了大盂鼎、毛公鼎、散氏盘等五万余件青铜器。研究青铜器(含Cu、Sn等)在潮湿环境中发生的腐蚀对于文物保护和修复有重要意义。下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图,下列说法不正确的是
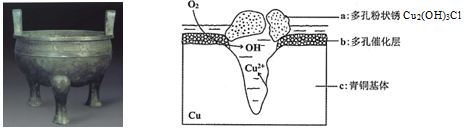

| A.青铜器发生电化学腐蚀,图中c作负极,被氧化 |
| B.正极发生的电极反应为O2+ 4e-+2H2O=4OH- |
| C.环境中的Cl-与正、负两极反应的产物作用生成a的离子方程式为2Cu2++3OH-+Cl-=Cu2 (OH)3Cl↓ |
| D.若生成0.2 mol Cu2(OH)3Cl,则理论上消耗的O2体积为4.48L |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】结合图判断,下列叙述正确的是


| A.I和II中正极均被保护 |
| B.I和II中负极反应均是Fe-2e-=Fe2+ |
| C.I和II中正极反应均是O2+2H2O+4e-=4OH- |
| D.I和II中分别加入少量氯水和KSCN溶液均变红色 |
您最近一年使用:0次

 ,可减少
,可减少 及温室气体的排放
及温室气体的排放

