下列有关各装置图的叙述,正确的是
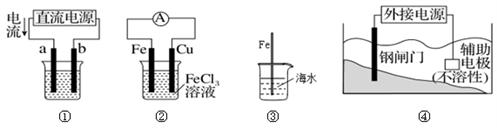

| A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 |
| B.装置②的总反应式:Cu+2Fe3+==Cu2++2Fe2+ |
| C.装置③中插入海水中的铁棒,越靠近底端腐蚀越严重 |
| D.装置④中钢闸门应与外接电源的负极相连被保护,该方法叫做牺牲阳极的阴极保护法 |
更新时间:2018-01-27 17:41:34
|
相似题推荐
【推荐1】下列有关电极反应的书写中,错误的是
A.氯碱工业电解装置中,阳极上的电极反应: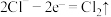 |
B.粗铜精炼时,阴极上的电极反应: |
C.钢铁发生电化学腐蚀时,负极上的电极反应: |
D.碱性氢氧燃料电池中,正极上的电极反应: |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】电镀是应用电解原理在某些金属表面镀上一薄层其他金属的方法。下列叙述错误的是
| A.电镀铜时,只能选用氯化铜溶液作电解质溶液 |
| B.镀层金属通常是在空气或溶液里不易起变化的金属或合金 |
| C.电镀的方法可以应用在铜的精炼上 |
| D.电镀的主要目的之一是使金属增强抗腐蚀的能力 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列由实验事实所得出的结论正确的是
| 选项 | 实验事实 | 结论 |
| A | 电解精炼铜时,粗铜作阳极,CuSO4溶液作电解质溶液,阴极析出精铜 | 电解质溶液中铜离子的浓度减小 |
| B | 向饱和NaHCO3溶液中加入CaCl2溶液,溶液变浑浊 | 溶液中c(Ca2+)·c(CO32-)<Ksp(CaCO3) |
| C | 室温下,用pH试纸测得0.1mol/LNaHSO3溶液的pH约为5 | HSO3-在水溶液中的水解程度大于其电离程度 |
| D | 由M、N与稀硫酸构成的原电池中,M上产生大量气泡 | 金属性:M>N |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】如图所示,各烧杯中均盛有海水,铁在其中的腐蚀速率由快到慢的顺序为


| A.②>①>③>④>⑤>⑥ | B.⑤>④>③>①>②>⑥ |
| C.⑤>④>②>①>③>⑥ | D.⑤>③>②>④>①>⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.电解质溶液的导电过程就是电解质溶液被电解的过程 |
| B.电解盐酸、硫酸溶液等,H+放电,溶液的pH逐渐增大 |
| C.根据得失电子守恒可知电解精炼铜时,阳极减少的质量和阴极增加的质量相等 |
| D.在船体外嵌入锌块,可以减缓船体的腐蚀,属于牺牲阴极的保护法 |
您最近一年使用:0次



