已知25℃、101kPa条件下:
①4Al(s)+3O2(g) 2Al2O3(s) ΔH=-2834.9 kJ•mol-1
2Al2O3(s) ΔH=-2834.9 kJ•mol-1
②4Al(s)+2O3(g) 2Al2O3(s) ΔH=-3119.1 kJ•mol-1
2Al2O3(s) ΔH=-3119.1 kJ•mol-1
由此得出的正确结论是
①4Al(s)+3O2(g)
 2Al2O3(s) ΔH=-2834.9 kJ•mol-1
2Al2O3(s) ΔH=-2834.9 kJ•mol-1②4Al(s)+2O3(g)
 2Al2O3(s) ΔH=-3119.1 kJ•mol-1
2Al2O3(s) ΔH=-3119.1 kJ•mol-1由此得出的正确结论是
| A.O3比O2稳定,由O2变O3为放热反应 |
| B.由反应①可确定铝的燃烧热是708.7kJ |
| C.等质量的O2比O3能量低,O2变O3为吸热反应 |
| D.由反应②可确定铝的燃烧热是779.78 kJ•mol-1 |
2018高二上·全国·专题练习 查看更多[1]
(已下线)2018年12月17日 《每日一题》人教选修4-吸热反应与放热反应的判断
更新时间:2018-12-20 07:58:43
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】已知某些化学键键能如下,下列说法不正确 的是
| 化学键 |  |  |  |  |  |
键能/kJ·mol | 436 | 243 | 194 | 432 | a |
A.根据键能可估算反应 的 的 kJ·mol kJ·mol |
| B.根据原子半径可知键长:H—Cl<H—Br,进而推测a<432 |
| C.可以根据H—Cl和H—Br的键能大小判断HCl和HBr的稳定性 |
D.常温下 和 和 的状态不同,与Cl—Cl和Br—Br的键能有关 的状态不同,与Cl—Cl和Br—Br的键能有关 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】关于热化学方程式,下列说法正确的是
A.标准状况下,2gH2完全燃烧生成液态水,放出热量285.8kJ,则表示H2燃烧热的热化学方程式为:  |
B.向50mL 0.5mol/L盐酸中加入50mL 0.55mol/L氢氧化钠溶液测得放出热量QkJ,则该反应的热化学方程式为: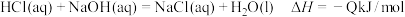 |
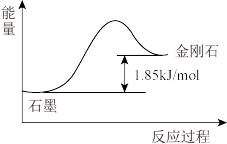
C.C(石墨,s)=C(金刚石s)  ,则石墨比金刚石稳定 ,则石墨比金刚石稳定 |
D.一定条件下,1mol碘蒸气和1mol H2充分混合反应生成HI并放热9.48kJ,则该反应的热化学方程式为: |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列有关说法正确的是
A.铅蓄电池放电时负极反应式:  |
| B.在航海轮船船底外壳焊上少量铜块,可以防止海轮腐蚀 |
C.已知: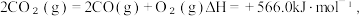 则CO 的燃烧热为566.0kJ·mol-1 则CO 的燃烧热为566.0kJ·mol-1 |
| D.在铜器上镀银时,把镀层金属银与电源正极相连,铜器与电源负极相连 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知碳的燃烧热为393.5kJ•mol-1,氢气的燃烧热为285.8kJ•mol-1,一氧化碳的燃烧热为283.0kJ•mol-1。某同学发现在灼热的煤炭上洒少量水,煤炉中会产生淡蓝色火焰,煤炭燃烧更旺。下列有关说法正确的是
A.氢气燃烧热的热化学方程式为H2(g)+ O2(g)=H2O(g) △H=-285.8kJ•mol-1 O2(g)=H2O(g) △H=-285.8kJ•mol-1 |
B.反应C(s)+ O2(g)=CO(g)的△H<-393.5kJ•mol-1 O2(g)=CO(g)的△H<-393.5kJ•mol-1 |
| C.“煤炭燃烧得更旺”是因为少量固体碳与水反应生成了可燃性气体 |
| D.C(s)+H2O(g)=CO(g)+H2(g) △H=175.3kJ•mol-1 |
您最近一年使用:0次