利用下图装置测定中和热的实验步骤如下:
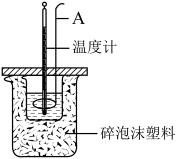
①量取50mL 0.25mol/L H2SO4溶液倒入小烧杯中,测量温度;
②量取50mL 0.55mol/L NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度。请回答:
(1)如图所示,仪器A的名称是_______________ ;
(2)NaOH溶液稍过量的原因______________ 。
(3)加入NaOH溶液的正确操作是_______ (填字母)。
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(4)使硫酸与NaOH溶液混合均匀的正确操作是_________________________ 。
(5)实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)______
a.实验装置保温、隔热效果差
b.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度

①量取50mL 0.25mol/L H2SO4溶液倒入小烧杯中,测量温度;
②量取50mL 0.55mol/L NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度。请回答:
(1)如图所示,仪器A的名称是
(2)NaOH溶液稍过量的原因
(3)加入NaOH溶液的正确操作是
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(4)使硫酸与NaOH溶液混合均匀的正确操作是
(5)实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)
a.实验装置保温、隔热效果差
b.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
更新时间:2019-01-14 18:47:50
|
【知识点】 中和热的测定与误差分析解读
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】(Ⅰ).2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。
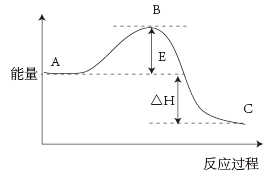
已知1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ•mol-1.请回答下列问题:
(1)E的大小对该反应的反应热______ (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点 ______ (填“升高”还是“降低”)。
(2)完成SO2氧化为SO3的热化学方程式____________________ 。
(Ⅱ).用 50mL0.50mol/L 盐酸与 50mL0.55mol/LNaOH 溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
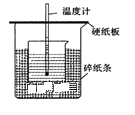
(1)从实验装置上看,图中尚缺少的一种玻璃用品是_____________ 。实验中能否用环形铜丝搅拌棒代替该用品 _______ (填“能”或“否”)
(2)向盐酸溶液中加入NaOH溶液的正确操作是_______ (从下列选出)。
A.沿玻璃棒缓慢倒入 B.一次迅速倒入 C.分三次少量倒入
(3)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会_____ (填“偏大”、“偏小”、“无影响”)。
(4)小明利用上述装置做实验,测得中和热的数值偏低,请你分析可能的原因是___ 。
A.测量完盐酸的温度再次测量NaOH溶液温度时,温度计上残留的酸液未用水冲洗干净。
B.做本实验的当天室温较高
C.大小烧杯口不平齐,小烧杯口未接触硬纸板。
D.大烧杯的盖板中间小孔太大

已知1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ•mol-1.请回答下列问题:
(1)E的大小对该反应的反应热
(2)完成SO2氧化为SO3的热化学方程式
(Ⅱ).用 50mL0.50mol/L 盐酸与 50mL0.55mol/LNaOH 溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是
(2)向盐酸溶液中加入NaOH溶液的正确操作是
A.沿玻璃棒缓慢倒入 B.一次迅速倒入 C.分三次少量倒入
(3)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会
(4)小明利用上述装置做实验,测得中和热的数值偏低,请你分析可能的原因是
A.测量完盐酸的温度再次测量NaOH溶液温度时,温度计上残留的酸液未用水冲洗干净。
B.做本实验的当天室温较高
C.大小烧杯口不平齐,小烧杯口未接触硬纸板。
D.大烧杯的盖板中间小孔太大
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol。回答有关中和反应的问题。
(1)用0.1 mol Ba(OH)2配成稀溶液与足量稀硝酸反应,能放出______ kJ热量。
(2)如图装置中仪器A的名称_____ ,作用是_______ ,碎泡沫塑料的作用是___________ 。
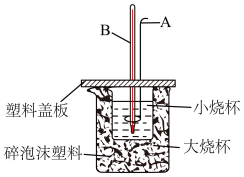
(3)若通过实验测定中和热的ΔH,其结果常常大于-57.3 kJ/mol,其原因可能是____________ 。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得中和热的数值会________ (填“偏大”、“偏小”或“无影响”)。
(1)用0.1 mol Ba(OH)2配成稀溶液与足量稀硝酸反应,能放出
(2)如图装置中仪器A的名称

(3)若通过实验测定中和热的ΔH,其结果常常大于-57.3 kJ/mol,其原因可能是
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得中和热的数值会
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某学习小组研究NaOH与某些酸之间的反应。
Ⅰ.中和热的测定
在25℃、101kPa条件下,强酸与强碱的稀溶液中和热可表示为:H+(aq)+OH─(aq)=H2O(l) △H=-57.3kJ ·mol-1。按照图1所示装置进行实验。

(1)仪器A的名称是________ 。
(2)碎泡沫塑料的作用是________ 。
(3)在25℃、101kPa条件下,取50mL 0.50 mol·L-1 CH3COOH溶液、50mL 0.55 mol·L-1 NaOH溶液进行实验,测得的中和热△H________ -57. 3 kJ ·mol-1(填“>”“=”或“<”),原因是 ________ 。
Ⅱ.中和滴定
(1)用_______ 量取20.00 mL待测稀盐酸溶液放入锥形瓶中,并滴加1~2滴酚酞作指示剂,用0.20 mol·L—1NaOH标准溶液进行滴定。为了减小实验误差,该同学一共进行了三次实验,假设每次所取稀盐酸体积均为20.00 mL,三次实验结果记录如下:
该盐酸的浓度约为________ (保留两位有效数字)。滴定达到终点的标志是________ 。
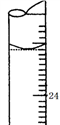
(2)若某次滴定结束时,滴定管液面如图2所示,则终点读数为________ mL。
Ⅰ.中和热的测定
在25℃、101kPa条件下,强酸与强碱的稀溶液中和热可表示为:H+(aq)+OH─(aq)=H2O(l) △H=-57.3kJ ·mol-1。按照图1所示装置进行实验。

(1)仪器A的名称是
(2)碎泡沫塑料的作用是
(3)在25℃、101kPa条件下,取50mL 0.50 mol·L-1 CH3COOH溶液、50mL 0.55 mol·L-1 NaOH溶液进行实验,测得的中和热△H
Ⅱ.中和滴定
(1)用
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 19.00 | 23.00 | 23.02 |
(2)若某次滴定结束时,滴定管液面如图2所示,则终点读数为

您最近半年使用:0次



