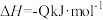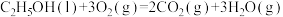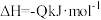对热化学方程式H2(g) + I2(g) = 2HI(g);△H = +52kJ·mol-1的叙述中,正确的是
| A.1mol氢气和1mol碘蒸气完全反应需要吸收26kJ热量 |
| B.1个氢分子和1个碘分子完全反应需要吸收52kJ热量 |
| C.1molH2(g)与1molI2(g)完全反应生成2mol HI气体需吸收52kJ热量 |
| D.1molH2(g)与1molI2(g)完全反应放出26kJ热量 |
更新时间:2019-06-23 18:53:06
|
【知识点】 热化学方程式
相似题推荐
单选题
|
较易
(0.85)
【推荐1】键能为破坏1mol化学键所需要吸收的能量或形成1mol化学键所放出的能量。已知H—H的键能为436kJ/mol,H—Cl的键能为432kJ/mol,氢气与氯气反应时放出热量。据此判断,下列说法不正确的是
| A.H2分子比H原子更稳定 |
| B.可求出Cl—Cl 的键能为428 kJ/mol |
| C.1mol氢气与1mol氯气所含的总能量比2mol HCl所含的总能量高 |
| D.理论上利用此反应制取盐酸的同时,可依据原电池原理获取电能 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】1g H2完全燃烧生成液态水放出a kJ的热量,下列热化学方程式正确的是
| A.H2(g)+ 1/2O2(g)= H2O(l)△H =-akJ.mol-1 |
| B.2H2(g) + O2(g) = 2H2O(l)△H =-4akJ.mol-1 |
| C.2H2(g) + O2(g) = 2H2O(l)△H =+4akJ.mol-1 |
| D.H2(g) + 1/2 O2(g) = H2O(g) △H =-2akJ.mol-1 |
您最近半年使用:0次

 与足量澄清石灰水反应得到100g沉淀,则表示乙醇燃烧的热化学方程式是
与足量澄清石灰水反应得到100g沉淀,则表示乙醇燃烧的热化学方程式是