写出该反应的热化学方程式。
1 mol氢气完全燃烧生成液态水放出285.8 kJ热量______________________________
1 mol氢气完全燃烧生成液态水放出285.8 kJ热量
更新时间:2019-06-24 22:45:23
|
【知识点】 热化学方程式
相似题推荐
填空题
|
容易
(0.94)
解题方法
【推荐1】煤燃烧的反应热可通过以下两个途径来利用:a.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧;b.利用煤在充足的空气中直接燃烧产生的反应热。这两个过程的热化学方程式为:
a.C(s)+H2O(g)=CO(g)+H2(g) ΔH=E1 ①
H2(g)+ O2(g)=H2O(g) ΔH=E2 ②
O2(g)=H2O(g) ΔH=E2 ②
CO(g)+ O2(g)=CO2(g) ΔH=E3 ③
O2(g)=CO2(g) ΔH=E3 ③
b.C(s)+O2(g)=CO2(g) ΔH=E4 ④
(1)上述四个热化学方程式中ΔH>0的反应有___________ (填序号)。
(2)理论上等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是___________。
(3)根据能量守恒定律,E1、E2、E3、E4之间的关系为___________ 。
a.C(s)+H2O(g)=CO(g)+H2(g) ΔH=E1 ①
H2(g)+
 O2(g)=H2O(g) ΔH=E2 ②
O2(g)=H2O(g) ΔH=E2 ②CO(g)+
 O2(g)=CO2(g) ΔH=E3 ③
O2(g)=CO2(g) ΔH=E3 ③b.C(s)+O2(g)=CO2(g) ΔH=E4 ④
(1)上述四个热化学方程式中ΔH>0的反应有
(2)理论上等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是___________。
| A.a与b相同 | B.a比b少 | C.a比b多 | D.两者无法比较 |
您最近半年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】意义
热化学方程式不仅表示化学反应中的___________ 变化,也表示了___________ 变化。还说明了物质的“量”与“能量”之间的数量关系。H2(g)+ O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1表示的意义是在25 ℃、101 kPa下,
O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1表示的意义是在25 ℃、101 kPa下,___________ 气态H2与___________ 气态O2反应生成___________ 时,___________ 的热量是285.8 kJ。
热化学方程式不仅表示化学反应中的
 O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1表示的意义是在25 ℃、101 kPa下,
O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1表示的意义是在25 ℃、101 kPa下,
您最近半年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐3】(1)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:
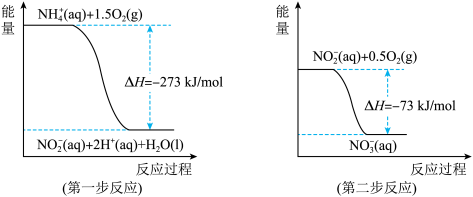
①第一步反应是________ (填“放热”或“吸热”)反应,判断依据是______________ 。
②1molNH4+(aq)全部氧化成NO3- (aq)的热化学方程式是____________________ 。

(2)如图所示是101kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,此反应的热化学方程式为_____________ 。

①第一步反应是
②1molNH4+(aq)全部氧化成NO3- (aq)的热化学方程式是

(2)如图所示是101kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,此反应的热化学方程式为
您最近半年使用:0次



