氨在工农业生产中应用广泛。在压强为30MPa时,不同温度时合成氨平衡混合气体中NH3的体积分数如下:
请回答:
(1)根据图中所示,合成氨的热化学方程式为___ 。
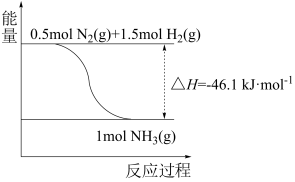
(2)将1molN2(g)和3molH2(g)通入一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量___ 92.2kJ(填“大于”“等于”或“小于”),原因是___ ;若加入催化剂,ΔH___ (填“变大”“变小”或“不变”)。
(3)已知破坏1molN≡N键、1molH—H键需要吸收的能量分别为946kJ、436kJ,则破坏1molN—H键需要吸收的能量为___ kJ。
(4)N2H4可视为NH3分子中的一个H被—NH2取代的产物。发射卫星用N2H4(g)为燃料,以NO2为氧化剂发生反应生成N2和H2O(g)。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ·mol-1。
则1molN2H4与NO2完全反应的热化学方程式为___ 。
| 温度/℃ | 200 | 300 | 400 | 500 | 600 |
| 氨含量/% | 89.9 | 71.0 | 47.0 | 26.4 | 13.8 |
(1)根据图中所示,合成氨的热化学方程式为

(2)将1molN2(g)和3molH2(g)通入一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量
(3)已知破坏1molN≡N键、1molH—H键需要吸收的能量分别为946kJ、436kJ,则破坏1molN—H键需要吸收的能量为
(4)N2H4可视为NH3分子中的一个H被—NH2取代的产物。发射卫星用N2H4(g)为燃料,以NO2为氧化剂发生反应生成N2和H2O(g)。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ·mol-1。
则1molN2H4与NO2完全反应的热化学方程式为
更新时间:2019-12-06 13:26:19
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】Ⅰ.已知下列热化学方程式:
①2C(s)+O2(g)=2CO(g) ΔH=-220.0 kJ•mol-1;
②C(s)+O2(g)=CO2(g) ΔH =-393.5 kJ•mol-1;
③2CO(g)+O2(g)=2CO2(g) ΔH =-566.0 kJ•mol-1;
④CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH =-890.0 kJ•mol-1。
请回答下列问题:
(1)CO的燃烧热为________________ 。
(2)炽热的木炭与二氧化碳反应生成一氧化碳的反应为___ (填“放热”或“吸热”)反应,理由是____________ 。
(3)写出甲烷与氧气反应生成CO的热化学方程式:_________________________ 。
Ⅱ.常温常压下,一定质量的无水乙醇(C2H5OH)完全燃烧时放出热量Q kJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100 g CaCO3沉淀,请写出乙醇燃烧的热化学方程式__________________________ 。
①2C(s)+O2(g)=2CO(g) ΔH=-220.0 kJ•mol-1;
②C(s)+O2(g)=CO2(g) ΔH =-393.5 kJ•mol-1;
③2CO(g)+O2(g)=2CO2(g) ΔH =-566.0 kJ•mol-1;
④CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH =-890.0 kJ•mol-1。
请回答下列问题:
(1)CO的燃烧热为
(2)炽热的木炭与二氧化碳反应生成一氧化碳的反应为
(3)写出甲烷与氧气反应生成CO的热化学方程式:
Ⅱ.常温常压下,一定质量的无水乙醇(C2H5OH)完全燃烧时放出热量Q kJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100 g CaCO3沉淀,请写出乙醇燃烧的热化学方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】I.写出下列反应的热化学方程式。
(1)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是_____________________ 。
(2)在1.01×105 Pa时,16 g S固体在足量的氧气中充分燃烧生成二氧化硫,放出148.5 kJ的热量,则S固体燃烧热的热化学方程式为________________________ 。
II.研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(3)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S固体。已知:
①CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是_____________________ 。
(4)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
若用标准状况下3.36 L CO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为________ mol,放出的热量为______________ kJ(用含有a和b的代数式表示)。
(1)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是
(2)在1.01×105 Pa时,16 g S固体在足量的氧气中充分燃烧生成二氧化硫,放出148.5 kJ的热量,则S固体燃烧热的热化学方程式为
II.研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(3)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S固体。已知:
①CO(g)+
 O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是
(4)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
若用标准状况下3.36 L CO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】“西气东输”是我国开发的重点工程,这里的气是指天然气,其主要成分是甲烷。工业上将碳与水在高温下反应制得水煤气,水煤气的主要成分是CO和H2,二者的体积比为1:1。已知1 molCO气体完全燃烧生成CO2气体放出282. 6kJ热量; 1mol氢气完全燃烧生成液态水放出285. 8kJ热量;1molCH4气体完全燃烧生成CO2气体和液态水放出889. 6kJ热量。
(1)写出氢气完全燃烧生成液态水的热化学方程式:_________ 。
(2)若1molCH4 气体完全燃烧生成CO2气体和水蒸气, 放出的热量______ (填“大于”“等于”或“小于”)889. 6kJ。
(3)忽略水煤气中其他成分,相同状况下若得到相等的热量,所需水煤气与甲烷的体积比约为________ (整数比)。
(1)写出氢气完全燃烧生成液态水的热化学方程式:
(2)若1molCH4 气体完全燃烧生成CO2气体和水蒸气, 放出的热量
(3)忽略水煤气中其他成分,相同状况下若得到相等的热量,所需水煤气与甲烷的体积比约为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】能源是人类生存和发展的重要支柱,研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义,已知下列热化学方程式:
①H2(g)+ O2(g)= H2O( g) ΔH = - 242kJ/mol;
O2(g)= H2O( g) ΔH = - 242kJ/mol;
②2H2(g)+ O2(g)= 2H2O( l) ΔH= - 572kJ/mol;
③C(s)+ O2(g)=CO (g) ΔH =-110.5 kJ/mol;
O2(g)=CO (g) ΔH =-110.5 kJ/mol;
④C(s)+O2(g)= CO2(g) ΔH=- 393.5 kJ/mol;
⑤CO2(g)+2H2O(g)= CH4(g)+ 2O2( g) ΔH = + 802kJ/mol:
回答下列问题
(1)写出能表示H2燃烧热的热化学方程式___________ ;
(2)已知C(s)+ H2O(g) H2(g)+ CO(g) ΔH =
H2(g)+ CO(g) ΔH =_______ kJ/mol;
(3)估算出C=O键能为____ kJ/mol:
(4)CH4的燃烧热ΔH =_______ kJ/mol:
(5)25℃、101kPa下,某燃具中CH4的燃烧效率是90%(注:相当于10%的CH4未燃烧),水壶的热量利用率是70%,则用此燃具和水壶,烧开 1L 水所需要的CH4的物质的量为_____ mol[保留到小数点后2位:已知:c(H2O)=4.2J/(g•℃)]。
①H2(g)+
 O2(g)= H2O( g) ΔH = - 242kJ/mol;
O2(g)= H2O( g) ΔH = - 242kJ/mol;②2H2(g)+ O2(g)= 2H2O( l) ΔH= - 572kJ/mol;
③C(s)+
 O2(g)=CO (g) ΔH =-110.5 kJ/mol;
O2(g)=CO (g) ΔH =-110.5 kJ/mol; ④C(s)+O2(g)= CO2(g) ΔH=- 393.5 kJ/mol;
⑤CO2(g)+2H2O(g)= CH4(g)+ 2O2( g) ΔH = + 802kJ/mol:
| 化学键 | O=O | C-C | H-H | O-O | C-O | O-H | C-H |
| 键能 kJ/mol | 497 | 348 | 436 | 142 | 351 | 463 | 414 |
(1)写出能表示H2燃烧热的热化学方程式
(2)已知C(s)+ H2O(g)
 H2(g)+ CO(g) ΔH =
H2(g)+ CO(g) ΔH =(3)估算出C=O键能为
(4)CH4的燃烧热ΔH =
(5)25℃、101kPa下,某燃具中CH4的燃烧效率是90%(注:相当于10%的CH4未燃烧),水壶的热量利用率是70%,则用此燃具和水壶,烧开 1L 水所需要的CH4的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)沼气是一种能源,它的主要成分是CH4,常温下,0.5molCH4完全燃烧生成CO2(g)和液态水时,放出445kJ热量,则热化学方程式为__ 。
(2)已知: N2(g)+
N2(g)+ H2(g)=N(g)+3H(g) ΔH1=+akJ·mol-1
H2(g)=N(g)+3H(g) ΔH1=+akJ·mol-1
N(g)+3H(g)=NH3(g) ΔH2=-bkJ·mol-1
NH3(g)=NH3(l) ΔH3=-ckJ·mol-1
写出N2(g)和H2(g)反应生成液氨的热化学方程式__ 。
(3)SF6是一种优良的绝缘气体,分子结构中,只存在S-F键,已知1molS(s)转化为气态硫原子吸收能量280kJ,F-F键能为160kJ·mol-1,S-F键能为330kJ·mol-1,试写出S(s)和F2(g)反应生成SF6(g)的热化学方程式__ 。
(2)已知:
 N2(g)+
N2(g)+ H2(g)=N(g)+3H(g) ΔH1=+akJ·mol-1
H2(g)=N(g)+3H(g) ΔH1=+akJ·mol-1N(g)+3H(g)=NH3(g) ΔH2=-bkJ·mol-1
NH3(g)=NH3(l) ΔH3=-ckJ·mol-1
写出N2(g)和H2(g)反应生成液氨的热化学方程式
(3)SF6是一种优良的绝缘气体,分子结构中,只存在S-F键,已知1molS(s)转化为气态硫原子吸收能量280kJ,F-F键能为160kJ·mol-1,S-F键能为330kJ·mol-1,试写出S(s)和F2(g)反应生成SF6(g)的热化学方程式
您最近一年使用:0次
【推荐3】氢气作为一种清洁能源,一直是能源研究的热点,工业上制取氢气有多种方法:
①C(s)+H2O(g)=CO(g)+H2(g) △H1=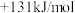
②CH4 (g)+CO2(g)=2CO(g)+2H2 (g) △H2=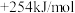
③CH4 (g)+H2O(g)=CO(g)+3H2 (g) △H3=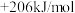
④CH3OH(1)=CO(g)+2H2 (g) △H4=
(1)根据以上数据,请写出CH4(g)分解生成C(s)和H2(g)的热化学方程式______ 。
(2)几种化学键的键能如下表所示:
根据以上有关反应的△H,计算 x=______ 。
(3)我国科学家通过计算机模拟,研究了在某催化剂表面上发生反应④的反应历程(吸附在催化剂表面的物质,用"*"标注)。甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式Ⅰ: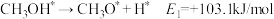
方式Ⅱ:
活化能E值推测,甲醇脱氢过程中主要历程的方式为______ (填"Ⅰ"或"Ⅱ")。计算机模拟的各步反应的能量变化示意图如下。

该历程中最大能垒(活化能)E正=______ kJ/mol,写出该步骤的化学方程式______ 。
①C(s)+H2O(g)=CO(g)+H2(g) △H1=
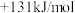
②CH4 (g)+CO2(g)=2CO(g)+2H2 (g) △H2=
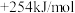
③CH4 (g)+H2O(g)=CO(g)+3H2 (g) △H3=
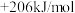
④CH3OH(1)=CO(g)+2H2 (g) △H4=

(1)根据以上数据,请写出CH4(g)分解生成C(s)和H2(g)的热化学方程式
(2)几种化学键的键能如下表所示:
| 化学键 | C=O | H—H | 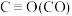 | C—H | O—H |
| 键能/kJ·mol-1 | 803 | 436 | x | 414 | 463 |
根据以上有关反应的△H,计算 x=
(3)我国科学家通过计算机模拟,研究了在某催化剂表面上发生反应④的反应历程(吸附在催化剂表面的物质,用"*"标注)。甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式Ⅰ:
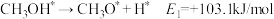
方式Ⅱ:

活化能E值推测,甲醇脱氢过程中主要历程的方式为

该历程中最大能垒(活化能)E正=
您最近一年使用:0次



