按要求写出下列方程式:
①碳酸氢钠在水中的电离方程式:__________________ 。
②碳酸钙与稀盐酸反应制二氧化碳气体的离子方程式:__________ 。
③硫酸铜溶液中加入氢氧化钡溶液的离子方程式:_______________ 。
①碳酸氢钠在水中的电离方程式:
②碳酸钙与稀盐酸反应制二氧化碳气体的离子方程式:
③硫酸铜溶液中加入氢氧化钡溶液的离子方程式:
更新时间:2019-12-13 22:10:36
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】高铁酸钠( )具有很强的氧化性,是一种优良的多功能水处理剂,工业上制备高铁酸钠有两种方法,主要反应原理如下:
)具有很强的氧化性,是一种优良的多功能水处理剂,工业上制备高铁酸钠有两种方法,主要反应原理如下:
①湿法制备:___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ (未配平)
(未配平)
②干法制备: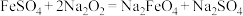
(1) 中Fe元素的化合价为
中Fe元素的化合价为___________ ,其在水溶液中的电离方程式为___________ 。
(2) 的电子式为
的电子式为___________ ,其与 反应的化学方程式为
反应的化学方程式为___________ 。
(3)配平反应①,并用“双线桥”标出中电子转移的方向和数目___________ 。该反应每生成1 mol  ,转移的电子数为
,转移的电子数为___________ 。
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________
(4)由反应②可知氧化性:
___________  (选填“<”或“>”)。
(选填“<”或“>”)。
(5) 在水中可被还原为
在水中可被还原为 ,其还原产物常用试剂
,其还原产物常用试剂___________ 检验。 可作为优良水处理剂的原因是
可作为优良水处理剂的原因是___________ 。
 )具有很强的氧化性,是一种优良的多功能水处理剂,工业上制备高铁酸钠有两种方法,主要反应原理如下:
)具有很强的氧化性,是一种优良的多功能水处理剂,工业上制备高铁酸钠有两种方法,主要反应原理如下:①湿法制备:___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ (未配平)
(未配平)②干法制备:
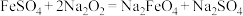
(1)
 中Fe元素的化合价为
中Fe元素的化合价为(2)
 的电子式为
的电子式为 反应的化学方程式为
反应的化学方程式为(3)配平反应①,并用“双线桥”标出中电子转移的方向和数目
 ,转移的电子数为
,转移的电子数为___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________
(4)由反应②可知氧化性:

 (选填“<”或“>”)。
(选填“<”或“>”)。(5)
 在水中可被还原为
在水中可被还原为 ,其还原产物常用试剂
,其还原产物常用试剂 可作为优良水处理剂的原因是
可作为优良水处理剂的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.物质的分类是学习化学的一种重要方法,有下列几种物质:①盐酸;② ;③
;③ ;④
;④ 溶液;⑤
溶液;⑤ ;⑥纯碱;⑦
;⑥纯碱;⑦ 。回答下列问题:
。回答下列问题:
(1)属于碱性氧化物的是_______ (填序号),属于盐类的是_______ (填序号)。
(2)写出⑦在熔融状态下的电离方程式:_______ 。
(3)写出少量③和④反应的离子方程式:_______ 。
Ⅱ.有以下四个反应:①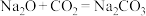 ;②
;② ;③
;③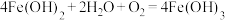 ;④
;④ 。
。
(4)属于复分解反应的是_______ (填序号,下同),既是化合反应又是氧化还原反应的是_______ 。
Ⅲ.单质到盐的转化关系可表示为:A(单质) B(氧化物)
B(氧化物) C
C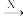 D(盐)。
D(盐)。
(5)若A是碳单质,则C的水溶液呈_______ (填“酸”“碱”或“中”)性。
(6)若B是一种淡黄色固体,X是 ,则B的用途是
,则B的用途是_______ (举一例),D的化学式可能是_______ 。
 ;③
;③ ;④
;④ 溶液;⑤
溶液;⑤ ;⑥纯碱;⑦
;⑥纯碱;⑦ 。回答下列问题:
。回答下列问题:(1)属于碱性氧化物的是
(2)写出⑦在熔融状态下的电离方程式:
(3)写出少量③和④反应的离子方程式:
Ⅱ.有以下四个反应:①
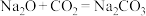 ;②
;② ;③
;③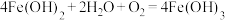 ;④
;④ 。
。(4)属于复分解反应的是
Ⅲ.单质到盐的转化关系可表示为:A(单质)
 B(氧化物)
B(氧化物) C
C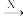 D(盐)。
D(盐)。(5)若A是碳单质,则C的水溶液呈
(6)若B是一种淡黄色固体,X是
 ,则B的用途是
,则B的用途是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有以下物质:①NaOH溶液;②液氨;③BaCO3固体;④熔融KHSO4;⑤Fe(OH)3胶体:⑥铝;⑦CO2;⑧CH3COOH;⑨蔗糖晶体
请回答下列问题:
(1)以上物质中属于混合物的是_______ (填序号),以上物质中属于电解质的是_______ (填序号);以上纯净物中能导电的是_______ (填序号)。
(2)写出④的电离方程式_______
(3)写出①和⑥反应的化学方程式_______
(4)在①溶液中缓缓通入过量的CO2可生成酸式盐,写出反应的化学方程式_______ 。
(5)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至液体呈红褐色,即制得Fe(OH)3胶体。写出该反应的化学方程式_______ 。
(6)下列叙述错误的是_______(填标号)。
请回答下列问题:
(1)以上物质中属于混合物的是
(2)写出④的电离方程式
(3)写出①和⑥反应的化学方程式
(4)在①溶液中缓缓通入过量的CO2可生成酸式盐,写出反应的化学方程式
(5)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至液体呈红褐色,即制得Fe(OH)3胶体。写出该反应的化学方程式
(6)下列叙述错误的是_______(填标号)。
| A.雾属于胶体,能产生丁达尔效应 |
| B.用盐卤点豆腐与胶体性质有关 |
| C.无法从颜色上区别FeCl3溶液和Fe(OH)3胶体 |
| D.工业静电除尘装置是根据胶体的性质设计的 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】①液态醋酸;②液氨;③Ba(OH)2溶液;④熔融AlCl3;⑤Fe(OH)3胶体;⑥镁;⑦CO2;⑧HI溶液;⑨蔗糖(C12H22O11)
(1)以上物质中属于电解质的是_______ (填序号);以上纯净物中能导电的是_______ (填序号)。
(2)写出⑥⑦反应的化学方程式:________ 。
(3)将34.2g蔗糖完全燃烧后的产物通过足量Na2O2,Na2O2增重_______ 34.2g(填“>”、“<”或“=”)。
(4)写出⑤和足量⑧反应的离子方程式________ 。
(1)以上物质中属于电解质的是
(2)写出⑥⑦反应的化学方程式:
(3)将34.2g蔗糖完全燃烧后的产物通过足量Na2O2,Na2O2增重
(4)写出⑤和足量⑧反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硅、硫、氮是重要的非金属元素。回答下列问题:
(1)SiO2属于___________ (填“酸性”“碱性”或“两性”)氧化物。盛装NaOH等碱性溶液的试剂瓶不能用玻璃塞,其原因为___________ (用化学方程式表示)。
(2)工业上用石英砂和焦炭混合高温制取粗硅,其反应的化学方程式为___________ ;硅的用途有___________ (任写1个)。
(3)由SO3制备H2SO4的过程中,一般用98.3%的浓硫酸吸收SO3,而不是直接用蒸馏水吸收的原因是___________ 。
(4)实验室利用含Fe3+的溶液吸收SO2,从而实现SO2的回收利用。写出Fe3+与SO2在水溶液中发生反应的离子方程式:___________ ;每消耗32gSO2,转移电子的物质的量为___________ mol。
(5)氨气遇氯化氢时会产生白烟,写出白烟化学成分的电子式:___________ 。
(1)SiO2属于
(2)工业上用石英砂和焦炭混合高温制取粗硅,其反应的化学方程式为
(3)由SO3制备H2SO4的过程中,一般用98.3%的浓硫酸吸收SO3,而不是直接用蒸馏水吸收的原因是
(4)实验室利用含Fe3+的溶液吸收SO2,从而实现SO2的回收利用。写出Fe3+与SO2在水溶液中发生反应的离子方程式:
(5)氨气遇氯化氢时会产生白烟,写出白烟化学成分的电子式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请按要求回答下列问题:
(1)写出苏打的化学式:___________ ;
(2)写出实验室制取氯气的离子反应方程式:___________ ;
(3)现有下列七种物质:①CaCO3;②CO2;③氯化铁溶液;④Ba(OH)2;⑤稀硫酸;⑥熔融KNO3;⑦Na。在上述物质中,能导电的是___________ ;属于电解质的是___________ 。
(4)工业废水中含有的重铬酸根离子( )有毒,必须处理达标后才能排放。工业上常用绿矾(
)有毒,必须处理达标后才能排放。工业上常用绿矾( )做处理剂,反应的离子方程式如下:
)做处理剂,反应的离子方程式如下: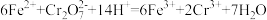
①在该反应中还原产物是___________ (填离子符号);
②用单线桥标出该反应电子转移的方向和数目___________ 。
(1)写出苏打的化学式:
(2)写出实验室制取氯气的离子反应方程式:
(3)现有下列七种物质:①CaCO3;②CO2;③氯化铁溶液;④Ba(OH)2;⑤稀硫酸;⑥熔融KNO3;⑦Na。在上述物质中,能导电的是
(4)工业废水中含有的重铬酸根离子(
 )有毒,必须处理达标后才能排放。工业上常用绿矾(
)有毒,必须处理达标后才能排放。工业上常用绿矾( )做处理剂,反应的离子方程式如下:
)做处理剂,反应的离子方程式如下: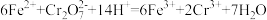
①在该反应中还原产物是
②用单线桥标出该反应电子转移的方向和数目
您最近一年使用:0次



