将煤直接作为燃料燃烧,不但热效率较低,且产生烟尘、二氧化硫、氮氧化物等物质,造成严重的环境污染。煤的干馏是提高煤的利用率、生产重要化工原料、降低污染物排放量的有效措施之一。某化学学习小组在实验室条件下探究煤干馏的现象及产物,装置如图所示,请回答有关问题:
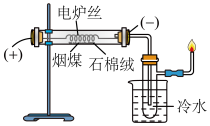
(1)煤干馏的条件是_______ 。
(2)盛有冷水的烧杯的作用是__________________
(3)实验后检验有粗氨水生成的操作是___
(4)已知CO不能使溴水褪色,若将从具支试管支管口处逸出的气体通入溴水中,发现溴水褪色,则说明煤的干馏产生了_______________________
(5)点燃尾气,火焰的颜色为________________________
(6)从煤焦油中分离出苯、甲苯、二甲苯的实验方法是_________________

(1)煤干馏的条件是
(2)盛有冷水的烧杯的作用是
(3)实验后检验有粗氨水生成的操作是
(4)已知CO不能使溴水褪色,若将从具支试管支管口处逸出的气体通入溴水中,发现溴水褪色,则说明煤的干馏产生了
(5)点燃尾气,火焰的颜色为
(6)从煤焦油中分离出苯、甲苯、二甲苯的实验方法是
19-20高一·全国·课时练习 查看更多[3]
8.1.2 煤、石油和天然气的综合利用——2020年春高一新人教版第二册化学一课一练2020年春高一化学新人教版第二册课后同步:8.1.2 煤、石油和天然气的综合利用(已下线)专题11 自然资源的开发利用(核心素养卷)-【新教材精创】2019-2020学年高一化学新教材知识讲学(必修第二册)
更新时间:2020/03/18 16:37:32
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】聚乙烯难以降解,处理不当会造成严重的“白色污染”。常见处理方法有填埋法、焚烧法与热裂解法等。
(1)聚乙烯安全无毒,可用于制食品包装袋。 工业合成聚乙烯的有机原料的电子式为____________ 。
(2)所有碳原子一定在同一 个平面上的 C5H10按照系统命名法命名为_________________ 。
(3)下列各物质中,一定是同系物的是___________ 。
A.CH4和C3H6 B. C3H6和C4H8
C. C2H2 和C4H6 D. C3H8和C4H10
(4)写出用焚烧法处理聚乙烯的化学方程式:____________________________________________ 。
(5)废旧塑料的热裂法处理方法如图:将废塑料隔绝空气加强热,使其变成有用的物质。实验装置如图所示。加热聚丙烯废塑料得到的产物如表:
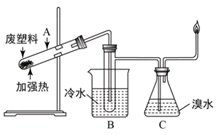
①试管A中残余物有多种用途,如利用下列转化制取高聚物聚乙炔。
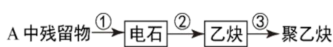
写出反应②、③的化学方程式:________________________________ 、__________________________ 。
②经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为_____________________ 。
(1)聚乙烯安全无毒,可用于制食品包装袋。 工业合成聚乙烯的有机原料的电子式为
(2)所有碳原子一定在同一 个平面上的 C5H10按照系统命名法命名为
(3)下列各物质中,一定是同系物的是
A.CH4和C3H6 B. C3H6和C4H8
C. C2H2 和C4H6 D. C3H8和C4H10
(4)写出用焚烧法处理聚乙烯的化学方程式:
(5)废旧塑料的热裂法处理方法如图:将废塑料隔绝空气加强热,使其变成有用的物质。实验装置如图所示。加热聚丙烯废塑料得到的产物如表:
产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |

①试管A中残余物有多种用途,如利用下列转化制取高聚物聚乙炔。

写出反应②、③的化学方程式:
②经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】概念辨析(括号内画“√”或“×”,正确的横线处不填,错误的说明原因)
(1)乙烯能使溴水和酸性高锰酸钾溶液褪色,发生的反应类型相同( ) _________ 。
(2)乙醇中混有的少量水可用金属钠进行检验( ) ____________ 。
(3)1 mol C2H5OH和1 mol CH3COOH在浓硫酸作用下加热可以完全反应生成1 mol CH3COOC2H5( ) _______________ 。
(4)淀粉、油脂、蛋白质都属于高分子化合物( ) ____________ 。
(1)乙烯能使溴水和酸性高锰酸钾溶液褪色,发生的反应类型相同
(2)乙醇中混有的少量水可用金属钠进行检验
(3)1 mol C2H5OH和1 mol CH3COOH在浓硫酸作用下加热可以完全反应生成1 mol CH3COOC2H5
(4)淀粉、油脂、蛋白质都属于高分子化合物
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】碳、氢元素可形成种类丰富的化合物,其中形成的A、B、C、D四种有机物结构模型如下:
(1)A模型的空间构型___________ ,键角为___________ ;其燃料电池在碱性环境中的负极反应式:___________ ;有机物B的电子式 ___________ ,C分子式为___________ 。
(2)有机物B使溴的四氯化碳溶液褪色的化学方程式为________ ,反应类型是___________ 。
(3) A、B、C三种有机物中,所有原子均共面的是________ (填名称)。
(4)等质量的四种有机物完全燃烧生成H2O和CO2,消耗氧气的体积(相同状况下)最大的是___________ (填分子式)。
A. B.
B. C.
C. D.
D.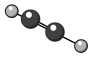
(1)A模型的空间构型
(2)有机物B使溴的四氯化碳溶液褪色的化学方程式为
(3) A、B、C三种有机物中,所有原子均共面的是
(4)等质量的四种有机物完全燃烧生成H2O和CO2,消耗氧气的体积(相同状况下)最大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】长期放置的 溶液易被氧化而变质,某兴趣小组进行了如下实验:
溶液易被氧化而变质,某兴趣小组进行了如下实验:
(1)设计实验检验 溶液的变质程度。
溶液的变质程度。
①上述方案补充完整_____ 、_____ 。
②若要使部分变质的 复原,方法是
复原,方法是___________ (用离子方程式表示)。
(2)利用部分变质的 溶液制备
溶液制备 。
。
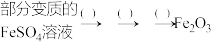
①“()”中所填是所需试剂或条件,分别为___________ 、___________ 、___________ 、“ ”中所填是含铁物质的化学式,分别是
”中所填是含铁物质的化学式,分别是___________ 、___________ (以离子形式存在的可写离子符号)。
②若 该变质溶液制得
该变质溶液制得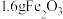 ,则变质前
,则变质前 溶液的浓度为
溶液的浓度为___________ 。
(3) 可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将
可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将 转化为
转化为 ,以利于人体吸收。为了验证这一猜想,设计了如下实验:
,以利于人体吸收。为了验证这一猜想,设计了如下实验:
由上述实验能否得出“维生素C可将 转化为
转化为 ”的结论?请说明理由:
”的结论?请说明理由:___________ 。
 溶液易被氧化而变质,某兴趣小组进行了如下实验:
溶液易被氧化而变质,某兴趣小组进行了如下实验:(1)设计实验检验
 溶液的变质程度。
溶液的变质程度。| 实验方案 | 步骤1 | 步骤2 |
取待检测液于试管中,向其中滴加 溶液 溶液 | 取待检测液于试管中,向其中滴加少量酸性高锰酸钾溶液 | |
| 实验现象 | ___________ | ___________ |
| 实验结论 |  溶液部分变质 溶液部分变质 | |
①上述方案补充完整
②若要使部分变质的
 复原,方法是
复原,方法是(2)利用部分变质的
 溶液制备
溶液制备 。
。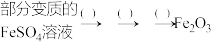
①“()”中所填是所需试剂或条件,分别为
 ”中所填是含铁物质的化学式,分别是
”中所填是含铁物质的化学式,分别是②若
 该变质溶液制得
该变质溶液制得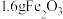 ,则变质前
,则变质前 溶液的浓度为
溶液的浓度为(3)
 可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将
可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将 转化为
转化为 ,以利于人体吸收。为了验证这一猜想,设计了如下实验:
,以利于人体吸收。为了验证这一猜想,设计了如下实验:| 实验方案 | 实验现象 |
取适量 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液 | 紫色褪去 |
由上述实验能否得出“维生素C可将
 转化为
转化为 ”的结论?请说明理由:
”的结论?请说明理由:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】1乙氧基萘是一种无色液体,密度比水的大,不溶于水,易溶于乙醇,熔点为5.5℃,沸点为267℃。1萘酚(性质与苯酚相似)的熔点为96℃,沸点为278℃,微溶于水,易溶于乙醇。乙醇的沸点为78.5℃。1乙氧基萘常用作香料,也可合成其他香料。实验室制备1乙氧基萘的反应原理如下:
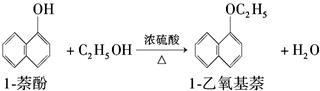
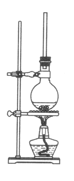
(1)将72g1萘酚溶于100mL无水乙醇中,再加入5mL浓硫酸。将混合溶液置于如图所示的圆底烧瓶中加热充分反应。实验中使用过量乙醇的原因是________ 。烧瓶上连接长玻璃管的主要作用是________________ 。
(2)反应结束后将烧瓶中的液体倒入冷水中,经处理得到有机层。为提纯产物有以下四步操作:①蒸馏;②水洗并分液;③用10%的NaOH溶液洗并分液;④用无水氯化钙干燥并过滤。正确的顺序是________ (填序号)。
A.③②④① B.①②③④ C.②①③④
(3)实验测得1乙氧基萘的产量与反应时间、温度的关系如图所示,时间延长、温度升高,1乙氧基萘的产量下降的原因可能是__________ 、____________ 。

(4)某同学推测经提纯的产品可能还含有1萘酚、乙醇、硫酸和水等杂质,设计了如下方案进行检验,请完成表中内容。

(1)将72g1萘酚溶于100mL无水乙醇中,再加入5mL浓硫酸。将混合溶液置于如图所示的圆底烧瓶中加热充分反应。实验中使用过量乙醇的原因是

(2)反应结束后将烧瓶中的液体倒入冷水中,经处理得到有机层。为提纯产物有以下四步操作:①蒸馏;②水洗并分液;③用10%的NaOH溶液洗并分液;④用无水氯化钙干燥并过滤。正确的顺序是
A.③②④① B.①②③④ C.②①③④
(3)实验测得1乙氧基萘的产量与反应时间、温度的关系如图所示,时间延长、温度升高,1乙氧基萘的产量下降的原因可能是

(4)某同学推测经提纯的产品可能还含有1萘酚、乙醇、硫酸和水等杂质,设计了如下方案进行检验,请完成表中内容。
| 实验目的 | 实验操作 | 预期现象和结论 |
| ①用金属钠检验1乙氧基萘是否纯净 | 取少量经提纯的产品于试管A中,加入金属钠 | 若 若 |
| ②检验经提纯的产品是否含有1萘酚 | 若 若 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】煤的综合利用有煤的干馏、气化等。煤干馏后可得到焦炭、煤焦油、粗氨水和焦炉气。
(1)焦炭可通过以下途径制取聚氯乙烯等化工产品(如下框图所示)
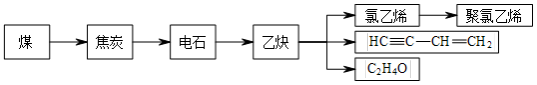
写出由氯乙烯制取聚氯乙烯的化学方程式___________ 。乙炔的结构简式为___________ ,随意丢弃聚氯乙烯制品会造成___________ 。
(2)从煤焦油中可以分离出一种重要的液态烃──苯,写出苯与溴在铁存在的情况下发生反应的化学方程式___________ ,该反应中反应物溴应该选用___________ (填“溴水”或“液溴”)。
(3)焦炉气具有可燃性,其主要成分是H2和___________ (该气体是最简单的烃)。
(1)焦炭可通过以下途径制取聚氯乙烯等化工产品(如下框图所示)

写出由氯乙烯制取聚氯乙烯的化学方程式
(2)从煤焦油中可以分离出一种重要的液态烃──苯,写出苯与溴在铁存在的情况下发生反应的化学方程式
(3)焦炉气具有可燃性,其主要成分是H2和
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】填空
(1)煤的气化——用来制取___________
①定义:___________
②反应方程式:___________
(2)煤的液化
①定义:___________
②反应方程式:___________
(3)煤的干馏
①定义:___________
②主要产物:___________
【科学史话】苯的发现之旅
(4)1825年,英国科学家法拉第在煤气灯中首先发现苯,并测得其含碳量,确定其最简式为CH;1834年,德国科学家米希尔里希制得苯,并将其命名为苯;之后,法国化学家日拉尔等确定其分子量为78,苯分子式为___________ 。
(1)煤的气化——用来制取
①定义:
②反应方程式:
(2)煤的液化
①定义:
②反应方程式:
(3)煤的干馏
①定义:
②主要产物:
【科学史话】苯的发现之旅
(4)1825年,英国科学家法拉第在煤气灯中首先发现苯,并测得其含碳量,确定其最简式为CH;1834年,德国科学家米希尔里希制得苯,并将其命名为苯;之后,法国化学家日拉尔等确定其分子量为78,苯分子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】煤是重要的能源,也是生产化工产品的重要原料。试用所学知识,解答下列问题:
(1)煤的转化技术包括煤的气化技术和液化技术。煤的液化技术又分为________ 和________ 。
(2)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理为FeS2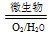 Fe2++SO42—
Fe2++SO42—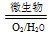 Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为
Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为_______________________ ,第二步反应的离子方程式为________________ 。
(3)工业煤干馏得到的产品有焦炭、________ 。
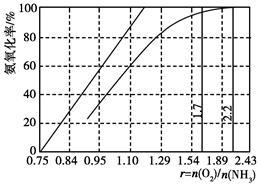
(4)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨-空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上r[n(O2)/n(NH3)]=________ ,实际生产要将r值维持在1.7~2.2之间,原因是__________________________________________ 。
(1)煤的转化技术包括煤的气化技术和液化技术。煤的液化技术又分为
(2)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理为FeS2
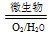 Fe2++SO42—
Fe2++SO42—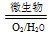 Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为
Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为(3)工业煤干馏得到的产品有焦炭、
(4)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨-空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上r[n(O2)/n(NH3)]=

您最近一年使用:0次