浙教版九年级上册 第一章 物质及其变化单元检测
全国
九年级
单元测试
2019-10-08
295次
整体难度:
适中
考查范围:
常见的物质、物质的运动与相互作用
一、选择题 添加题型下试题
| A.氧气用于急救病人 | B.干冰用于制冷剂 |
| C.稀有气体用于霓虹灯 | D.氦气用于磁悬浮列车 |
【知识点】 化学性质与物理性质的差别及应用
| A.牙膏或肥皂水 | B.食盐水 | C.火碱液 | D.食醋 |
【知识点】 中和反应及其应用 酸、碱的使用注意事项 溶液的酸碱性与pH值的关系
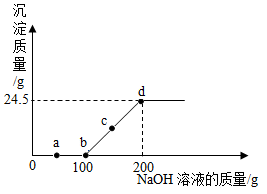
| A.a点溶液中含有两种溶质 |
| B.bc段发生反应的类型为置换反应 |
| C.根据图中数据可以计算出氢氧化钠溶液的浓度 |
| D.d点溶液中主要存在的离子为Na+、Cu2+、OH-、S042- |
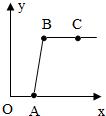
| A.图中纵坐标(y)表示生成CO2的质量 |
| B.反应进行到C点时,溶液中的溶质只有NaCl |
| C.C点溶液的pH>7 |
| D.AB段发生反应的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
| A.一氧化碳是无色无味的气体 | B.碱式碳酸铜呈绿色,受热易分解 |
| C.铝是银白色固体、易导电、传热 | D.石墨是灰黑色固体,熔点较高 |
【知识点】 化学性质与物理性质的差别及应用
| A.风力发电 | B.石油蒸馏得到汽油等 | C.海水晒盐 | D.煤分解得到煤焦油等 |
【知识点】 化学变化和物理变化的判别
A.酚酞溶液 | B.镁条 | C.氯化钾溶液 | D.氯化铜溶液 |
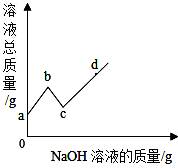
| A.a至b段对应溶液的pH逐渐减小 |
| B.b点对应溶液中的溶质为硫酸钠 |
| C.c点对应溶液中的溶质种类最少 |
| D.a至d段硫酸钠的质量逐渐增大 |
【知识点】 酸的化学性质 盐的性质及用途 溶液的酸碱性与pH值的关系
| A.Na2CO3溶液开始与稀盐酸不反应 |
| B.与CaCO3和过量CO2水溶液反应类似,Na2CO3溶液与稀盐酸反应先生成了 NaHCO3 |
| C.NaHCO3溶液碱性比Na2CO3溶液强,与盐酸反应快 |
| D.Na2CO3溶液呈酸性 |
| A.只有① | B.只有③ | C.只有②和③ | D.①②③都可以 |
【知识点】 酸碱指示剂及其性质 溶液的酸碱性与pH值的关系
| A.冰块制成冰雕 | B.利用膜法从海水中获得淡水 |
| C.泥土烧成瓷器 | D.工业上从空气中分离出氧气 |
【知识点】 化学变化和物理变化的判别
| A.粗盐提纯中蒸发时用玻璃棒搅拌是为了加快水分的蒸发 |
| B.稀释浓硫酸需将水沿器壁缓慢倒入浓硫酸中,并不断搅拌 |
| C.酸雨形成的原因是 CO2和 H2O 反应生成了 H2CO3 |
| D.中和反应生成盐和水,生成盐和水的不一定是中和反应 |
【知识点】 粗盐提纯实验 酸的物理性质及用途 浓硫酸的性质及浓硫酸的稀释
| 加入的物质 | 稀盐酸 | 石灰水 | 酚酞试液 |
| 现象 | 有气泡冒出 | 有白色沉淀 | 变成红色 |
| A.Na2CO3溶液 | B.稀硫酸 | C.NaOH溶液 | D.NaCl溶液 |
二、填空题 添加题型下试题
| 胃舒平 【主要成分】氢氧化铝 【作用与用途】 本品有中和胃酸,减少胃液分泌和解痉止疼作用.用于胃酸过多、胃溃疡及胃痛等. |
【知识点】 酸碱性对生命活动和农作物生长的影响
【知识点】 碱的物理性质及用途
【知识点】 酸的物理性质及用途
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有
(2)写出下列反应的化学方程式:
①用熟石灰中和硫酸厂排出的废水
②将生锈铁钉加入稀硫酸中一段时间后铁锈消失铁钉表面有气泡:
③稀硫酸与碳酸钠溶液反应:
(3)盐酸的下列用途中,不能用硫酸代替盐酸的是
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH.
【知识点】 酸的化学性质

(1)为了验证反应①,小明将无色酚酞试液滴入NaOH溶液中,溶液变成
(2)依据反应②说明NaOH必须密封保存,否则在空气中会变质,其化学方程式为
(3)小明用微观示意图(如图乙)来说明反应③的发生,在反应过程中,没有发生变化的离子是:
(4)为了验证反应④能够发生,你选择的物质是
A. Na2CO3
 B. HCl
B. HCl  C. CuSO4
C. CuSO4 D. NaCl.
D. NaCl.
【知识点】 碱的化学性质 酸碱指示剂及其性质 溶液的酸碱性与pH值的关系
【知识点】 酸的物理性质及用途 浓硫酸的性质及浓硫酸的稀释
(1)下列物质中,误食后不会引起人体中毒的是
A. BaCO3
 B. Pb(NO3)2
B. Pb(NO3)2  C. CuSO4
C. CuSO4  D. BaSO4
D. BaSO4(2)医疗上用X射线检查肠胃病时,病人服用的“钡餐”中不能含有BaCO3 ,其原因是BaCO3与人的胃液中含有的少量盐酸反应产生有毒的BaCl2 , 该反应的化学方程式为
(3)AgNO3遇到蛋白质即生成黑色的蛋白银。有一天学生小王实验时不慎在手指上沾染了少量AgNO3溶液,第二天发现手指上沾染过AgNO3溶液的皮肤颜色
【知识点】 盐的性质及用途
| 废液酸碱度 | 甲 | 乙 | 丙 | 丁 |
| pH | 6.5 | 11.3 | 7.0 | 2.0 |
(1)各取溶液少许,分别滴入 1~2 滴无色酚酞试液,能使酚酞试液变红的废液是
(2)乙、丁分别是未用完的氢氧化钾溶液和稀硝酸。为了防止废液对环境的污染,小聪将丁溶液逐滴滴入乙中,刚好完全反应。该反应的化学方程式为:
三、探究题 添加题型下试题
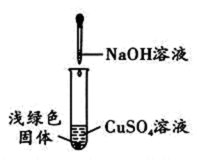
【查阅资料】
①NaOH与CuSO4反应会生成Cu(OH)2,也会生成Cu4(OH)6SO4(碱式硫酸铜)。
②Cu(OH)2在80℃会分解生成CuO
③Cu4(OH)6SO4不溶于水,能与酸反应,分解温度需300℃
【猜想与假设】
NaOH溶液
猜想一:浅绿色固体为Cu(OH)2;
猜想二:浅绿色固体为Cu4(OH)6SO4;
猜想三:浅绿色固体为Cu(OH)2和Cu4(OH)6SO4
【获取事实与证据】
(1)取少量浅绿色固体放入试管中,加热至100℃,观察到黑色固体物质,说明浅绿色固体中存在
(2)另取少量浅绿色固体放入试管中,加入足量稀硝酸,再滴加Ba(NO3)2溶液,出现白色沉淀,该白色沉淀
(3)【结论】分析整个实验现象,你能得出的实验结论是
(4)【应用】碱式硫酸铜在植物表面上能逐步释放铜离子,抑制真菌孢子萌发和菌丝发育,能有效防治作物的真菌及细菌性病害。农业上常用作
【知识点】 盐的性质及用途
四、解答题 添加题型下试题
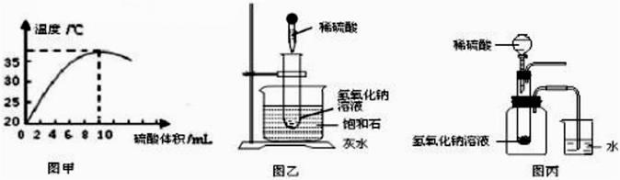
(1)甲同学取10mL10%的NaOH溶液于试管中,逐滴加入10%的稀硫酸,随着硫酸的加入,烧杯中溶液温度与加入硫酸体积之间的变化关系如甲图所示。本实验选用 10%的NaOH 溶液而不选用 NaOH 固体的原因是
(2)乙同学按乙图装置进行实验,其中饱和澄清石灰水的作用是
(3)丙同学按丙图实验,可以根据
【知识点】 溶解时的吸热或放热现象 固体溶解度的影响因素 中和反应及其应用
五、填空题 添加题型下试题
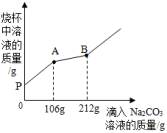
(1)在实验过程中,其中出现冒气泡的是
(2)逐渐滴入碳酸钠溶液的过程中,杯中溶液的pH如何变化?
(3)原溶液中HCl的质量是多少克?
(4)当滴入Na2CO3溶液至图中B点时,通过计算求烧杯中(不饱和溶液)溶质的质量分数为多少?
六、解答题 添加题型下试题
【知识点】 酸、碱、盐的鉴别
①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴紫色石蕊试液(质量忽略不计),重新称量);
②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由红色恰好变为紫色时,停止滴加,再次称量,数据如下表:
| 锥形瓶 | 锥形瓶+稀盐酸 | 锥形瓶+反应后溶液 | |
| 质量(克) | 35.5 | 55.5 | 80.5 |
(1)若要配制500克16%的氢氧化钠溶液,需要氢氧化钠固体
(2)本次实验中,实际消耗的氢氧化钠溶液质量为
(3)请通过计算确定该瓶稀盐酸的溶质质量分数
(4)另有同学做了同样实验,却得到了不同的结果,于是用精密pH试纸测得反应后锥形瓶内溶液的pH为8.2,则他测出的盐酸溶质质量分数
七、填空题 添加题型下试题
(1)喝酸牛奶后,胃容物的pH
(2)“别把含乳饮料当作牛奶喝”,是因为含乳饮料中
(3)“钙尔奇D”是生活中一种常见的补钙剂,现摘自某制药有限公司生产的“钙尔奇D600”说明书的一部分内容如下:本品“每片含主要成分碳酸钙1.5g(相当于钙600mg)”.你认为此说明中的数字有科学依据吗?
【知识点】 溶液的酸碱性与pH值的关系
试卷分析
试卷题型(共 29题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 化学性质与物理性质的差别及应用 | |
| 2 | 0.85 | 中和反应及其应用 酸、碱的使用注意事项 溶液的酸碱性与pH值的关系 | |
| 3 | 0.85 | 酸的化学性质 盐的性质及用途 pH值的变化 | |
| 4 | 0.4 | 碱的化学性质 置换反应及其应用 复分解反应及其应用 | |
| 5 | 0.65 | 二氧化碳的化学性质 酸的化学性质 盐的性质及用途 | |
| 6 | 0.85 | 化学性质与物理性质的差别及应用 | |
| 7 | 0.85 | 化学变化和物理变化的判别 | |
| 8 | 0.65 | 碱的化学性质 酸碱指示剂及其性质 | |
| 9 | 0.65 | 酸的化学性质 盐的性质及用途 溶液的酸碱性与pH值的关系 | |
| 10 | 0.65 | 酸的化学性质 盐的性质及用途 | |
| 11 | 0.85 | 氧气的用途 碱的物理性质及用途 | |
| 12 | 0.85 | 酸碱指示剂及其性质 溶液的酸碱性与pH值的关系 | |
| 13 | 0.85 | 化学变化和物理变化的判别 | |
| 14 | 0.85 | 粗盐提纯实验 酸的物理性质及用途 浓硫酸的性质及浓硫酸的稀释 | |
| 15 | 0.65 | 盐的性质及用途 常见物质的鉴定 酸碱指示剂及其性质 | |
| 二、填空题 | |||
| 16 | 0.65 | 酸碱性对生命活动和农作物生长的影响 | |
| 17 | 0.85 | 碱的物理性质及用途 | |
| 18 | 0.85 | 酸的物理性质及用途 | |
| 19 | 0.65 | 酸的化学性质 | |
| 20 | 0.65 | 碱的化学性质 酸碱指示剂及其性质 溶液的酸碱性与pH值的关系 | |
| 21 | 0.85 | 酸的物理性质及用途 浓硫酸的性质及浓硫酸的稀释 | |
| 22 | 0.65 | 盐的性质及用途 | |
| 23 | 0.85 | 中和反应及其应用 盐与化肥 酸碱指示剂及其性质 | |
| 26 | 0.4 | 溶质质量分数的简单计算 盐的性质及用途 溶液的酸碱性与pH值的关系 根据化学反应方程式的计算 | |
| 29 | 0.4 | 溶液的酸碱性与pH值的关系 | |
| 三、探究题 | |||
| 24 | 0.4 | 盐的性质及用途 | |
| 四、解答题 | |||
| 25 | 0.65 | 溶解时的吸热或放热现象 固体溶解度的影响因素 中和反应及其应用 | |
| 27 | 0.4 | 酸、碱、盐的鉴别 | |
| 28 | 0.4 | 溶质质量分数的简单计算 溶液的酸碱性与pH值的关系 质量守恒定律及其应用 根据化学反应方程式的计算 | |



 纯碱用于改良酸性土壤
纯碱用于改良酸性土壤 一氧化碳做燃料
一氧化碳做燃料 氧气用于炼钢
氧气用于炼钢  石墨做电极
石墨做电极

