浙江省嘉兴市桐乡市城区初中2019年九年级上学期期中联考科学试题
浙江
九年级
期中
2020-02-07
271次
整体难度:
适中
考查范围:
常见的物质、当代社会重大课题、物质的运动与相互作用、生物的新陈代谢、人、健康与环境、科学探究所需要的基本技能、物质的结构
一、选择题 添加题型下试题
A. 可回收物 可回收物 | B. 厨余垃圾 厨余垃圾 |
C. 有害垃圾 有害垃圾 | D. 其他垃圾 其他垃圾 |
【知识点】 金属的回收利用及其重要性 环境污染的危害性与防治措施
| A.年糕——真空包装:能使食品不与氧气接触 |
| B.薯片——充氮气:能隔绝空气并防止食品变形 |
| C.月饼——放铁粉包:能除去包装袋内的氧气和水蒸气 |
| D.海苔——放生石灰包:能除去包装袋内的氧气 |
【知识点】 空气的利用 金属锈蚀的条件及其防护 碱的化学性质
| A.5.5W | B.55W | C.550W | D.5500W |
【知识点】 功率计算公式的应用
| A.我国有丰富的食盐资源,来源广泛,可以来自海水、井水、盐湖 |
| B.人体内多余的氯化钠可以通过呼吸、汗液、尿液和粪便排出体外 |
| C.用浓的食盐溶液清洗伤口,可以使细胞内的水渗出,使蛋白质凝固、具有杀菌作用 |
| D.食盐既可以作食物佐料,也是重要的化工原料 |
| A.重力势能一定减小,动能一定增加 |
| B.重力势能一定增加,动能一定减小 |
| C.重力势能一定减小,动能不一定增加 |
| D.重力势能不一定减小,动能也不一定增加 |
【知识点】 动能和势能的大小变化

| A.该实验是将氢氧化钠溶液滴入稀盐酸中 |
| B.a点所示溶液中,溶质只有NaCl |
| C.b点表示稀盐酸和氢氧化钠溶液恰好完全反应 |
| D.向点c所示溶液中滴加紫色石蕊溶液,溶液变蓝色 |

A.置换反应  | B.分解反应  | C.化合反应  | D.复分解反应 |
【知识点】 质量守恒定律及其应用 置换反应及其应用 识别化学反应基本类型
| A.碳酸钾 | B.烧碱 |
| C.乙醇 | D.熟石灰 |
【知识点】 盐的性质及用途

| A.B管中铁钉不会锈蚀 |
| B.若将A管中的水改为食盐水能加快铁的锈蚀 |
| C.左右试管对比说明铁锈蚀与水、空气有关 |
| D.L端与R端液面高度保持一致 |
【知识点】 金属锈蚀的条件及其防护
A. | B. |
C. | D. |
【知识点】 金属的化学性质
①证明变质:取少量溶液,滴加适量的氯化钡,观察现象
②确定成分:取少量溶液,加入足量氯化钙,过滤,向滤液中滴加酚酞溶液
③测定纯度:取一定量溶液,加入足量浓盐酸,用氢氧化钠固体吸收气体,称量
④除去杂质:取溶液,滴加石灰水至恰好完全反应,过滤
| A.②③ | B.①②③ | C.①②④ | D.①③④ |
【知识点】 碱的化学性质 常见离子的检验方法及现象 常见物质的鉴定 物质除杂或净化

| A.a至b段对应溶液的pH逐渐减小 |
| B.b点对应溶液中的溶质为氯化钠 |
| C.c点对应溶液中的溶质种类最少 |
| D.a至d段碳酸钠的质量逐渐增大 |
【知识点】 酸的化学性质 中和反应及其应用 盐的性质及用途 溶液的酸碱性与pH值的关系

| A.AgNO3和Al(NO3)3 |
| B.Al(NO3)3 和Cu(NO3)2 |
| C.Al(NO3)3 和Cu(NO3)2和Zn(NO3)2 |
| D.Zn(NO3)2、 Al(NO3)3 和Cu(NO3)2 |
【知识点】 金属活动性顺序及其应用 金属的化学性质

| A.A→B段对应的实验现象是固体部分溶解,无气泡冒出 |
| B.B→C段对应溶液pH逐渐变大 |
| C.C点对应溶液中一定含有的溶质是硝酸、硝酸钠、碳酸钠、硝酸钡 |
| D.原白色固体中一定含有碳酸钠、硫酸钠、硝酸钡 |
【知识点】 碱的化学性质 盐的性质及用途 常见离子的检验方法及现象 常见物质的鉴定

| A.①② | B.①②③ |
| C.①②④ | D.①②③④ |
二、填空题 添加题型下试题
【知识点】 pH值的测量及方法 溶液的酸碱性与pH值的关系

(1)甲装置中盛放的液体是
(2)实验过程中观察到无水硫酸铜不变色,澄清石灰水变浑浊,则原气体中一定含有
(3)从环保上考虑实验装置应该增加
【知识点】 常见气体的检验与除杂方法 二氧化碳的检验和验满 金属的冶炼
三、解答题 添加题型下试题

(1)图甲描述了NaOH溶液与盐酸反映的微观示意图,该反应的实质是
A.Fe B.酚酞溶液 C.
 D.
D.
(2)图乙表示的反应中涉及4种物质,其中属于氧化物的是
(3)除了如图所示的两种反应外,请在写出一个生成氯化钠的化学反应方程式:
【知识点】 中和反应及其应用 酸碱指示剂及其性质 氧化物、酸、碱和盐的概念
四、填空题 添加题型下试题

【知识点】 影响摩擦力大小的因素 功的计算公式的应用 动能的影响因素

(1)“锡纸”燃烧揭秘
“锡纸”在中间狭窄的地方先开始燃烧的原因是:由于电源短路,产生较大的电流,且“锡纸”在中间狭窄的地方电阻大,产生的热量多,温度先达到着火点。电池在工作时将
(2)锡纸”成分揭秘
查阅资料:“锡纸”是锡箔或铝箔和纸粘合而成。
实验探究:取包口香糖的“锡纸”,将有金属的一面打磨后,朝上放在点滴板上;并向其表面滴加氯化锌溶液,观察到有深灰色固体析出。
实验分析:
①通过上述实验现象,可知“锡纸”是
②实验中打磨“锡纸”的目的是
③下列物质的溶液可以替代氯化锌溶液完成上述探究实验的是
A. 硝酸银 B.稀盐酸 C.硫酸亚铁 D.氯化镁
【知识点】 导体 能量的相互转化和转移

【知识点】 金属的化学性质 根据化学反应方程式的计算
五、探究题 添加题型下试题
有关的实验设计,用的是三个体积相同而质量不同的小球,实验时分别从某个高度自由落下到花泥上, ( 已知m钢>m玻>m木)
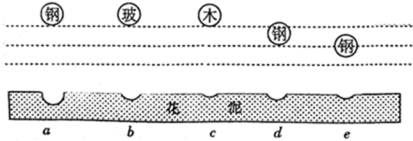
(1)本实验通过观察
(2)实验a、b、c可研究重力势能与质量的关系,a、b、c三个小球的
【提出问题】氢氧化钠溶液是否变质?
【查阅资料】氯化钠溶液、氯化钡溶液呈中性.
【实验探究】小王、小李两同学分别设计了不同方案并加以实验.
| 实验步骤 | 实验现象 | 结论 | |
| 小王 | 用pH试纸测溶液的pH | 溶液的pH>7 | 溶液没有变质 |
| 小李 | 取少量溶液于试管中,加入适量氯化钡溶液 | ____________ | 溶液已经变质 |
(1)小李同学认为小王同学的结论不科学,其理由是
(2)小李同学的实验中观察到实验现象为
(3)小张为判断溶液是否完全变质,取少量溶液于试管中,向试管中加入
(4)若氢氧化钠溶液已经变质,则变质的原因是
【知识点】 碱的化学性质 常见离子的检验方法及现象 常见物质的鉴定 酸碱指示剂及其性质
资料1:2KMnO4 + 5 H2C2O4 + 3H2SO4 = K2SO4 + 2MnSO4 + 8H2O + 10CO2↑
资料2:通常情况下,反应物浓度变大,反应加快;温度升高,反应加快。
(1)根据这些资料,小明提出了两个假设。
假设一:褪色速度突然加快是由反应物浓度变大引起的;
假设二:褪色速度突然加快是由反应过程中温度升高引起的;
小明经过分析,否定了假设一,理由是
(2)小丽针对假设二进行实验探究后,经过思考,又做了如下实验:
把经过硫酸酸化的高锰酸钾溶液等分为两份,分装A、B两试管,同时向两支试管中加入等量等浓度的草酸溶液,并置于同一水浴中。迅速向A试管中加入一定量的MnSO4 , 发现A试管中溶液褪色明显快于B试管。上述实验中,把2支试管置于用一水浴中的目的是
【知识点】 影响化学反应速率的因素 催化剂在化学反应中的作用
猜想一:可能是CaCO3和Fe。
猜想二:可能是CaCO3和Fe2O3。
猜想三:可能是
【实验设计】小明设计了下图所示的实验
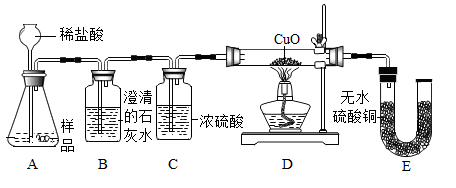
【实验与分析】
(1)向A装置中加入稀盐酸,B装置中出现浑浊现象,证明样品中含有CaCO3。
(2)若粉末中含有Fe,装置E中应观察到的现象是
【实验与分析】
上述实验中,如果将E装置去掉,是否还能验证粉末中含有Fe,请说明理由
六、解答题 添加题型下试题
(1)为什么不能用铁桶或铝桶配制波尔多液(用化学方程式表示)
(2)硫酸铜溶液和石灰乳混合时,应该怎样操作才能避免失去药效

求:
(1)每次投下的水在下落过程中重力做功的平均功率;
(2)飞机在水面沿直线匀速滑行时,飞机所受的牵引力。
七、探究题 添加题型下试题

(1)滤液X的pH
(2)CD段发生反应的化学方程式为
(3)滤液X中含有的溶质是
(4)滴加入30克稀硫酸时,烧杯中沉淀的质量m2的值为多少?(写出计算过程)
【知识点】 碱的化学性质 根据化学反应方程式的计算
试卷分析
试卷题型(共 28题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 金属的回收利用及其重要性 环境污染的危害性与防治措施 | |
| 2 | 0.85 | 空气的利用 金属锈蚀的条件及其防护 碱的化学性质 | |
| 3 | 0.85 | 功率计算公式的应用 | |
| 4 | 0.85 | 水盐平衡 营养素的作用 | |
| 5 | 0.85 | 动能和势能的大小变化 | |
| 6 | 0.65 | 中和反应及其应用 酸碱指示剂及其性质 pH值的变化 | |
| 7 | 0.85 | 质量守恒定律及其应用 置换反应及其应用 识别化学反应基本类型 | |
| 8 | 0.94 | 盐的性质及用途 | |
| 9 | 0.65 | 金属锈蚀的条件及其防护 | |
| 10 | 0.65 | 金属的化学性质 | |
| 11 | 0.65 | 碱的化学性质 常见离子的检验方法及现象 常见物质的鉴定 物质除杂或净化 | |
| 12 | 0.65 | 酸的化学性质 中和反应及其应用 盐的性质及用途 溶液的酸碱性与pH值的关系 | |
| 13 | 0.4 | 金属活动性顺序及其应用 金属的化学性质 | |
| 14 | 0.4 | 碱的化学性质 盐的性质及用途 常见离子的检验方法及现象 常见物质的鉴定 | |
| 15 | 0.65 | 铁锈的主要成分 金属的化学性质 酸的化学性质 | |
| 二、填空题 | |||
| 16 | 0.85 | pH值的测量及方法 溶液的酸碱性与pH值的关系 | |
| 17 | 0.4 | 常见气体的检验与除杂方法 二氧化碳的检验和验满 金属的冶炼 | |
| 19 | 0.85 | 影响摩擦力大小的因素 功的计算公式的应用 动能的影响因素 | |
| 20 | 0.85 | 导体 能量的相互转化和转移 | |
| 21 | 0.4 | 金属的化学性质 根据化学反应方程式的计算 | |
| 三、解答题 | |||
| 18 | 0.65 | 中和反应及其应用 酸碱指示剂及其性质 氧化物、酸、碱和盐的概念 | |
| 26 | 0.65 | 碱的物理性质及用途 盐的性质及用途 | |
| 27 | 0.65 | 功率计算公式的应用 功的计算公式的应用 | |
| 四、探究题 | |||
| 22 | 0.85 | 控制变量法 势能的影响因素 | |
| 23 | 0.4 | 碱的化学性质 常见离子的检验方法及现象 常见物质的鉴定 酸碱指示剂及其性质 | |
| 24 | 0.4 | 影响化学反应速率的因素 催化剂在化学反应中的作用 | |
| 25 | 0.65 | 金属的化学性质 酸的化学性质 常见物质的鉴定 | |
| 28 | 0.15 | 碱的化学性质 根据化学反应方程式的计算 | |



