永州市某中学的初三化学课堂上,刘老师布置了一道计算题,题目如下:
【思考题】取100g溶质质量分数为8%的氢氧化钠溶液于烧杯中,向其中加入100g19.6%的稀硫酸,充分反应后,求所得溶液中硫酸钠的质量分数;检查作业发现,班上出现了下表所示的两种情形:
请通过计算分析你赞同的计算结果。
【思考题】取100g溶质质量分数为8%的氢氧化钠溶液于烧杯中,向其中加入100g19.6%的稀硫酸,充分反应后,求所得溶液中硫酸钠的质量分数;检查作业发现,班上出现了下表所示的两种情形:
| 结果编号 | ① | ② |
| 计算结果 | 14.2% | 7.1% |
请通过计算分析你赞同的计算结果。
更新时间:2020/05/07 13:56:51
|
相似题推荐
解答题
|
较难
(0.4)
【推荐1】某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成,取四份样品分别加稀硫酸反应,其实验数据记录如下表。
(1)画出在50.0g样品中加稀硫酸的质量与产生气体质量变化关系旳示意图___________
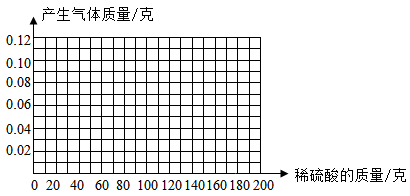
(2)试计算第2份样品反应后溶液中硫酸锌质量分数为多少___________ ?(保留到0.1%)
| 样品 | 第1份 | 第2份 | 第3份 | 第4份 |
| 取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 产生气体质量(g) | 0.04 | 0.08 | 0.1 | 0.1 |
(1)画出在50.0g样品中加稀硫酸的质量与产生气体质量变化关系旳示意图

(2)试计算第2份样品反应后溶液中硫酸锌质量分数为多少
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】向含 和HCl的84.8g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图。据图回答:
和HCl的84.8g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图。据图回答:
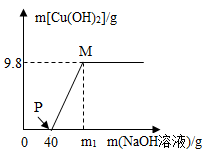
(1)整个反应过程中,原混合溶液中个数不变的微粒有________ 。
(2)P点溶液中的溶质是________ 。
(3)M点溶液的溶质质量分数是多少?________
 和HCl的84.8g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图。据图回答:
和HCl的84.8g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图。据图回答:
(1)整个反应过程中,原混合溶液中个数不变的微粒有
(2)P点溶液中的溶质是
(3)M点溶液的溶质质量分数是多少?
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐3】某科学兴趣小组使用图所示装置,对某种铁铜合金的成分进行测量。先取足量稀硫酸于烧杯中,再向其中加入14.0g合金样品开始计时,并将电子天平的读数记录在下表中,请回答下列问题:

(1)根据电子天平读数和时间的关系分析,该反应进行过程中,氢气的产生速度有什么特点_______ ?
(2)合金中铁元素的质量百分含量为多少_______ ?
(3)完全反应后,烧杯中FeSO4的质量分数为多少_______ ?(用百分数表示)
| 空烧杯 加入硫酸后 | 加铁粉后 | ||||||
| 5分钟 | 12分钟 | 21分钟 | 40分钟 | 3小时 | |||
| 读数(g) | 28.5 | 169.7 | 183.6 | 183.5 | 183.4 | 183.3 | 183.3 |

(1)根据电子天平读数和时间的关系分析,该反应进行过程中,氢气的产生速度有什么特点
(2)合金中铁元素的质量百分含量为多少
(3)完全反应后,烧杯中FeSO4的质量分数为多少
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】工业盐酸中通常因溶有少量的 FeCl3 而呈黄色,小红为测定某工业盐酸中 HCl 的含量进行如下实验:取某工业盐酸 l00g,滴加一定溶质质量分数的 NaOH 溶液,测得加入 NaOH溶液质量与反应生成的沉淀质量关系如图所示,FeCl3 与 NaOH 反应的化学方程式为FeCl3+3NaOH═Fe(OH)3↓+3NaCl.请回答下列问题:
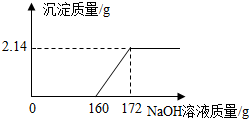
(1)FeCl3 与 NaOH 恰好完全反应时,生成沉淀的质量是________ g;
(2)所滴加的 NaOH 溶液质量为 160 克时,溶液中的溶质是________ ;
(3)该工业盐酸中 HCl 的质量分数是多少?________

(1)FeCl3 与 NaOH 恰好完全反应时,生成沉淀的质量是
(2)所滴加的 NaOH 溶液质量为 160 克时,溶液中的溶质是
(3)该工业盐酸中 HCl 的质量分数是多少?
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】位于天津滨海新区塘沽开发区曾发生特大爆炸,爆炸共造成173人遇难,巨大财产损失。据调查元凶是硝酸铵,已知高温或猛烈撞击均会使化肥硝酸铵发生剧烈的分解反应,产生大量气体,放出大量热,因而发生爆炸。硝酸铵爆炸的化学方程式2NH4NO3═2N2↑+O2↑+4H2O↑,生成氧气又为易燃物的燃烧提供条件,从而引发火灾,由于硝酸铵会与水反应生成硝酸,在爆炸过后环境监察人员马上对下水道中水样进行抽检,发现硝酸含量超标,故紧急调运大量碱性的白色粉末进行中和稀释,最后硝酸被拦截在限定区域,使影响控制在最小的范围内。根据题意回答下列问题。
(1)请根据化学方程式计算16吨硝酸铵完全分解,会产生多少氧气?________
(2)调运大量碱性的白色粉末进行稀释,根据你学过的知识,从可行、经济、环保等综合因素考虑,白色粉末可能是_______ ,理由是什么______ ?.
(1)请根据化学方程式计算16吨硝酸铵完全分解,会产生多少氧气?
(2)调运大量碱性的白色粉末进行稀释,根据你学过的知识,从可行、经济、环保等综合因素考虑,白色粉末可能是
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】“双吸剂”是一种常见袋装食品的保鲜剂,能吸收空气中的氧气、二氧化碳、水蒸气等。某包“双吸剂”标签如图所示。某科学兴趣小组通过定性探究,发现这包久置的“双吸剂”固体样品中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3的几种或全部。为进一步确定这包久置的“双吸剂”固体的成分,进行如下定量实验∶取3g样品研碎,并用磁铁充分吸引后,得到剩余固体2.6 g,按照下图流程进行实验。


请回答相关问题∶
(1)铁粉的质量是___________ g。
(2)操作二名称是___________ 。
(3)根据实验数据计算判断,固体I的成分是否同时含有Fe2O3和CaCO3?___________ (填“是”或“否”)。
(4)烧杯C中溶液的溶质为___________ 。
(5)依据有关实验数据判断,这包久置“双吸剂”固体的成分中一定含有Ca(OH)2,是否同时含有CaO?___________ (填“是”或“否”)。


请回答相关问题∶
(1)铁粉的质量是
(2)操作二名称是
(3)根据实验数据计算判断,固体I的成分是否同时含有Fe2O3和CaCO3?
(4)烧杯C中溶液的溶质为
(5)依据有关实验数据判断,这包久置“双吸剂”固体的成分中一定含有Ca(OH)2,是否同时含有CaO?
您最近一年使用:0次
解答题
|
较难
(0.4)
名校
【推荐2】“过碳酸钠”(2Na2CO3·3H2O2)俗称固体双氧水,它既有碳酸盐的性质,又有双氧水的不稳定性和氧化性,是很好的消毒剂和供氧剂,广泛应用于洗涤、印染和医药等领域。“过碳酸钠”的制备流程如下:
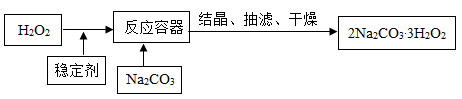
请回答下列问题:
(1)H2O2在催化或受热条件下易分解,其化学方程式为________ ;在上述流程中,向反应前的H2O2中加入稳定剂的作用是________ ;
(2)在“过碳酸钠”中加入下列物质时,不会导致“过碳酸钠”变质的是________ (填序号);
A.二氧化锰 B.稀盐酸 C.硫酸钠 D.石灰水
(3)“过碳酸钠”极易分解,得到碳酸钠、水和氧气,其反应方程式可表示为2(2Na2CO3·3H2O2)=4Na2CO3+6H2O+3O2↑,请通过计算说明:
①若“过碳酸钠”分解产生氧气12g,则同时产生碳酸钠的质量是多少________ ?
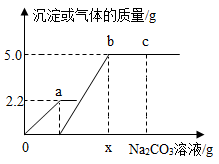
②若将上述产生的碳酸钠全部配制成溶质质量分数为10%的溶液,逐滴加入一定质量的CaCl2和HCl的混合溶液中,反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示。则x的数值为多少________ ?

请回答下列问题:
(1)H2O2在催化或受热条件下易分解,其化学方程式为
(2)在“过碳酸钠”中加入下列物质时,不会导致“过碳酸钠”变质的是
A.二氧化锰 B.稀盐酸 C.硫酸钠 D.石灰水
(3)“过碳酸钠”极易分解,得到碳酸钠、水和氧气,其反应方程式可表示为2(2Na2CO3·3H2O2)=4Na2CO3+6H2O+3O2↑,请通过计算说明:
①若“过碳酸钠”分解产生氧气12g,则同时产生碳酸钠的质量是多少
②若将上述产生的碳酸钠全部配制成溶质质量分数为10%的溶液,逐滴加入一定质量的CaCl2和HCl的混合溶液中,反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示。则x的数值为多少

您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐3】如图装置是检验CO及CO被氧化后氧化产物的化学性质。通入的气体主要含有CO,所含杂质在此条件下不参与任何反应。玻璃管中的黑色粉末主要含氧化铜,杂质在此条件下不参与任何反应。所有反应充分发生,反应生成的气体全部被澄清石灰水吸收。
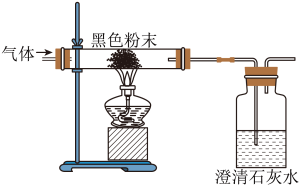
(1)在实验前,出于安全考虑,正确的操作是______ 。当玻璃管中黑色粉末变成光亮的红色后,仅凭此现象能否说明CO具有还原性?请说明理由。______
(2)该实验装置的不足之处是______ (写出一条即可)。
(3)已知下列数据:反应前通入的气体总质量为m1,反应前黑色粉末的质量m2,玻璃管质量为m3,充分反应后玻璃管及物质总质量为m4,根据以上已知条件,通过计算,能测出的科学量有______
A.气体中的CO的质量分数 B.CO被氧化后的氧化产物的质量
C.黑色粉末中氧化铜的质量分数 D.黑色粉末中氧元素的质量分数

(1)在实验前,出于安全考虑,正确的操作是
(2)该实验装置的不足之处是
(3)已知下列数据:反应前通入的气体总质量为m1,反应前黑色粉末的质量m2,玻璃管质量为m3,充分反应后玻璃管及物质总质量为m4,根据以上已知条件,通过计算,能测出的科学量有
A.气体中的CO的质量分数 B.CO被氧化后的氧化产物的质量
C.黑色粉末中氧化铜的质量分数 D.黑色粉末中氧元素的质量分数
您最近一年使用:0次