某同学在实验室进行有关配制稀硫酸的实验时观察瓶上的标签,试分析并回答下列问题。
(1)这瓶浓硫酸溶液的质量为多少?其中含溶质硫酸为多少?
(2)该同学利用这瓶浓硫酸欲配制溶质质量分数为10%的稀硫酸600克,则他需要这种浓硫酸多少毫升?应加入蒸馏水多少毫升?
| 浓硫酸(H2SO4) 300mL 密度1.80g/cm 质量分数98% |
(1)这瓶浓硫酸溶液的质量为多少?其中含溶质硫酸为多少?
(2)该同学利用这瓶浓硫酸欲配制溶质质量分数为10%的稀硫酸600克,则他需要这种浓硫酸多少毫升?应加入蒸馏水多少毫升?
更新时间:2020-12-31 20:46:01
|
相似题推荐
解答题
|
较易
(0.85)
【推荐1】现有200g10%的食盐溶液,要使其溶质质量分数变为20%,若采用如下方法:试计算(写出计算过程)
(1)增加溶质:可加入食盐的质量是多少克?
(2)加入浓溶液:可加入溶质质量分数为25%的食盐溶液多少克?
(3)蒸发水需要多少克?
(1)增加溶质:可加入食盐的质量是多少克?
(2)加入浓溶液:可加入溶质质量分数为25%的食盐溶液多少克?
(3)蒸发水需要多少克?
您最近一年使用:0次
解答题
|
较易
(0.85)
【推荐2】如图,在新鲜的冬瓜内倒入10%的食盐水300克,现在将一木块放入该溶液中,木块处于漂浮状态,木块露出水面的部分高为h。

(1)经测量,一天后的食盐水质量分数变为6%,一天之后,h值与原来相比将___ 。(填“变大”、“变小”或“不变”)
(2)一天之后因冬瓜失水质量减少了,求冬瓜的质量减少了多少?___ (不考虑水的蒸发,请写出计算过程)
(3)现需要将300克10%的食盐水变成溶质质量分数为20%的溶液,请写出一种可行的方法,并计算说明。___

(1)经测量,一天后的食盐水质量分数变为6%,一天之后,h值与原来相比将
(2)一天之后因冬瓜失水质量减少了,求冬瓜的质量减少了多少?
(3)现需要将300克10%的食盐水变成溶质质量分数为20%的溶液,请写出一种可行的方法,并计算说明。
您最近一年使用:0次
解答题
|
较易
(0.85)
【推荐1】20 克蔗糖溶于水后,得到溶质的质量分数为 40%的溶液,则得到的溶液的质量为多少?若想要得到溶质质量分数为 20%的蔗糖溶液,则需要再加入水的质量为多少?
您最近一年使用:0次
解答题
|
较易
(0.85)
【推荐2】下表是硫酸溶液和氨水的密度及其溶质质量分数对照表(20℃),请计算:
(1)配制 12%的硫酸溶液,需要24%的硫酸溶液多少毫升?
12%的硫酸溶液,需要24%的硫酸溶液多少毫升?
(2)将 12%的氨水稀释成3%的溶液,需要加水多少毫升?(水的密度取
12%的氨水稀释成3%的溶液,需要加水多少毫升?(水的密度取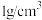 )
)
(1)配制
 12%的硫酸溶液,需要24%的硫酸溶液多少毫升?
12%的硫酸溶液,需要24%的硫酸溶液多少毫升?(2)将
 12%的氨水稀释成3%的溶液,需要加水多少毫升?(水的密度取
12%的氨水稀释成3%的溶液,需要加水多少毫升?(水的密度取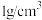 )
)| 溶液中溶质质量分数 | 4% | 12% | 16% | 24% | 28% |
硫酸溶液的密度( ) ) | 1.02 | 1.08 | 1.11 | 1.17 | 1.20 |
氨水的密度( ) ) | 0.98 | 0.95 | 0.94 | 0.92 | 0.90 |
您最近一年使用:0次
解答题
|
较易
(0.85)
【推荐3】质量分数不同的硫酸溶液其密度不相同,对照表如下:
(1)分析表中数据,可以归纳出硫酸溶液的密度与溶质质量分数的关系是____ 。
(2)质量分数80%和20%的两种硫酸溶液等体积混合后,溶液中溶质的质量分数______ 50%。(填“大于”“等于”或“小于”)
(3)某铅酸蓄电池用的酸溶液是质量分数为40%的硫酸,若用3升溶质质量分数为50%的硫酸配制法稀硫酸时,配得的稀硫酸的质量多少千克?______
质量分数 | 10% | 20% | 30% | 40% | 50% | 60% | 70% | 80% | 90% | 98% |
密度 | 1.07 | 1.14 | 1.22 | 1.30 | 1.40 | 1.50 | 1.61 | 1.73 | 1.81 | 1.84 |
(1)分析表中数据,可以归纳出硫酸溶液的密度与溶质质量分数的关系是
(2)质量分数80%和20%的两种硫酸溶液等体积混合后,溶液中溶质的质量分数
(3)某铅酸蓄电池用的酸溶液是质量分数为40%的硫酸,若用3升溶质质量分数为50%的硫酸配制法稀硫酸时,配得的稀硫酸的质量多少千克?
您最近一年使用:0次




