某科学兴趣小组为测定大理石中碳酸钙的含量,进行如图1所示实验:
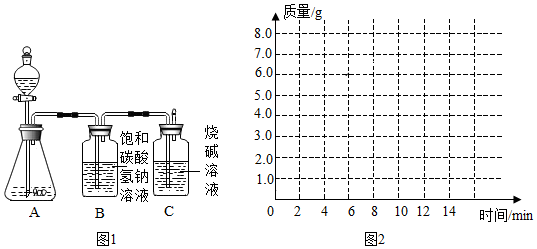
将过量的稀盐酸加入20g大理石中(其他成分不与盐酸反应),把产生的CO2气体用足量的烧碱溶液吸收,同时测量C瓶烧碱溶液增加的质量,结果如下表所示:
(1)请在如图的坐标纸上,以时间为横坐标,以产生CO2气体的质量为纵坐标,面出能够表明产生气体的质量随时间变化规律的关系曲线。__________
(2)计算大理石样品中碳酸钙的质量分数。__________ (要写计算过程)
(3)B中所装药品为饱和碳酸氢钠溶液,作用是吸收挥发出的HCl气体,请你分析去掉该装置进行实验比使用该装置进行实验测量结果__________ (填“偏高”“偏低”或“没有影响”)。

将过量的稀盐酸加入20g大理石中(其他成分不与盐酸反应),把产生的CO2气体用足量的烧碱溶液吸收,同时测量C瓶烧碱溶液增加的质量,结果如下表所示:
| 时间/分 | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
| C增加质量/g | 0 | 3.0 | 5.0 | 6.0 | 6.6 | 6.6 | 6.6 |
(1)请在如图的坐标纸上,以时间为横坐标,以产生CO2气体的质量为纵坐标,面出能够表明产生气体的质量随时间变化规律的关系曲线。
(2)计算大理石样品中碳酸钙的质量分数。
(3)B中所装药品为饱和碳酸氢钠溶液,作用是吸收挥发出的HCl气体,请你分析去掉该装置进行实验比使用该装置进行实验测量结果
更新时间:2021-11-19 18:48:45
|
相似题推荐
解答题
|
适中
(0.65)
【推荐1】治污水是“五水共治”内容之一、根据国家标准,废水排放时铅元素的含量不允许超过 1.0毫克/升。蓄电池生产企业往往采用化学沉淀法处理 Pb2+,其中以氢氧化物沉淀法应用较多。
(1)根据下表信息,沉淀剂除了 NaOH 外,还可使用的两种钠盐是___________。20℃时,各种铅的化合物在水中的溶解度
(2)在弱碱性环境中,氢氧化铅的沉淀更完全。此时废水经沉淀过滤后,检测出铅元素含量仅为0.0207毫克/升。假设废水中的铅元素全部以Pb(OH)2的形式存在,请你通过计算确定,此时1升废水中溶解的Pb(OH)2是多少毫克?
| 物质 | 溶解度/ g | 物质 | 溶解度/ g |
| Pb(NO3 ) 2 | 54.3 | PbCO3 | 7.3×10-5 |
| Pb(OH) 2 | 1.6×10-4 | PbS | 6.8×10-13 |
(1)根据下表信息,沉淀剂除了 NaOH 外,还可使用的两种钠盐是___________。20℃时,各种铅的化合物在水中的溶解度
(2)在弱碱性环境中,氢氧化铅的沉淀更完全。此时废水经沉淀过滤后,检测出铅元素含量仅为0.0207毫克/升。假设废水中的铅元素全部以Pb(OH)2的形式存在,请你通过计算确定,此时1升废水中溶解的Pb(OH)2是多少毫克?
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】有一家工厂处理含铜垃圾的生产流程如下:

(1)黑色固体 是
是______ (填化学式)。
(2)浸入铁屑时发生反应的化学方程式______ 。
(3)在过滤2后,为了得到纯净的铜,还需要进行的操作是洗涤和干燥,检验是否洗涤干净的方法是______ 。

(1)黑色固体
 是
是(2)浸入铁屑时发生反应的化学方程式
(3)在过滤2后,为了得到纯净的铜,还需要进行的操作是洗涤和干燥,检验是否洗涤干净的方法是
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐3】Mg(OH)2具有广泛的应用,常用菱镁矿制备。研究人员向一定质量的菱镁矿粉中加入过量的稀硫酸,充分溶解后除杂、过滤得到只含MgSO4和H2SO4的混合溶液,为确定混合溶液中镁元素的含量,取4份混合溶液各100g,向每份混合溶液中加入一定质量的4%NaOH溶液,得到实验数据如下表所示:
(1)实验④中生成Mg(OH)2的质量______ 克;
(2)实验②与①相比,NaOH溶液质量增加10g,生成Mg(OH)2的质量增加了0.29g,实验①中生成Mg(OH)2质量不是0.29克的原因是______ ;
(3)计算100g混合溶液中含MgSO4的质量(写出计算过程)______ ;
(4)若要配置质量分数为4%的氢氧化钠40g,需要往质量分数10%的氢氧化钠溶液中加水多少克______ ?
| 实验编号 | ① | ② | ③ | ④ |
| NaOH溶液质量/g | 10.0 | 20.0 | 30.0 | 40.0 |
| Mg(OH)2质量/g | 0.232 | 0.522 | 0.580 | ? |
(1)实验④中生成Mg(OH)2的质量
(2)实验②与①相比,NaOH溶液质量增加10g,生成Mg(OH)2的质量增加了0.29g,实验①中生成Mg(OH)2质量不是0.29克的原因是
(3)计算100g混合溶液中含MgSO4的质量(写出计算过程)
(4)若要配置质量分数为4%的氢氧化钠40g,需要往质量分数10%的氢氧化钠溶液中加水多少克
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】为了测定大理石样品中钙元素的质量分数,小科向烧杯中加入25.0g大理石样品,并将200g稀盐分四次加入烧杯中。实验过程的数据如右表所示(杂质不与稀盐酸反应)。
(1)m的值是______ 。
(2)该样品中钙元素质量分数是______ 。
(3)200g盐酸中溶质的质量是多少______ ?
(4)若要中和最终剩余的盐酸,需要氢氧化钠固体的质量是多少______ ?
次数 | 一 | 二 | 三 | 四 |
盐酸质量/g | 50.0 | 50.0 | 50.0 | 50.0 |
混合物总质量/g | 72.8 | 120.6 | m | 219.5 |
(2)该样品中钙元素质量分数是
(3)200g盐酸中溶质的质量是多少
(4)若要中和最终剩余的盐酸,需要氢氧化钠固体的质量是多少
您最近一年使用:0次
解答题
|
适中
(0.65)
名校
【推荐2】某公司生产的纯碱产品中经检测只含有氯化钠杂质。为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品26.5g,加入盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示。求:
(1)生成 的质量为
的质量为___________ 。
(2)该纯碱样品中 的质量分数。
的质量分数。___________
(3)根据条件,此题还可求出下列的哪些量:___________ (选填序号)。
A.该纯碱样品中NaCl的质量分数 B.反应所用稀盐酸的溶质质量分数
C反应后所得溶液中NaCl的质量分数 D.反应生成水的质量

(1)生成
 的质量为
的质量为(2)该纯碱样品中
 的质量分数。
的质量分数。(3)根据条件,此题还可求出下列的哪些量:
A.该纯碱样品中NaCl的质量分数 B.反应所用稀盐酸的溶质质量分数
C反应后所得溶液中NaCl的质量分数 D.反应生成水的质量

您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐3】实验室有一变质的氢氧化钠样品(样品中只含碳酸钠杂质,且成分均匀),为测定样品组成,称取10g氢氧化钠样品放入烧杯中,将120g稀盐酸平均分6份依次加入到烧杯中(烧杯的质量为50g),每次充分反应后都用电子天平进行称量(假设产生的气体完全逸出)
图表示产生气体的质量与加入稀盐酸质量的关系。
(1)小科认为:滴加稀盐酸,若氢氧化钠溶液不变质,不会产生二氧化碳,生成的碳酸钠越多,产生的二氧化碳越多;氢氧化钠完全变质,完全反应所需的稀盐酸的质量越大。请判断小科的推测是否正确:___________ 。
(2)分析表格数据和图像,判断表中m的值为___________ ,a的值为 ___________ 。
(3)列式计算该份氢氧化钠样品变质前的质量。___________

实验次数 | 1 | 2 | 3 | 4 | 5 | 6 |
加入稀盐酸的质量(克) | 20 | 20 | 20 | 20 | 20 | 20 |
电子天平的示数(克) | 120 | 140 | 160 | 179.1 | m | 218.9 |
(1)小科认为:滴加稀盐酸,若氢氧化钠溶液不变质,不会产生二氧化碳,生成的碳酸钠越多,产生的二氧化碳越多;氢氧化钠完全变质,完全反应所需的稀盐酸的质量越大。请判断小科的推测是否正确:
(2)分析表格数据和图像,判断表中m的值为
(3)列式计算该份氢氧化钠样品变质前的质量。

您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】农技人员采用“测土配方”技术对一片果园进行了土壤检测,结果显示该果园需要补充一定量的氮元素和钾元素.某同学取丰收牌钾肥(如图1)样品2.0g,溶于足量的水中,滴加过量氯化钡溶液,产生沉淀质量与所加氯化钡溶液质量的关系如图2.试计算该钾肥样品中硫酸钾的质量分数?判断是否符合产品外包装说明?


您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】二氧化氯ClO2是一种黄绿色到橙黄色的气体,被国际上公认为安全、低毒的绿色消毒剂,一种新型制取水处理剂二氧化氯的化学方程式为2KClO3+CH3OH+H2SO4=2ClO2↑+K2SO4+HCHO+2H2O,完成下列小题:
(1)氯酸钾KClO3属于盐,写出氯酸钾中的阴离子符号。
(2)若生成27克二氧化氯,需要硫酸质量为多少克?(列式计算)
(1)氯酸钾KClO3属于盐,写出氯酸钾中的阴离子符号。
(2)若生成27克二氧化氯,需要硫酸质量为多少克?(列式计算)
您最近一年使用:0次



