天然碱的主要成分是碳酸钠,工业上常采用“天然碱苛化法"制取氢氧化钠,流程如下:

(1)操作1的名称是___________ 。
(2)用150克天然碱(含杂质10%,杂质不溶于水)配制溶质质量分数为20%的碳酸钠溶液,需要加水多少克?___________
(3)在制取氢氧化钠的过程中,固体回收池的碳酸钙可以回收再利用。回收得到的碳酸钙质量与石灰石质量的比值称为碳酸钙回收率。小明测量回收池中的固体质量,计算碳酸钙回收率,记录为a%;小红通过氢氧化钠晶体质量计算碳酸钙的质量,并算得碳酸钙的回收率,记录为b%, 发现a大于b、请说明a大于b原因:___________ 。(例举一个)

(1)操作1的名称是
(2)用150克天然碱(含杂质10%,杂质不溶于水)配制溶质质量分数为20%的碳酸钠溶液,需要加水多少克?
(3)在制取氢氧化钠的过程中,固体回收池的碳酸钙可以回收再利用。回收得到的碳酸钙质量与石灰石质量的比值称为碳酸钙回收率。小明测量回收池中的固体质量,计算碳酸钙回收率,记录为a%;小红通过氢氧化钠晶体质量计算碳酸钙的质量,并算得碳酸钙的回收率,记录为b%, 发现a大于b、请说明a大于b原因:
更新时间:2022-05-17 16:49:44
|
相似题推荐
解答题
|
适中
(0.65)
【推荐1】实验室需要配置100mL30%的稀硫酸(ρ1=1.22g/cm3),求:
(1)所配置的稀硫酸的质量为多少千克;
(2)需要98%浓硫酸多少毫升(ρ2=1.84g/cm3)
(1)所配置的稀硫酸的质量为多少千克;
(2)需要98%浓硫酸多少毫升(ρ2=1.84g/cm3)
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】小明在老师的指导下测一瓶稀盐酸的溶质质量分数,具体步骤如下:
步骤一:配制溶质质量分数为10%的氢氧化钠溶液。
步骤二:向20克待测稀盐酸中逐滴滴入上述氢氧化钠溶液,并使用pH计记录溶液的pH变化情况,绘制图像如下图。

(1)在步骤一中需要用到的玻璃仪器有________ 。(写出两种)
(2)在往稀盐酸中逐渐滴入氢氧化钠溶液的过程中,当溶液的pH达到2时,溶液中的溶质有________ 。(用化学式表示)
(3)已知发生反应的化学方程式为:NaOH + HCl=NaCl + H2O,请结合右图,计算该稀盐酸的溶质质量分数。________ (结果精确到0.01%)
步骤一:配制溶质质量分数为10%的氢氧化钠溶液。
步骤二:向20克待测稀盐酸中逐滴滴入上述氢氧化钠溶液,并使用pH计记录溶液的pH变化情况,绘制图像如下图。

(1)在步骤一中需要用到的玻璃仪器有
(2)在往稀盐酸中逐渐滴入氢氧化钠溶液的过程中,当溶液的pH达到2时,溶液中的溶质有
(3)已知发生反应的化学方程式为:NaOH + HCl=NaCl + H2O,请结合右图,计算该稀盐酸的溶质质量分数。
您最近一年使用:0次
解答题
|
适中
(0.65)
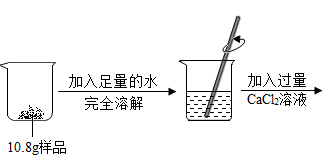
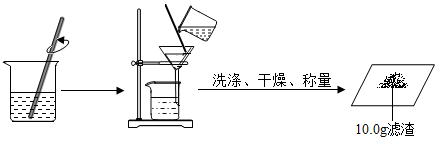
【推荐1】国家标准规定工业纯碱中碳酸钠的质量分数≥98.0%为合格品。为测定某工业纯碱是否为合格品,兴趣小组成员分别进行了如图的实验。(杂质可溶于水且不参与反应,过滤后滤渣损失忽略不计)
(1)实验中加入过量CaCl2溶液的目的是_________;
(2)若滤渣未经干燥便进行称量,会导致碳酸钠质量分数的计算结果________ (填“偏大”或“偏小”);
(3)通过计算判断该工业纯碱是否为合格品。(写出计算过程,结果精确到0.1%)
(1)实验中加入过量CaCl2溶液的目的是_________;
(2)若滤渣未经干燥便进行称量,会导致碳酸钠质量分数的计算结果________ (填“偏大”或“偏小”);
(3)通过计算判断该工业纯碱是否为合格品。(写出计算过程,结果精确到0.1%)


您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】向含溶质40.0g的NaOH溶液中缓慢通入64.0g SO2气体,请分析通入SO2的质量与溶液中溶质组成的关系,填写下表空格。
请画出溶液中溶质的总质量随缓慢通入SO2的质量的变化曲线。(作图时请在起点、拐点和终点注明坐标)
________________________
| M(SO2)的范围/g | 溶液中溶质的化学式 |
| (0, 32.0) | (1) |
| (2) |  、 、 |
请画出溶液中溶质的总质量随缓慢通入SO2的质量的变化曲线。(作图时请在起点、拐点和终点注明坐标)
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐3】为测定某NaCl、Na2CO3固体混合物的组成,小明同学取16g该混合物放入烧杯中,分五次加入稀盐酸(每次加入稀盐酸的质量为25g),待反应完全后,得到下面的质量关系:
请分析以上数据后计算:
(1)原固体混合物中Na2CO3的质量______________ 。
(2)当加入稀盐酸至固体混合物恰好完全反应时,所得溶液的溶质质量分数__________ 。
| 加入稀盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 烧杯及反应后混合物的总质量/g | 122.2 | 146.1 | 170.0 | 193.9 | 218.9 |
请分析以上数据后计算:
(1)原固体混合物中Na2CO3的质量
(2)当加入稀盐酸至固体混合物恰好完全反应时,所得溶液的溶质质量分数
您最近一年使用:0次




