初三某班利用稀硫酸与氧化铜粉末反应探究稀硫酸的化学性质,实验后废液集中在一个废液缸中。为了探究废液的成分,同学们又进行了如下实验:取上层废液于烧杯中,加入一定溶质质量分数的氢氧化钠溶液。下表为生成沉淀总质量与所加氢氧化钠溶液总质量的关系。
(1)表中n=___________。
(2)所取的废液中溶质是___________。
(3)所加氢氧化钠溶液溶质的质量分数是多少?
| 氢氧化钠溶液总质量/g | 20 | 40 | 60 | 80 | 100 | 120 |
| 生成沉淀总质量/g | 0.49 | 2.94 | 5.39 | m | n | 9.8 |
(2)所取的废液中溶质是___________。
(3)所加氢氧化钠溶液溶质的质量分数是多少?
更新时间:2022-05-19 09:06:09
|
相似题推荐
解答题
|
适中
(0.65)
【推荐1】小金做了两个实验如图所示。

(1)试管A有明显的实验现象,请用化学方程式解释:_____ 。
(2)由于在试管B没有观察到明显实验现象,于是小徐同学对稀盐酸能否与氢氧化钡发生反应表示质疑。老师告诉他,只要在实验前向装有氢氧化钡的试管中滴加几滴石蕊试液,再滴加稀盐酸,当观察到_____ 的现象时,就能证明两种物质发生反应了。
(3)实验结束后,他将试管A和试管B的液体倒入到一个空烧杯中。
①若只观察到有气泡产生的现象,则试管A的溶液中含有的阴离子_____ (填符号)。
②若开始阶段观察到有气泡,一段时间后又出现白色沉淀的现象。待反应结束后,将烧杯中混合液过滤,滤液中的溶质除氯化钾外,还可能有_____ (填化学式)。

(1)试管A有明显的实验现象,请用化学方程式解释:
(2)由于在试管B没有观察到明显实验现象,于是小徐同学对稀盐酸能否与氢氧化钡发生反应表示质疑。老师告诉他,只要在实验前向装有氢氧化钡的试管中滴加几滴石蕊试液,再滴加稀盐酸,当观察到
(3)实验结束后,他将试管A和试管B的液体倒入到一个空烧杯中。
①若只观察到有气泡产生的现象,则试管A的溶液中含有的阴离子
②若开始阶段观察到有气泡,一段时间后又出现白色沉淀的现象。待反应结束后,将烧杯中混合液过滤,滤液中的溶质除氯化钾外,还可能有
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】实验室有一瓶久置的氢氧化钠固体,实验员猜测固体已变质,为验证其猜想,取少量该固体样品进行如下实验:(提示:CaCl2溶液显中性)

(1)上述实验中,A操作的名称是______ ;
(2)“无色溶液”中除了CaCl2,还有其它溶质为:______ ;
(3)取10g已变质的氢氧化钠固体于干燥的烧杯中,并向其中加入100g一定质量分数的稀盐酸,充分反应后称得溶液的质量为107.8g,求:
①样品中没有发生变质的氢氧化钠的质量______ ;
②氢氧化钠固体在变质前的质量是多少______ 。

(1)上述实验中,A操作的名称是
(2)“无色溶液”中除了CaCl2,还有其它溶质为:
(3)取10g已变质的氢氧化钠固体于干燥的烧杯中,并向其中加入100g一定质量分数的稀盐酸,充分反应后称得溶液的质量为107.8g,求:
①样品中没有发生变质的氢氧化钠的质量
②氢氧化钠固体在变质前的质量是多少
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐3】实验室里有 、
、 两瓶久置的氢氧化钠固体,为测定两瓶氢氧化钠固体的变质程度,小博进行了如下实验:
两瓶久置的氢氧化钠固体,为测定两瓶氢氧化钠固体的变质程度,小博进行了如下实验:
①用天平测得 试剂瓶中固体质量为
试剂瓶中固体质量为 ,加入
,加入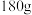 水(足量)溶解后,将其置于电子天平上(如图所示)。
水(足量)溶解后,将其置于电子天平上(如图所示)。
②将质量为 稀盐酸分7次加入烧杯中,使之充分反应,实验结果记录在下表中。
稀盐酸分7次加入烧杯中,使之充分反应,实验结果记录在下表中。
(1)当第2次加入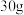 稀盐酸充分反应后,溶液中的溶质为
稀盐酸充分反应后,溶液中的溶质为___________ 。
(2)样品中碳酸钠的质量分数为多少___________ ?
(3)小博结合实验数据,并绘制成如图所示的变化曲线。之后,他也从 试剂瓶中取20克固体重复上述实验,若
试剂瓶中取20克固体重复上述实验,若 中氢氧化钠的变质程度高于
中氢氧化钠的变质程度高于 瓶,请在图中大致画出产生二氧化碳的质量随加入稀盐酸的质量的变化曲线,并在曲线上标出当所有药品恰好完全反应时所消耗的稀盐酸的量,用点Q表示
瓶,请在图中大致画出产生二氧化碳的质量随加入稀盐酸的质量的变化曲线,并在曲线上标出当所有药品恰好完全反应时所消耗的稀盐酸的量,用点Q表示___________ 。

 、
、 两瓶久置的氢氧化钠固体,为测定两瓶氢氧化钠固体的变质程度,小博进行了如下实验:
两瓶久置的氢氧化钠固体,为测定两瓶氢氧化钠固体的变质程度,小博进行了如下实验:①用天平测得
 试剂瓶中固体质量为
试剂瓶中固体质量为 ,加入
,加入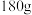 水(足量)溶解后,将其置于电子天平上(如图所示)。
水(足量)溶解后,将其置于电子天平上(如图所示)。②将质量为
 稀盐酸分7次加入烧杯中,使之充分反应,实验结果记录在下表中。
稀盐酸分7次加入烧杯中,使之充分反应,实验结果记录在下表中。| 实验序号 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | 第7次 |
| 加入稀盐酸 的质量(克) | 30 | 30 | 30 | 30 | 30 | 30 | 30 |
| 烧杯中剩余物质 的质量(克) | 230 | 260 | 289.9 | 317.7 | 345.5 | 374.4 | 404.4 |
(1)当第2次加入
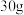 稀盐酸充分反应后,溶液中的溶质为
稀盐酸充分反应后,溶液中的溶质为(2)样品中碳酸钠的质量分数为多少
(3)小博结合实验数据,并绘制成如图所示的变化曲线。之后,他也从
 试剂瓶中取20克固体重复上述实验,若
试剂瓶中取20克固体重复上述实验,若 中氢氧化钠的变质程度高于
中氢氧化钠的变质程度高于 瓶,请在图中大致画出产生二氧化碳的质量随加入稀盐酸的质量的变化曲线,并在曲线上标出当所有药品恰好完全反应时所消耗的稀盐酸的量,用点Q表示
瓶,请在图中大致画出产生二氧化碳的质量随加入稀盐酸的质量的变化曲线,并在曲线上标出当所有药品恰好完全反应时所消耗的稀盐酸的量,用点Q表示
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】为验证Ba(OH)2的化学性质做如图所示的四个实验:

(1)写出实验三中发生反应的化学方程式________ ;
(2)将上述实验后四支试管中的所有物质倒入同一个烧杯,充分混合后过滤,得到白色固体和溶液A。取一定量溶液A,加入少量Ba(OH)2溶液,振荡后只得到无色溶液,综上分析,溶液A中除酚酞外,一定还含有的溶质是_________ 。

(1)写出实验三中发生反应的化学方程式
(2)将上述实验后四支试管中的所有物质倒入同一个烧杯,充分混合后过滤,得到白色固体和溶液A。取一定量溶液A,加入少量Ba(OH)2溶液,振荡后只得到无色溶液,综上分析,溶液A中除酚酞外,一定还含有的溶质是
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】医用氯化钙可用于生产补钙、抗过敏和消炎等药物.以工业碳酸钙(含有少量Al2(CO3)3、Fe2(CO3)3)为原料,经过溶解、除杂、过虑、蒸发结旵等过程,得到较纯的氯化钙晶体,其工艺如下图:

(1)两次加入的酸都是____ (填写酸的名称);其中第二次加入酸的目的是____ 。
(2)滤渣C中一定含有的成分是____ 。

(1)两次加入的酸都是
(2)滤渣C中一定含有的成分是
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】四位同学元旦去仙华山风景区游玩,带回了几小块石灰石样品。为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用浓度相同的稀盐酸与样品充分反应来进行实验测定,(样品中的杂质不溶于水,且不与盐酸反应)测定数据如下:
试回答:
(1)四位同学里面,___________同学的石灰石样品完全反应了;12.0g石灰石样品与___________g稀盐酸恰好完全反应;
(2)样品中碳酸钙的质量分数为多少?(写出计算过程)
(3)请在图中大致画出生成气体的质量与加入稀盐酸质量的变化关系(标注必要的数值)。

| 甲同学 | 乙同学 | 丙同学 | 丁同学 | |
| 所取石灰石样品的质量(g) | 12.0 | 12.0 | 12.0 | 12.0 |
| 加入盐酸的质量(g)烧杯中 | 10.0 | 20.0 | 30.0 | 40.0 |
| 剩余物质的总质量(g) | 21.0 | 30.0 | 39.0 | 48.7 |
试回答:
(1)四位同学里面,___________同学的石灰石样品完全反应了;12.0g石灰石样品与___________g稀盐酸恰好完全反应;
(2)样品中碳酸钙的质量分数为多少?(写出计算过程)
(3)请在图中大致画出生成气体的质量与加入稀盐酸质量的变化关系(标注必要的数值)。

您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】氮氧化物(如NO2、NO等)进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾。因此必须对含有氮氧化物的废气进行处理。
(1)用氢氧化钠溶液可吸收废气中的氮氧化物。反应的化学方程式:NO2+NO+2NaOH═2NaNO2+H2O,产物NaNO2中N元素的化合价为__________ ;已知“HNO2”读作“亚硝酸”,则NaNO2的名称为__________ 。NaNO2中氮、氧两种元素的质量比__________ 。
(2)氨气(NH3)也可用来处理氮氧化物。例如,氨气与二氧化氮反应:8NH3+6NO2═7N2+12H2O。若某工厂排出废气中NO2含量为1.38%,则处理1.0×103米3这种废气,需要多少千克氨气(假设此时NO2气体的密度为2.0克/升)?___
(1)用氢氧化钠溶液可吸收废气中的氮氧化物。反应的化学方程式:NO2+NO+2NaOH═2NaNO2+H2O,产物NaNO2中N元素的化合价为
(2)氨气(NH3)也可用来处理氮氧化物。例如,氨气与二氧化氮反应:8NH3+6NO2═7N2+12H2O。若某工厂排出废气中NO2含量为1.38%,则处理1.0×103米3这种废气,需要多少千克氨气(假设此时NO2气体的密度为2.0克/升)?
您最近一年使用:0次




