有一瓶敞口放置的氢氧化钠固体,为判断是否变质,进行了以下操作。
(1)向装有少量该固体的试管中加过量稀盐酸,如果现象为___________,可知氢氧化钠变质;
(2)为进一步确定其变质程度,另取16g样品配成溶液,配制过程如下。烧杯A、B、C中的溶液一定为饱和溶液的是___________;

(3)向(2)中的C烧杯逐滴加入10% 氯化钙溶液,产生沉淀的质量与氯化钙溶液的质量关系如图所示,计算16克样品中碳酸钠的质量。


(1)向装有少量该固体的试管中加过量稀盐酸,如果现象为___________,可知氢氧化钠变质;
(2)为进一步确定其变质程度,另取16g样品配成溶液,配制过程如下。烧杯A、B、C中的溶液一定为饱和溶液的是___________;

(3)向(2)中的C烧杯逐滴加入10% 氯化钙溶液,产生沉淀的质量与氯化钙溶液的质量关系如图所示,计算16克样品中碳酸钠的质量。


更新时间:2022-05-30 00:16:42
|
【知识点】 根据化学反应方程式的计算
相似题推荐
解答题
|
较易
(0.85)
【推荐1】工业上常采用“天然苛化法”制取氢氧化钠,部分流程如下:

(1)生产工艺中可以回收再利用的物质是________ 。
(2)由天然碱得到碳酸钠溶液时,将天然碱粉碎的目的是__________ 。
(3)制备时将53克溶质质量分数为20%的碳酸钠溶液与17克石灰乳(含水)混合,若二者恰好完全反应,计算经过浓缩、结晶后(不计损失),则可制得氢氧化钠晶体的质量(写出计算过程)。_______

(1)生产工艺中可以回收再利用的物质是
(2)由天然碱得到碳酸钠溶液时,将天然碱粉碎的目的是
(3)制备时将53克溶质质量分数为20%的碳酸钠溶液与17克石灰乳(含水)混合,若二者恰好完全反应,计算经过浓缩、结晶后(不计损失),则可制得氢氧化钠晶体的质量(写出计算过程)。
您最近一年使用:0次
解答题
|
较易
(0.85)
【推荐2】某化学兴趣小组为测定大理石中碳酸钙的含量,进行如图1所示实验:将过量的稀盐酸加入到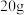 大理石中(其他成分不与盐酸反应),把产生的
大理石中(其他成分不与盐酸反应),把产生的 气体用足量的烧碱溶液吸收,同时测量C瓶烧碱溶液增加的质量(B中所装碳酸氢钠溶液作用是吸收挥发出的
气体用足量的烧碱溶液吸收,同时测量C瓶烧碱溶液增加的质量(B中所装碳酸氢钠溶液作用是吸收挥发出的 气体,不考虑反应产生的二氧化碳对实验的影响),结果如下表所示:
气体,不考虑反应产生的二氧化碳对实验的影响),结果如下表所示:
________ 克。
(2)计算大理石样品中碳酸钙的质量分数。___________ (写出计算过程)
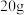 大理石中(其他成分不与盐酸反应),把产生的
大理石中(其他成分不与盐酸反应),把产生的 气体用足量的烧碱溶液吸收,同时测量C瓶烧碱溶液增加的质量(B中所装碳酸氢钠溶液作用是吸收挥发出的
气体用足量的烧碱溶液吸收,同时测量C瓶烧碱溶液增加的质量(B中所装碳酸氢钠溶液作用是吸收挥发出的 气体,不考虑反应产生的二氧化碳对实验的影响),结果如下表所示:
气体,不考虑反应产生的二氧化碳对实验的影响),结果如下表所示:时间/分 | 0 | 2 | 4 | 6 | 8 | 10 |
C瓶溶液增加的质量 | 0 | 3.0 | 5.0 | 6.0 | 6.6 | 6.6 |

(2)计算大理石样品中碳酸钙的质量分数。
您最近一年使用:0次
解答题
|
较易
(0.85)
【推荐3】四氯化硅(SiCl4)是一种重要的化工原料,遇水会发生如下反应:SiCl4+3H2O═H2SiO3↓+4HCl。某地曾发生将含有四氯化硅的废料倒入池塘造成污染事件,事后环保人员在受污染的池塘中投放熟石灰[Ca(OH)2]做了有效处理。
(1)已知H2SiO3不跟Ca(OH)2反应,为了确定投入熟石灰的质量,要先测定废料倒入池塘后生成HCl的质量,选用下列哪组数据能确定池塘中生成HCl的质量________ ;
A.倒入废料的总质量,废料中SiCl4的质量分数
B.池塘水的的pH
C.池塘水中HCl的质量分数
(2)经测定池塘水中共有7.3kgHCl,则需要加入多少吨熟石灰才能将其完全反应___ (列式计算,相对原子质量:1、:16、:35.5、:40)
(1)已知H2SiO3不跟Ca(OH)2反应,为了确定投入熟石灰的质量,要先测定废料倒入池塘后生成HCl的质量,选用下列哪组数据能确定池塘中生成HCl的质量
A.倒入废料的总质量,废料中SiCl4的质量分数
B.池塘水的的pH
C.池塘水中HCl的质量分数
(2)经测定池塘水中共有7.3kgHCl,则需要加入多少吨熟石灰才能将其完全反应
您最近一年使用:0次



