“氯碱工业”是我国目前化学工业的重要支柱之一,它的主要原理是电解饱和食盐水,其化学方程式为xNaCl+2H2O xNaOH+H2↑+Cl2↑。在20℃时,取100g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g。已知:20℃时,NaCl的溶解度为36g。请分析并计算回答:
xNaOH+H2↑+Cl2↑。在20℃时,取100g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g。已知:20℃时,NaCl的溶解度为36g。请分析并计算回答:
(1)运用质量守恒定律可知上述反应中x=__________。
(2)通过计算,求上述过程中同时产生H2的质量。
(3)计算电解后剩余溶液中NaCl的质量分数(写出计算过程,结果精确到0. 1%)。
 xNaOH+H2↑+Cl2↑。在20℃时,取100g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g。已知:20℃时,NaCl的溶解度为36g。请分析并计算回答:
xNaOH+H2↑+Cl2↑。在20℃时,取100g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g。已知:20℃时,NaCl的溶解度为36g。请分析并计算回答:(1)运用质量守恒定律可知上述反应中x=__________。
(2)通过计算,求上述过程中同时产生H2的质量。
(3)计算电解后剩余溶液中NaCl的质量分数(写出计算过程,结果精确到0. 1%)。
更新时间:2020-10-27 09:32:19
|
相似题推荐
解答题
|
较难
(0.4)
名校
【推荐1】硝酸溶解废旧CPU所得溶液中含有 和
和 ,用适当浓度的盐酸、氯化钠溶液、氨水和铁粉,按照如图方法回收Cu和Ag(图中标注的试剂均不同)。
,用适当浓度的盐酸、氯化钠溶液、氨水和铁粉,按照如图方法回收Cu和Ag(图中标注的试剂均不同)。
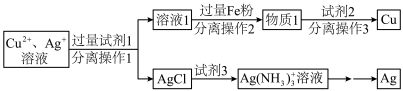
(1)加入过量Fe粉发生的主要反应为___________ (写化学方程式);
(2)试剂1和试剂3的名称依次是___________ ;
(3)若向66g物质1中加入100g试剂2后,恰好完全反应,剩余固体质量为60.4g。求所得溶液中溶质的质量分数为___________ 。(计算结果精确到0.1%)。
 和
和 ,用适当浓度的盐酸、氯化钠溶液、氨水和铁粉,按照如图方法回收Cu和Ag(图中标注的试剂均不同)。
,用适当浓度的盐酸、氯化钠溶液、氨水和铁粉,按照如图方法回收Cu和Ag(图中标注的试剂均不同)。
(1)加入过量Fe粉发生的主要反应为
(2)试剂1和试剂3的名称依次是
(3)若向66g物质1中加入100g试剂2后,恰好完全反应,剩余固体质量为60.4g。求所得溶液中溶质的质量分数为
您最近一年使用:0次
解答题
|
较难
(0.4)
名校
【推荐2】已知30℃时100克水中溶解50克氯化铵恰好达到饱和,30℃时将80克氯化铵配制成400克的溶液。
(1)计算此时溶液的溶质质量分数。______
(2)若不饱和,为了使其饱和可用下面的方法:
①蒸发溶剂法:需蒸发多少克水才能成为饱和溶液?______
②加溶质法:需再加入多少克氯化铵才能成为饱和溶液?_____________
(1)计算此时溶液的溶质质量分数。
(2)若不饱和,为了使其饱和可用下面的方法:
①蒸发溶剂法:需蒸发多少克水才能成为饱和溶液?
②加溶质法:需再加入多少克氯化铵才能成为饱和溶液?
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】某同学在一份资料中了解到:铜有CuO和Cu2O(红色)两种常见的氧化物。因为Cu和Cu2O均为红色,故他们猜测,在H2还原CuO所得的红色产物中可能含有Cu2O。(H2+CuO ═ Cu+H2O反应条件“△”)
(1)该同学准确称取了8.0g黑色CuO粉末放入大试管中,不断通入足量的H2,在加热条件下进行还原,如果产物只有Cu,其质量应为___________________ 。
(2)该同学在H2还原CuO时,当发现8.0g黑色CuO粉末全部转变成红色时,停止加热,冷却后称得固体质量为6.8g。此红色固体中氧元素的质量为___________ ,以此推得Cu2O的质量为______________ 。
(3)将⑵中所得的6.8g固体放入烧杯中,加入48.0g过量稀盐酸(Cu2O与稀盐酸的反应为:Cu2O+2HCl=CuCl2+Cu+H2O),充分搅拌,除有红色固体外,还发现溶液变蓝。试计算此蓝色溶液中CuCl2的质量分数?______
(1)该同学准确称取了8.0g黑色CuO粉末放入大试管中,不断通入足量的H2,在加热条件下进行还原,如果产物只有Cu,其质量应为
(2)该同学在H2还原CuO时,当发现8.0g黑色CuO粉末全部转变成红色时,停止加热,冷却后称得固体质量为6.8g。此红色固体中氧元素的质量为
(3)将⑵中所得的6.8g固体放入烧杯中,加入48.0g过量稀盐酸(Cu2O与稀盐酸的反应为:Cu2O+2HCl=CuCl2+Cu+H2O),充分搅拌,除有红色固体外,还发现溶液变蓝。试计算此蓝色溶液中CuCl2的质量分数?
您最近一年使用:0次
解答题
|
较难
(0.4)
真题
【推荐2】黄铜是铜和锌的合金,某化学兴趣小组的同学在测定黄铜中铜的含量时,取黄铜样品40g,放入烧杯中,向其中加入200g稀硫酸,恰好完全反应,反应后烧杯中剩余物的总质量为239.6g,请计算:
①、产生氢气的质量是 ;
②、参与反应的稀硫酸的质量是 ;
③、黄铜中铜的质量分数
①、产生氢气的质量是 ;
②、参与反应的稀硫酸的质量是 ;
③、黄铜中铜的质量分数
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐3】以石灰石为主要原料的“石头纸”,之一种介于纸张和塑料之间的新型材料,既可替代传统部分纸张,又能替代传统部分塑料包装物,为测定“石头纸”中碳酸钙的含量,课外活动小组的同学先在4只烧杯中加入一定量的“石头纸”样品,再分别加入50g稀盐酸,充分反应后测量生成的气体质量,实验数据见表(假设纸张其他成分既不溶于酸,也不与酸反应)
(1)表中m的数值是_______ 。
(2)求“石头纸”样品中碳酸钙的质量分数。_______
(3)求该盐酸溶液的质量分数_______ (写出计算过程)
| 烧杯① | 烧杯② | 烧杯③ | 烧杯④ | |
| 加入“石头纸”样品的质量/g | 5 | 10 | 15 | 20 |
| 加入稀盐酸的质量/g | 50 | 50 | 50 | 50 |
| 充分反应后生成气体的质量/g | 1.76 | 3.52 | 4.4 | m |
(1)表中m的数值是
(2)求“石头纸”样品中碳酸钙的质量分数。
(3)求该盐酸溶液的质量分数
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】实验室用足量的稀盐酸和大理石制取CO2, 为了分析反应后滤液的成分,取100g反应后的滤液,逐滴滴入溶质质量分数为20.0%的Na2CO3溶液,测得滴加溶液的质量与产生沉淀的关系如图。回答下列问题:(已知:CaCl2溶液呈中性)
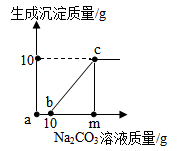
(1)从开始加入碳酸钠溶液至10g时,没有产生沉淀的原因是________ 。
(2)计算原滤液中氯化钙的质量。________
(3)通过计算求出图中m的大小。________
(4)随着滴加Na2CO3溶液质量的增加,烧杯中溶液的pH也呈现一定的变化规律。结合图像判断:b→c段烧杯中溶 液pH如何变化?________ 。

(1)从开始加入碳酸钠溶液至10g时,没有产生沉淀的原因是
(2)计算原滤液中氯化钙的质量。
(3)通过计算求出图中m的大小。
(4)随着滴加Na2CO3溶液质量的增加,烧杯中溶液的pH也呈现一定的变化规律。结合图像判断:b→c段烧杯中溶 液pH如何变化?
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】工业纯碱中常含有少量的氯化钠。某学习小组对其组成展开探究。现取24g纯碱样品,加入100g水使其完全溶解,再加入96g过量的氯化钙溶液,完全反应后,过滤、洗涤、干燥得沉淀20g。完成下列问题:
(1)反应后溶液中含有的溶质是____________ 。(写化学式)。
(2)通过已知数据,能求出的量有_____ (写字母序号)。
A.反应后溶液的总质量
B.参加反应的氯化钙的质量
C.样品中碳酸钠的质量分数
D.氯化钙溶液中溶质的质量分数
(3)计算反应后溶液中氯化钠的质量分数。(写出计算过程,结果保留到0.1%)_____
(1)反应后溶液中含有的溶质是
(2)通过已知数据,能求出的量有
A.反应后溶液的总质量
B.参加反应的氯化钙的质量
C.样品中碳酸钠的质量分数
D.氯化钙溶液中溶质的质量分数
(3)计算反应后溶液中氯化钠的质量分数。(写出计算过程,结果保留到0.1%)
您最近一年使用:0次



