现有硝酸钡和稀硝酸的混合溶液, 向该混合溶液中滴入X溶液,产生沉淀的质量与加入X溶液质量的关系图象有如下3种可能:
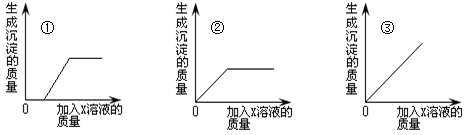
请回答:
(1)若X为Na2SO4 , 则对应的图象应为______ (填标号),所发生的反应的化学方程式为________ 。
(2)若X为Na2CO3 , 则对应的图象应为________ (填标号)。

请回答:
(1)若X为Na2SO4 , 则对应的图象应为
(2)若X为Na2CO3 , 则对应的图象应为
更新时间:2016-12-29 09:18:32
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】如图以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同.结合此图回答下列问题:

(1)稀盐酸中阳离子的符号是________ ;
(2)反应②中现象为________ ;
(3)反应⑤的化学方程式为________ ;
(4)图中属于复分解反应的有________ (填序号);
(5)若X溶液既能跟稀盐酸反应,又能跟Ca(OH)2反应,则X可能是(BaCl2、CuSO4、K2CO3)中的________ .

(1)稀盐酸中阳离子的符号是
(2)反应②中现象为
(3)反应⑤的化学方程式为
(4)图中属于复分解反应的有
(5)若X溶液既能跟稀盐酸反应,又能跟Ca(OH)2反应,则X可能是(BaCl2、CuSO4、K2CO3)中的
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】现有 4 瓶失去标签的溶液,分别为 Ba(NO3)2、H2SO4、BaCl2、NaOH,某同学设计了如下方案:
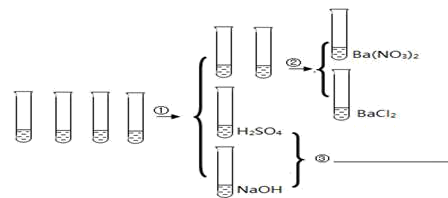
(1)步骤①滴加紫色石蕊试剂,试管中出现________ 现象,则该试管盛放的是 NaOH 溶液。
(2)若要区分 Ba(NO3)2 和 BaCl2 , 则②中需要添加的试剂是________ 。
(3)③处两试管的液体倒入烧杯,请写出反应的化学方程式________ 。

(1)步骤①滴加紫色石蕊试剂,试管中出现
(2)若要区分 Ba(NO3)2 和 BaCl2 , 则②中需要添加的试剂是
(3)③处两试管的液体倒入烧杯,请写出反应的化学方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】黑白复印机用的墨粉中常添加Fe3O4粉末。Fe3O4是由Fe2+、Fe3+和O2﹣按1:2:4的个数比构成的。下图是氧化沉淀法生产复印用Fe3O4粉末的流程简图.已知第④步反应中各元素化合价保持不变.

(1)Fe3O4粉末在复印机的电磁场作用下能使墨粉形成字迹或图案,这不仅利用了Fe3O4有磁性,还利用了Fe3O4是________ 色。
(2)第②步加入试剂X,生成Fe(OH)2的反应方程式为_______ 。
(3)在第③步反应中要控制通入O2的量,以使生成的Fe(OH)2和Fe(OH)3的质量比等于________ ,才能确保最终生成Fe3O4。

(1)Fe3O4粉末在复印机的电磁场作用下能使墨粉形成字迹或图案,这不仅利用了Fe3O4有磁性,还利用了Fe3O4是
(2)第②步加入试剂X,生成Fe(OH)2的反应方程式为
(3)在第③步反应中要控制通入O2的量,以使生成的Fe(OH)2和Fe(OH)3的质量比等于
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】初中化学中物质鉴别与除杂是非常重要内容,充分体现了学生对物质转化规律的掌握程度,下面请同学仔细思考并解答下面两个小题:
① FeCl3溶液中混有少量的稀HCl,欲除去稀HCl,可向溶液中加入过量的________ ,待充分反应后过滤,反应的化学方程为______________ 。
②实验桌上有四瓶无色溶液,只知是稀HCl、Na2SO4、Na2CO3、NaOH溶液中的各一种,小明欲借助下列试剂的一种将四瓶无色溶液鉴别出来,你认为可行的有_____ (填代号)。
①BaCl2溶液 ②Ca(OH)2溶液 ③酚酞试液 ④石蕊试液
① FeCl3溶液中混有少量的稀HCl,欲除去稀HCl,可向溶液中加入过量的
②实验桌上有四瓶无色溶液,只知是稀HCl、Na2SO4、Na2CO3、NaOH溶液中的各一种,小明欲借助下列试剂的一种将四瓶无色溶液鉴别出来,你认为可行的有
①BaCl2溶液 ②Ca(OH)2溶液 ③酚酞试液 ④石蕊试液
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】硝酸钾是一种重要的工业原料,我国年产量达到6万多吨。小科和小宁在实验室用不同的方案制取硝酸钾。
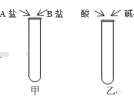
I. 小科将A、B盐加到装有少量水的试管中,充分振荡制取硝酸钾,如图甲。
II.小宁向试管中依次加入浓度为10%的酸溶液15g,浓度为15%的碱溶液8g,充分振荡制取硝酸钾,如图乙。
[实验分析]
(1)小宁想分析小科所用的A、B盐成分,分别取A、B盐配成溶液后进行以下实验。
I.取少量A、B盐溶液分别滴加稀盐酸,A盐溶液有气泡生成,B盐溶液无明显现象。
II.另取少量A、B盐溶液,分别滴加氢氧化钠溶液,A、B盐溶液均无明显现象。
则B盐可能是___________ (写出一种即可) 。
(2)工业生产中,目的产物的实际生成量占目的产物的理论生成量的百分率称为收率。已知小宁最终制得硝酸钾1.8g,则反应的收率为___________ ( 计算结果保留到0.1%) 。
(3)请你从安全的角度,对小宁制取硝酸钾的方案进行评价:___________ 。
I. 小科将A、B盐加到装有少量水的试管中,充分振荡制取硝酸钾,如图甲。
II.小宁向试管中依次加入浓度为10%的酸溶液15g,浓度为15%的碱溶液8g,充分振荡制取硝酸钾,如图乙。
[实验分析]
(1)小宁想分析小科所用的A、B盐成分,分别取A、B盐配成溶液后进行以下实验。
I.取少量A、B盐溶液分别滴加稀盐酸,A盐溶液有气泡生成,B盐溶液无明显现象。
II.另取少量A、B盐溶液,分别滴加氢氧化钠溶液,A、B盐溶液均无明显现象。
则B盐可能是
(2)工业生产中,目的产物的实际生成量占目的产物的理论生成量的百分率称为收率。已知小宁最终制得硝酸钾1.8g,则反应的收率为
(3)请你从安全的角度,对小宁制取硝酸钾的方案进行评价:
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】在烧杯中加入氯化钠和碳酸氢钠的固体混合物10.0g后,再加入73g稀盐酸恰好完全反应。反应过程用精密仪器测得烧杯连同药品的总质量(m)与反应时间(t)的关系如图所示。烧杯连同药品的起始总质量为165.0g。反应的方程式为NaHCO3+HCl=NaCl+H2O+CO2↑;试回答下列问题:

(1)完全反应时产生二氧化碳的质量为________ g。
(2)NaHCO3中碳元素的质量分数是_______
(3)稀盐酸中溶质的质量分数是多少?______
(4)反应后所得氯化钠溶液中有氯化钠溶质________ 克。

(1)完全反应时产生二氧化碳的质量为
(2)NaHCO3中碳元素的质量分数是
(3)稀盐酸中溶质的质量分数是多少?
(4)反应后所得氯化钠溶液中有氯化钠溶质
您最近一年使用:0次



