实验小组研究盐酸、氢氧化钠的化学性质,做了如图甲所示的实验.请你利用图中所给药品和他们一起进行研究。
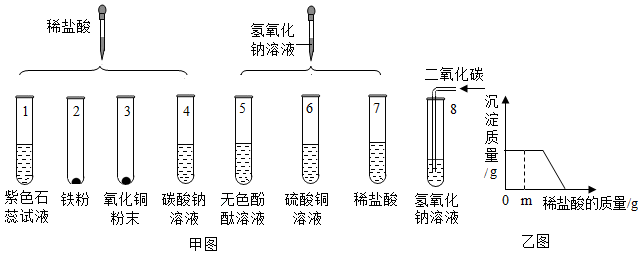
(1)实验后得到红色溶液的是_____________ (填试管序号,下同);有盐和水生成的实验是______________ ;
(2)实验中有明显现象产生,最终得到无色溶液,该试管内发生反应的化学方程式为____________________________________________________ ;
(3)实验后某试管内产生蓝色絮状沉淀的化学方程式为:________________________________ ,继续向该试管中滴加足量的稀盐酸,试管内沉淀的质量与加入稀盐酸的质量关系如图乙所示。当滴加稀盐酸至mg时,静置试管,试管内上层清液中的溶质为______________________ 。

(1)实验后得到红色溶液的是
(2)实验中有明显现象产生,最终得到无色溶液,该试管内发生反应的化学方程式为
(3)实验后某试管内产生蓝色絮状沉淀的化学方程式为:
更新时间:2018-11-14 22:13:18
|
相似题推荐
探究题
|
较难
(0.4)
【推荐1】小娜及学习小组的同学在老师的指导下,对黄铜中铜和锌的含量及其性质展开了探究。
【查阅资料】HCl+AgNO3=AgCl↓+HNO3,AgCl是一种白色沉淀,这个反应在化学上用于检验和鉴别。
【提出问题】测定黄铜中锌、铜的质量分数。
【实验原理及实验方案设计】(略)。
【探究实验】
(1)先将黄铜在热碱液中浸泡一段时间,以除去表面的油污。然后再放在稀盐酸中浸泡片刻,其目的是_______ 。用蒸馏水清洗干净,干燥,取少量研碎,称取质量为ag。
(2)将ag试样放入小烧杯中,加入足量稀盐酸,搅拌使其充分反应。
(3)将小烧杯中的混合物过滤,______ (请将此实验步骤补充完整)。
(4)称取固体的质量为bg。
(5)计算出黄铜中锌和铜的质量分数。
【反思与评价】在步骤1中,若试样用蒸馏水洗涤之后,不干燥,则计算出合金中锌的质量分数将_____ (填“偏大”、“偏小”或“不受影响”)。
【拓展探究】
(1)重复【探究实验】步骤1。
(2)将ag试样放入一定量的硝酸银溶液中,使其充分反应后过滤,得到固体和蓝色滤液,并对滤液的组成进行探究。
①锌和硝酸银溶液反应的化学方程式是_____ 。
②同学们对蓝色滤液中所含的溶质做出多种猜想,其中只有两种猜想可能成立,这两种猜想是:①溶质为硝酸锌和硝酸铜;②溶质为_______ 。
③设计一种实验方案来验证以上猜想:
【查阅资料】HCl+AgNO3=AgCl↓+HNO3,AgCl是一种白色沉淀,这个反应在化学上用于检验和鉴别。
【提出问题】测定黄铜中锌、铜的质量分数。
【实验原理及实验方案设计】(略)。
【探究实验】
(1)先将黄铜在热碱液中浸泡一段时间,以除去表面的油污。然后再放在稀盐酸中浸泡片刻,其目的是
(2)将ag试样放入小烧杯中,加入足量稀盐酸,搅拌使其充分反应。
(3)将小烧杯中的混合物过滤,
(4)称取固体的质量为bg。
(5)计算出黄铜中锌和铜的质量分数。
【反思与评价】在步骤1中,若试样用蒸馏水洗涤之后,不干燥,则计算出合金中锌的质量分数将
【拓展探究】
(1)重复【探究实验】步骤1。
(2)将ag试样放入一定量的硝酸银溶液中,使其充分反应后过滤,得到固体和蓝色滤液,并对滤液的组成进行探究。
①锌和硝酸银溶液反应的化学方程式是
②同学们对蓝色滤液中所含的溶质做出多种猜想,其中只有两种猜想可能成立,这两种猜想是:①溶质为硝酸锌和硝酸铜;②溶质为
③设计一种实验方案来验证以上猜想:
| 方案 | 实验操作 | 实验现象 | 结论 |
| 方案一 | 取少量滤液于试管中,在滤液中插入一根铜丝 | 猜想①成立 | |
| 猜想②成立 | |||
| 方案二 | 猜想①成立 | ||
| 猜想②成立 |
您最近一年使用:0次
探究题
|
较难
(0.4)
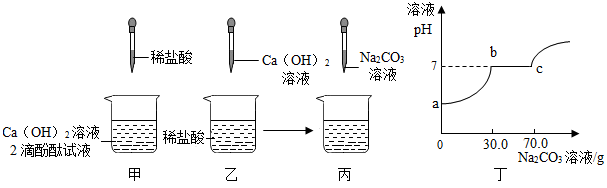
【推荐2】某实验小组的同学在做氢氧化钙溶液与稀盐酸反应的实验时,忘记加入指示剂,为探究反应溶液中溶质的成分,又进行了以下实验探究。
【提出问题】反应后溶液中溶质是什么?
【假设猜想】猜想一:溶质是CaCl2; 猜想二:溶质是CaCl2和Ca(OH)2
猜想三:溶质是____________ ; 猜想四:溶质是CaCl2、Ca(OH)2和HCl
【资料】CaCl2溶液呈中性
同学们经过讨论,一致认为猜想四是错误的,理由是___________________ ;
【交流反思】边巴同学认为,用下列试剂____________ (填序号),也可以得出上述猜想三成立。
①AgNO3 ②Fe2O3 ③NaOH
【拓展延伸】
(1)在判断反应后所得溶液中溶质成分时,既要考虑生成物,还要考虑反应物是否过量;
(2)倾倒猜想三的废液前,可向废液中加入足量__________ 并过滤,才能使废液中的溶质只含有CaCl2。
【提出问题】反应后溶液中溶质是什么?
【假设猜想】猜想一:溶质是CaCl2; 猜想二:溶质是CaCl2和Ca(OH)2
猜想三:溶质是
【资料】CaCl2溶液呈中性
同学们经过讨论,一致认为猜想四是错误的,理由是
| 实验操作 | 实验现象 | 结论 | |
| 实验一 | 取少量反应后的溶液于试管中,滴入酚酞溶液 | 溶液不变色 | 猜想二不成立 |
| 实验二 | 再取少量反应后的溶液与另一支试管中,加入少量铁粉 | 产生气泡 | 猜想三成立 |
【交流反思】边巴同学认为,用下列试剂
①AgNO3 ②Fe2O3 ③NaOH
【拓展延伸】
(1)在判断反应后所得溶液中溶质成分时,既要考虑生成物,还要考虑反应物是否过量;
(2)倾倒猜想三的废液前,可向废液中加入足量
您最近一年使用:0次
探究题
|
较难
(0.4)
【推荐1】一次用餐中,小胡同学对“固体酒精”产生好奇,于是他决定买回一袋,对其进行研究。
【收集资料】通过阅读标签及查阅资料,他获得如下信息:
(1)该固体酒精中含有酒精、氯化钙、氢氧化钠三种物质;
(2)酒精的化学式为C2H5OH;
(3)氯化钙、氯化钡的水溶液均呈中性。
【提出问题】
(1)酒精的化学式与NaOH相比,都有“OH”,那么酒精的水溶液是不是显碱性?
(2)固体酒精中的氢氧化钠是否变质及变质的程度如何?
【实验探究】
实验一:他取少量酒精溶液于试管中,滴加硫酸铜溶液,未观察到蓝色沉淀,说明酒精溶液____ (填“显”或“不显”)碱性。
实验二:(1)他先取少量固体酒精于烧杯中,加入足量水溶解后静置,发现烧杯底部有白色沉淀,再取沉淀于试管中加稀盐酸,观察到___ ,说明氢氧化钠已变质。请写出氢氧化钠在空气中变质的化学方程式 ___ 。
(2)他取上述烧杯中上层清液于试管中,先滴加足量澄清石灰水,发现生成白色沉淀,再滴入几滴无色酚酞溶液,液体呈红色,他认为氢氧化钠部分变质。老师发现后,提示他由该实验得出的结论不可靠。你认为只要将上述实验中的澄清石灰水变为____ (填化学式)溶液,即可得到氢氧化钠部分变质的结论。
【收集资料】通过阅读标签及查阅资料,他获得如下信息:
(1)该固体酒精中含有酒精、氯化钙、氢氧化钠三种物质;
(2)酒精的化学式为C2H5OH;
(3)氯化钙、氯化钡的水溶液均呈中性。
【提出问题】
(1)酒精的化学式与NaOH相比,都有“OH”,那么酒精的水溶液是不是显碱性?
(2)固体酒精中的氢氧化钠是否变质及变质的程度如何?
【实验探究】
实验一:他取少量酒精溶液于试管中,滴加硫酸铜溶液,未观察到蓝色沉淀,说明酒精溶液
实验二:(1)他先取少量固体酒精于烧杯中,加入足量水溶解后静置,发现烧杯底部有白色沉淀,再取沉淀于试管中加稀盐酸,观察到
(2)他取上述烧杯中上层清液于试管中,先滴加足量澄清石灰水,发现生成白色沉淀,再滴入几滴无色酚酞溶液,液体呈红色,他认为氢氧化钠部分变质。老师发现后,提示他由该实验得出的结论不可靠。你认为只要将上述实验中的澄清石灰水变为
您最近一年使用:0次
探究题
|
较难
(0.4)
【推荐2】X、Y、Z三种物质有如图所示的转化关系。试推断:

(1)X的化学式是______ ,Z的化学式是_______ 。
(2)试剂甲是______ ,试剂乙是_______ 。
(3)写出YZ的化学方程式:_______ ,属于______ 反应。
(4)写出XZ的化学方程式:________ ,属于______ 反应。

(1)X的化学式是
(2)试剂甲是
(3)写出YZ的化学方程式:
(4)写出XZ的化学方程式:
您最近一年使用:0次
探究题
|
较难
(0.4)
【推荐1】近年来,我国成功发射了“嫦娥—号”探月卫星和神舟系列飞船,标志着我国航天技术的研究已经进入世界领先行列,许多航天技术问题不断地被科学家研究解决。
(1)载人航天技术中难题之一:如何保证宇宙飞船燃料补给?
①下表是不同星体上“大气”(相当于地球上的空气)的主要成分。它们中可能成为宇宙飞船燃料补给站的星体是:___________
② 科学家发现在宇宙飞船飞过冥王星“大气”时,甲烷并没有被点燃,请分析其原因:____ ;
(2)载人航天技术中难题之二:如何提供在往返路程中宇航员呼吸所需要的氧气和消除呼吸过程中产生的二氧化碳等。新型航天飞行器座舱内空气更新过程如下图所示:

①装置Ⅱ是CO2和H2的反应装置,该反应的化学方程式为________________________ (可不写反应条件)。
②从装置Ⅰ、Ⅱ、Ⅲ可看出,O2的来源是CO2和H2O,若宇航员每天呼出的气体中含1012gCO2和180g水蒸气,则通过Ⅰ、Ⅱ、Ⅲ装置完全转化后可得到O2___________ g。
(3)在飞船绕行期间,宇航员翟志刚进行了出舱活动,如图所示是宇航员“漂浮”在地球外层空间的照片。宇航员在舱外活动时____________ 地球引力的作用(填“不受”或“仍受”)。
(4)图中出舱时宇航员穿着厚厚的宇航服,宇航服的作用很多,请写出其中的三点___________ 。

(1)载人航天技术中难题之一:如何保证宇宙飞船燃料补给?
①下表是不同星体上“大气”(相当于地球上的空气)的主要成分。它们中可能成为宇宙飞船燃料补给站的星体是:
| 星体名称 | 星体的“大气”主要成分 |
| 金星 | 二氧化碳、硫酸 |
| 火星 | 二氧化碳 |
| 冥王星 | 甲烷 |
② 科学家发现在宇宙飞船飞过冥王星“大气”时,甲烷并没有被点燃,请分析其原因:
(2)载人航天技术中难题之二:如何提供在往返路程中宇航员呼吸所需要的氧气和消除呼吸过程中产生的二氧化碳等。新型航天飞行器座舱内空气更新过程如下图所示:

①装置Ⅱ是CO2和H2的反应装置,该反应的化学方程式为
②从装置Ⅰ、Ⅱ、Ⅲ可看出,O2的来源是CO2和H2O,若宇航员每天呼出的气体中含1012gCO2和180g水蒸气,则通过Ⅰ、Ⅱ、Ⅲ装置完全转化后可得到O2
(3)在飞船绕行期间,宇航员翟志刚进行了出舱活动,如图所示是宇航员“漂浮”在地球外层空间的照片。宇航员在舱外活动时
(4)图中出舱时宇航员穿着厚厚的宇航服,宇航服的作用很多,请写出其中的三点

您最近一年使用:0次
探究题
|
较难
(0.4)
【推荐2】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2。
(1)请写出该反应的化学方程式:____________________________ 。
(2)探究有关因素对反应速率的影响。某同学在保证催化剂种类和质量不变的前提下设计了三组实验,部分实验条件已经填在下面实验设计表中。请完成以下实验设计表。
实验测得NO浓度随时间变化的关系如下图。

(3)实验①、②表明增大催化剂的表面积,此反应速率就_________ 。
(4)假设在密闭容器中发生上述反应,根据实验结果下列措施能提高NO转化率的是_________ 。
A.选用更有效的催化剂 B.增大催化剂的表面积
C.降低反应体系的温度 D.升高反应体系的温度
(1)请写出该反应的化学方程式:
(2)探究有关因素对反应速率的影响。某同学在保证催化剂种类和质量不变的前提下设计了三组实验,部分实验条件已经填在下面实验设计表中。请完成以下实验设计表。
| 实验编号 | 实验目的 | 温度(℃) | NO初始浓度(g/L) | CO初始浓度(g/L) | 催化剂的表面积(m2) |
| ① | 为②③提供参照 | 280 | 0.036 | 0.1624 | 124 |
| ② | 280 | 82 | |||
| ③ | 探究温度对化学反应速率的影响 | 350 | 0.036 | 0.1624 | 124 |
实验测得NO浓度随时间变化的关系如下图。

(3)实验①、②表明增大催化剂的表面积,此反应速率就
(4)假设在密闭容器中发生上述反应,根据实验结果下列措施能提高NO转化率的是
A.选用更有效的催化剂 B.增大催化剂的表面积
C.降低反应体系的温度 D.升高反应体系的温度
您最近一年使用:0次
探究题
|
较难
(0.4)
【推荐3】已知:
氯气的实验室制法MnO2+4HCl MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
氯气能溶于水,不溶于饱和食盐水。
氯气溶于水得到的氯水呈黄绿色。溶解在水中的部分氯气能与水发生反应,生成盐酸和次氯酸(HClO)。次氯酸能使染料等有机色素褪色,有漂白性,还能杀死水中的细菌,起消毒作用。次氯酸不稳定,容易分解放出氧气,在阳光的照射下,次氯酸分解加快。
工业生产中和实验室常用氢氧化钠溶液吸收氯气尾气。用湿润的淀粉KI试纸检验氯气。
(一)某校化学兴趣小组为研究氯气的性质,设计如图所示装置进行实验,装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。(品红是一种常用的生物染色剂)

(1)写出仪器X中药品的名称________ 。
(2)加入药品前,检查I中气体发生装置气密性的操作是:
用止水夹夹住________ 处,然后向分液漏斗中加水,打开________ (填“A”,“B”或“A和B”),液体不能顺利流下则气密性好。
(3)实验过程中,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象的原因是________ ,为达到预期现象,应如何改进装置________ 。
(4)写出装置V中发生反应的化学方程式________ 。
(二)为了探究某盐X(仅含有三种元素,式量为143)的组成与性质,设计并完成了以下实验。其中气体单质B可使带火星的木条复燃,固体C是常见的中性干燥剂CaCl2。

请回答
(1)化合物X的化学式为________ 。
(2)固体X与稀盐酸反应的化学方程式________ 。
氯气的实验室制法MnO2+4HCl
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O氯气能溶于水,不溶于饱和食盐水。
氯气溶于水得到的氯水呈黄绿色。溶解在水中的部分氯气能与水发生反应,生成盐酸和次氯酸(HClO)。次氯酸能使染料等有机色素褪色,有漂白性,还能杀死水中的细菌,起消毒作用。次氯酸不稳定,容易分解放出氧气,在阳光的照射下,次氯酸分解加快。
工业生产中和实验室常用氢氧化钠溶液吸收氯气尾气。用湿润的淀粉KI试纸检验氯气。
(一)某校化学兴趣小组为研究氯气的性质,设计如图所示装置进行实验,装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。(品红是一种常用的生物染色剂)

(1)写出仪器X中药品的名称
(2)加入药品前,检查I中气体发生装置气密性的操作是:
用止水夹夹住
(3)实验过程中,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象的原因是
(4)写出装置V中发生反应的化学方程式
(二)为了探究某盐X(仅含有三种元素,式量为143)的组成与性质,设计并完成了以下实验。其中气体单质B可使带火星的木条复燃,固体C是常见的中性干燥剂CaCl2。

请回答
(1)化合物X的化学式为
(2)固体X与稀盐酸反应的化学方程式
您最近一年使用:0次