取200g一定质量分数的CuSO4溶液,先逐滴滴加100gBa(OH)2溶液至b点,后再逐滴滴加稀HCl溶液至过量,整个过程中加入溶液的质量与沉淀质量关系如图所示。请回答相关问题:
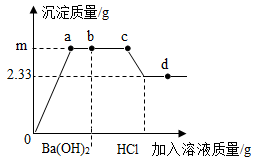
(1)oa 段溶液的导电性将逐渐________ (填“增强”、“减弱”、“不变”);
(2)至d点时溶液中所含的溶质有________ ;
(3)bc段发生反应的化学方程式________ ;
(4)通过计算确定m的值?_________ 。

(1)oa 段溶液的导电性将逐渐
(2)至d点时溶液中所含的溶质有
(3)bc段发生反应的化学方程式
(4)通过计算确定m的值?
更新时间:2019-09-28 08:13:32
|
相似题推荐
解答题
|
较难
(0.4)
【推荐1】有A、B、C三种物质,已知A是一种氯化物,B是一种酸,C是一种碱。如图所示A、B、C三种物质的溶液两两混合时的实验现象,请回答:

(1)A的化学式_____ 。
(2)白色沉淀D的化学式_____

(1)A的化学式
(2)白色沉淀D的化学式
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】按要求写物质的化学式或反应的化学方程式:
(1)检验市场上销售的食盐中是否含有碘元素(元素符号为I) 的一种方法,是在酸性条件下,使食盐样品溶液跟一种试剂X反应(KIO3 +5X+6HCl═6KCl+3I2+3H2O)。这种试剂X是 ,要完成这种实验还需要的一种物质是 (填名称),它遇到 会变蓝。
(2)有一种浸液,其配方如下:NaOH 6g、NaCl 10g、Ca(OH)2 59g、茶叶5g、H2O 210mL,用该浸液浸泡鸭蛋可制无泥皮蛋。配制浸液时,是否可以用生石灰和纯碱代替NaOH和Ca(OH)2。请用化学方程式说明理由 ;
(3)调味用的食醋中含有醋酸(用HAc表示其组成),可以用来浸泡除去水垢(主要成分是碳酸钙和氢氧化镁),请写出有关反应的化学方程式 ;
(4)从含Cu2S的铜矿石中炼出铜的方法有多种:其中一种方法是:
①先将该矿石通空气高温煅烧,生成一种黑色固态氧化物和一种有刺激性气味的气态氧化物;
②将燃烧过的矿石上加适量的未经燃烧的铜矿石,混合均匀后隔绝空气再进行高温煅烧,结果得到金属铜和上述刺激性气味的气体。写出上述两步反应的化学方程式:
① ;② 。
(1)检验市场上销售的食盐中是否含有碘元素(元素符号为I) 的一种方法,是在酸性条件下,使食盐样品溶液跟一种试剂X反应(KIO3 +5X+6HCl═6KCl+3I2+3H2O)。这种试剂X是 ,要完成这种实验还需要的一种物质是 (填名称),它遇到 会变蓝。
(2)有一种浸液,其配方如下:NaOH 6g、NaCl 10g、Ca(OH)2 59g、茶叶5g、H2O 210mL,用该浸液浸泡鸭蛋可制无泥皮蛋。配制浸液时,是否可以用生石灰和纯碱代替NaOH和Ca(OH)2。请用化学方程式说明理由 ;
(3)调味用的食醋中含有醋酸(用HAc表示其组成),可以用来浸泡除去水垢(主要成分是碳酸钙和氢氧化镁),请写出有关反应的化学方程式 ;
(4)从含Cu2S的铜矿石中炼出铜的方法有多种:其中一种方法是:
①先将该矿石通空气高温煅烧,生成一种黑色固态氧化物和一种有刺激性气味的气态氧化物;
②将燃烧过的矿石上加适量的未经燃烧的铜矿石,混合均匀后隔绝空气再进行高温煅烧,结果得到金属铜和上述刺激性气味的气体。写出上述两步反应的化学方程式:
① ;② 。
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐3】一包白色粉末由Mg、MgO、Mg(OH)2和MgCO3中的一种或几种组成。小乐为了探究该固体粉末的成分,取了2.4g样品,并设计如图所示的实验装置及如下所示方案:
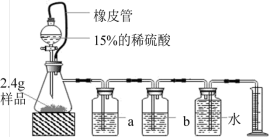
①检查装置气密性,加入药品并测量出b装置的质量为m1并连接仪器;
②打开分液漏斗活塞,将15%的稀硫酸缓缓注入锥形瓶中,使样品完全反应,测得量筒内共收集到112mL的水;
③拆下装置后,称量反应后b装置质量为m2;
④往锥形瓶内的溶液中注入足量氢氧化钠溶液,至沉淀完全,经过滤、洗涤和干燥后,称量沉淀质量;
(1)在步骤①中,b装置中加入的药品是_________ 溶液;
(2)此实验条件下,氢气密度为0.09g/L,则样品中Mg的质量为_________ g(保留2位小数);
(3)能否根据实验中无气泡产生这一现象,来判断样品完全反应_________ ;
(4)为确保样品完全反应请你估算一下15%的稀硫酸的质量为_________ 。

①检查装置气密性,加入药品并测量出b装置的质量为m1并连接仪器;
②打开分液漏斗活塞,将15%的稀硫酸缓缓注入锥形瓶中,使样品完全反应,测得量筒内共收集到112mL的水;
③拆下装置后,称量反应后b装置质量为m2;
④往锥形瓶内的溶液中注入足量氢氧化钠溶液,至沉淀完全,经过滤、洗涤和干燥后,称量沉淀质量;
(1)在步骤①中,b装置中加入的药品是
(2)此实验条件下,氢气密度为0.09g/L,则样品中Mg的质量为
(3)能否根据实验中无气泡产生这一现象,来判断样品完全反应
(4)为确保样品完全反应请你估算一下15%的稀硫酸的质量为
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】自然界的矿物中有一种重晶石矿的主要成分是BaSO4,它不溶于任何酸、碱和水,纯净的硫酸钡可供医疗等方面应用,某同学用重晶石和焦炭为原料,制取纯净硫酸钡,部分流程如下(设矿物中杂质不与焦炭反应,也不溶于水):
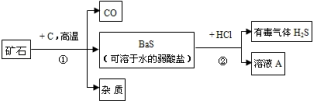
(1)步骤2中溶液A中溶质的化学式:_____________ 。
(2)步骤2产生有毒气体H2S,应加以改进,为使实验既不产生H2S又能获得纯净BaSO4,请你提出改进意见。_____________

(1)步骤2中溶液A中溶质的化学式:
(2)步骤2产生有毒气体H2S,应加以改进,为使实验既不产生H2S又能获得纯净BaSO4,请你提出改进意见。
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】现有A、B、C、D、E五种没有标签的无色溶液,分别是稀盐酸、碳酸钠溶液、澄清的石灰水、氢氧化钠溶液、无色酚酞溶液中的一种,为了鉴别它们进行如下实验,实验步骤及现象如下:
①先将A加入其他四种溶液中,结果只有C是无色的,其它均为红色;
②将B与剩下的两种溶液混合,B和D混合后呈现浑浊,B和E混合无现象。
根据现象回答下列问题:
(1)E物质是 ;
(2)利用现有试剂如何鉴别B和D ;
写出一个有关反应的化学方程式 。
①先将A加入其他四种溶液中,结果只有C是无色的,其它均为红色;
②将B与剩下的两种溶液混合,B和D混合后呈现浑浊,B和E混合无现象。
根据现象回答下列问题:
(1)E物质是 ;
(2)利用现有试剂如何鉴别B和D ;
写出一个有关反应的化学方程式 。
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐3】同学们利用如图所示的装置,对质量守恒定律进行了探究.实验结束后,老师另外提出了几个问题,请你一起参与思考.

(1)图甲装置内物质充分反应后,冷却至室温,气球仍胀大的是________ (选填“A”、“B”或“A和B”)
(2)若图乙装置内Na2CO3溶液的质量为5克,滴入试管的稀盐酸质量也是5克,装置内物质充分反应后,发现NaOH浓溶液质量增加0.22克,试管中滴入紫色石蕊试液变红.根据上述已知条件,通过分析可以确定的是________ (选填序号)
①原稀盐酸的溶质质量分数 ②原Na2CO3溶液的溶质质量分数
③原NaOH溶液的溶质质量分数 ④反应后试管中NaCl的溶质质量分数
(3)请你选择(2)所填的其中一项,通过计算确定其溶质质量分数是多少?________

(1)图甲装置内物质充分反应后,冷却至室温,气球仍胀大的是
(2)若图乙装置内Na2CO3溶液的质量为5克,滴入试管的稀盐酸质量也是5克,装置内物质充分反应后,发现NaOH浓溶液质量增加0.22克,试管中滴入紫色石蕊试液变红.根据上述已知条件,通过分析可以确定的是
①原稀盐酸的溶质质量分数 ②原Na2CO3溶液的溶质质量分数
③原NaOH溶液的溶质质量分数 ④反应后试管中NaCl的溶质质量分数
(3)请你选择(2)所填的其中一项,通过计算确定其溶质质量分数是多少?
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】某科学兴趣小组的同学为了测定某不纯氧化铁试样(其中的杂质不参与反应)中氧化铁的质量分数,设计了如下图的实验装置: 试回答下列问题:

(1)A发生装置的优点是 ;
(2)写出C中硬质玻管内发生的化学方程式 ;
(3)称10克不出纯氧化铁试样放入C中硬质玻管内,称得U形管和氯化钙干燥剂的质量为23.4克,按上述装置进行实验,经过充分反应后称得U形管和氯化钙干燥剂的质量为26.1克,则试样中氧化铁的质量分数为 ;

(1)A发生装置的优点是 ;
(2)写出C中硬质玻管内发生的化学方程式 ;
(3)称10克不出纯氧化铁试样放入C中硬质玻管内,称得U形管和氯化钙干燥剂的质量为23.4克,按上述装置进行实验,经过充分反应后称得U形管和氯化钙干燥剂的质量为26.1克,则试样中氧化铁的质量分数为 ;
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】家庭食用碱的主要成分是Na2CO3,为测定该食用碱中Na2CO3的质量分数,某同学进行了以下实验:取40g食用碱,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见表(假设该食用碱中不含难溶性杂质且杂质均不与CaCl2溶液反应产生沉淀):请分析表中数据回答并计算:
(1)m=________ 。
(2)实验一结束后的滤液中一定存在的阴离子有________ (用离子符号表示)。
(3)计算该食用碱中Na2CO3的质量分数及加入的CaCl2溶液的溶质质量分数。________
| 实验一 | 实验二 | 实验三 | 实验四 | |
| 食用碱的质量(g) | 10 | 10 | 10 | 10 |
| 加入CaCl2溶液的质量(g) | 20 | 40 | 60 | 80 |
| 生成沉淀的质量(g) | 3 | m | 8 | 8 |
(1)m=
(2)实验一结束后的滤液中一定存在的阴离子有
(3)计算该食用碱中Na2CO3的质量分数及加入的CaCl2溶液的溶质质量分数。
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐3】有铁粉和铜粉的均匀混合物,甲、乙、丙三位同学分别取该混合物与稀硫酸反应,所得数据如下表所示:
数据,回答下列问题:
(1)丙同学所得混合物中铜的质量是________。
(2)甲所得溶液中含有溶质的是________。
(3)根据实验数据分析,若取用金属混合物15g,加入120g稀硫酸中,充分反应后最终得到固体质量为________。
(4)计算丙同学所得溶液中溶质的质量分数。(写出计算过程,计算结果精确到0.1%)
| 甲 | 乙 | 丙 | |
| 取用金属混合物的质量/g | 10 | 10 | 20 |
| 取用稀硫酸的质量/g | 100 | 120 | 100 |
| 反应后过滤,得干燥固体的质量 | 4 | 4 | 13 |
数据,回答下列问题:
(1)丙同学所得混合物中铜的质量是________。
(2)甲所得溶液中含有溶质的是________。
(3)根据实验数据分析,若取用金属混合物15g,加入120g稀硫酸中,充分反应后最终得到固体质量为________。
(4)计算丙同学所得溶液中溶质的质量分数。(写出计算过程,计算结果精确到0.1%)
您最近一年使用:0次



