实验室有一份在空气中潮解变质的氢氧化钠样品,质量为3.0g某实验小组将这份样品完全溶解,配成100g溶液。然后缓慢滴入7.3%的稀盐酸,同时进行搅拌,使二氧化碳全部逸出。滴加过程中,多次测得溶液pH和溶液总质量,部分数据如下表所示:
请分析计算:
(1)第________ 次测量时,溶液中只有一种溶质。
(2)表中 m=________ 。
(3)样品中碳酸钠的质量分数_______ 。(计算结果精确到0.1%)
(4)3.0g样品中氢氧化钠固体的质量。_______
| 测量次数 | 第1次 | 第6次 | 第16次 | 第21次 | 第26次 |
| 滴加的盐酸总质量/g | 0 | 5 | 15 | 20 | 25 |
| 溶液总质量/g | 50 | 55 | m | 69.78 | 74.78 |
| 溶液 pH | 12.4 | 12.1 | 7.0 | 2.2 | 2.1 |
请分析计算:
(1)第
(2)表中 m=
(3)样品中碳酸钠的质量分数
(4)3.0g样品中氢氧化钠固体的质量。
更新时间:2019-10-26 14:22:36
|
相似题推荐
解答题
|
适中
(0.65)
【推荐1】工业上用电解NaCl溶液的方法来制取NaOH、Cl2和H2,反应的化学方程式为:2NaCl+2H2O 2NaOH+H2↑+Cl2↑。现取一定质量分数的NaCl溶液87.3g进行电解,当NaCl完全反应时,生成0.2gH2。
2NaOH+H2↑+Cl2↑。现取一定质量分数的NaCl溶液87.3g进行电解,当NaCl完全反应时,生成0.2gH2。
(1)当NaCl完全反应时,生成Cl2的质量为___________g,参加反应的NaCl的质量为___________g。
(2)当NaCl完全反应时,所得NaOH溶液中溶质的质量分数为多少?(假设生成的Cl2和H2全部逸出,要有计算过程)
 2NaOH+H2↑+Cl2↑。现取一定质量分数的NaCl溶液87.3g进行电解,当NaCl完全反应时,生成0.2gH2。
2NaOH+H2↑+Cl2↑。现取一定质量分数的NaCl溶液87.3g进行电解,当NaCl完全反应时,生成0.2gH2。(1)当NaCl完全反应时,生成Cl2的质量为___________g,参加反应的NaCl的质量为___________g。
(2)当NaCl完全反应时,所得NaOH溶液中溶质的质量分数为多少?(假设生成的Cl2和H2全部逸出,要有计算过程)
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】某化学兴趣小组为了测定铁铜合金中铁的质量分数,取出3g合金样品,将60g稀硫酸分6次加入样品中,充分反应后过滤、洗涤、干燥、称重。得到的实验数据如下:
(1)这六次实验中,第___________ 次加入稀硫酸时样品中的铁已经完全反应。
(2)表格中,
___________ 。
(3)计算稀硫酸溶液的质量分数___________ 。
| 稀硫酸用量 | 剩余固体质量 | 稀硫酸用量 | 剩余固体质量 |
第一次加入 |  | 第四次加入 | 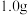 |
第二次加入 |  | 第五次加入 | 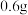 |
第三次加入 | 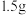 | 第六次加入 | 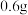 |
(1)这六次实验中,第
(2)表格中,

(3)计算稀硫酸溶液的质量分数
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】农技人员采用“测土配方”技术对一片果园进行了土壤检测,结果显示该果园需要补充一定量的氮元素和钾元素.

(1)氮是植物生长的重要元素,果园土壤中缺少氮元素,需要用氮肥来补充,下列属于氮肥的是(填序号)_____
①KCl; ②NH4NO3 ③ Ca3(PO4)2
(2)“测土配方”可以实现“缺什么、补什么”.小明同学想利用已有的知识点弄清上述氮肥的成分,他看到袋中化肥是白色晶体,用少量肥料跟熟石灰一起研磨,有浓烈的刺激性气味,初步判断是一种氮肥。请用化学方程式解释上述实验现象:_____________________________________
(3)某同学取丰收牌钾肥(如图甲)样品2.0g,溶于足量的水中,滴加过量氯化钡溶液,产生沉淀质量与所加氯化钡溶液质量的关系如图乙.试通过计算判断该钾肥中硫酸钾的质量分数是否符合产品外包装说明?(杂质不参加反应.)___________________________

(1)氮是植物生长的重要元素,果园土壤中缺少氮元素,需要用氮肥来补充,下列属于氮肥的是(填序号)
①KCl; ②NH4NO3 ③ Ca3(PO4)2
(2)“测土配方”可以实现“缺什么、补什么”.小明同学想利用已有的知识点弄清上述氮肥的成分,他看到袋中化肥是白色晶体,用少量肥料跟熟石灰一起研磨,有浓烈的刺激性气味,初步判断是一种氮肥。请用化学方程式解释上述实验现象:
(3)某同学取丰收牌钾肥(如图甲)样品2.0g,溶于足量的水中,滴加过量氯化钡溶液,产生沉淀质量与所加氯化钡溶液质量的关系如图乙.试通过计算判断该钾肥中硫酸钾的质量分数是否符合产品外包装说明?(杂质不参加反应.)
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】某化学小组同学按下图所示装置和表中所给试剂进行实验(图中铁架台等夹持仪器均已略去):

(1)在试管I中加入试剂后,塞紧橡皮塞,关闭止水夹a,打开止水夹b,试管Ⅱ中液面上升,溶液变浑浊。符合以上实验现象的试剂是 组,此时Ⅱ中发生反应化学方程式为________ _______。
(2)在试管I中加入试剂后,塞紧橡皮塞,立即打开止水夹a,关闭止水夹b,试管Ⅱ中有气泡冒出,溶液变浑浊。符合以上实验现象的试剂是 组。此时Ⅱ中发生反应的化学方程式为___________________________。

| 组别 | A组 | B组 | C组 | D组 |
| 试管I | Ca(OH)2 稀HCl | CaCO3 稀HCl | Zn 稀H2SO4 | Cu 稀H2SO4 |
| 试管Ⅱ | KNO3溶液 | Ca(OH)2溶液 | Ba(OH)2溶液 | Ba(OH)2溶液 |
(1)在试管I中加入试剂后,塞紧橡皮塞,关闭止水夹a,打开止水夹b,试管Ⅱ中液面上升,溶液变浑浊。符合以上实验现象的试剂是 组,此时Ⅱ中发生反应化学方程式为________ _______。
(2)在试管I中加入试剂后,塞紧橡皮塞,立即打开止水夹a,关闭止水夹b,试管Ⅱ中有气泡冒出,溶液变浑浊。符合以上实验现象的试剂是 组。此时Ⅱ中发生反应的化学方程式为___________________________。
您最近一年使用:0次
解答题
|
适中
(0.65)
名校
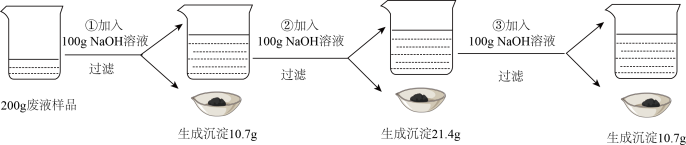
【推荐3】航母舰体需要定期除锈维护,为实现对除锈废液(溶质主要成分为HCl、FeCl3,其他杂质忽略) 的综合利用,需测定废液中 HCl的质量分数。取200g废液样品,依次加入100g溶质质量分数相同的 NaOH 溶液,过滤,称重,相关数据如图。
(1)第③次过滤后,滤液中溶质的成分为_________________ (用化学式表示)。
(2)所用 100gNaOH 溶液中溶质的质量。_____________
(3)废液样品中HCl的质量分数。_____________ (结果精确至0.1%)
(1)第③次过滤后,滤液中溶质的成分为
(2)所用 100gNaOH 溶液中溶质的质量。
(3)废液样品中HCl的质量分数。
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】AgNO3可用于电影胶片制作。现取含有NaNO3的AgNO3样品100g,在一定条件下让样品充分反应,只有AgNO3发生反应,得到固体69g,该过程中发生反应的化学方程式为: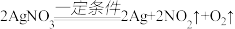 。试计算:
。试计算:
(1)AgNO3中N、O元素的质量比为____ 。
(2)分解产生的混合气体中O2的质量。____
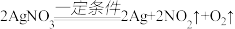 。试计算:
。试计算:(1)AgNO3中N、O元素的质量比为
(2)分解产生的混合气体中O2的质量。
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】小明同学将13.9g含杂质的的纯碱样品(碳酸钠与氯化钠的混合物)与90.5g稀盐酸相混合,充分反应,测得反应生成气体的质量(m)与反应时间(t)的数据如下表所示:
根据题目要求,回答下列问题:
(1)碳酸钠完全反应后,生成CO2的质量为________g。
(2)请画出反应是生成气体的质量(m)随时间(t)变化的曲线。
(3)求完全反应后所得溶液中溶质的质量分数。(Na2CO3+2HCl=2NaCl+CO2↑+H2O)。
反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
气体质量m/g | 0 | 0.88 | 1.76 | 2.64 | 3.52 | 4.4 | 4.4 |
根据题目要求,回答下列问题:
(1)碳酸钠完全反应后,生成CO2的质量为________g。
(2)请画出反应是生成气体的质量(m)随时间(t)变化的曲线。
(3)求完全反应后所得溶液中溶质的质量分数。(Na2CO3+2HCl=2NaCl+CO2↑+H2O)。
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐3】为测定锌铜合金中锌的含量,取该合金放入如图盛有稀硫酸的锥形瓶中,发生反应。多次实验后,取平均值所得数据如下表:

若不考虑干燥剂吸收空气中的水蒸气,计算:
(1)生成氢气的质量是________ 克。
(2)该合金中锌的质量分数为__________ 。
(3)装置中的干燥剂的作用是________ 。
(4)以下情形会导致样品中锌的质量分数测量结果偏高的原因可能有________ 。
A向锥形瓶中放入合金时,撒出了部分合金
B没有等装置中气体全部排尽就称量
C干燥剂部分失效
D干燥剂直接与空气接触

| 反应前 | 充分反应后装置及反应剩余物质质量 | |
| 装置和足量的稀硫酸质量 | 锌铜合金质量 | |
| 367.10g | 20.00g | 386.70g |
若不考虑干燥剂吸收空气中的水蒸气,计算:
(1)生成氢气的质量是
(2)该合金中锌的质量分数为
(3)装置中的干燥剂的作用是
(4)以下情形会导致样品中锌的质量分数测量结果偏高的原因可能有
A向锥形瓶中放入合金时,撒出了部分合金
B没有等装置中气体全部排尽就称量
C干燥剂部分失效
D干燥剂直接与空气接触
您最近一年使用:0次



