某公司生产出的纯碱产品中经检测只含有氯化钠杂质。为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品26.5g,加入盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液;反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示。
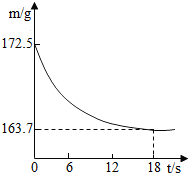
(1)生成CO2的质量为_______ ;
(2)求恰好完全反应后所得到不饱和NaCl溶液中溶质的质量分数。_______

(1)生成CO2的质量为
(2)求恰好完全反应后所得到不饱和NaCl溶液中溶质的质量分数。
更新时间:2019-10-14 16:02:11
|
相似题推荐
解答题
|
较难
(0.4)
【推荐1】某科学兴趣小组同学为测定大理石和盐酸反应后的废液成分,取50克该废液逐滴加入碳酸钠溶液,根据实验测定的数据绘出右图,其中纵坐标表示沉淀的质量,横坐标表示碳酸钠溶液的质量。请回答:
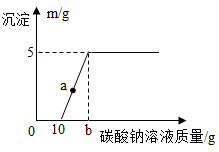
(1)分析图像可知,开始加入碳酸钠溶液至10克,没有产生沉淀的原因________
(2)如图在a点时溶液中的溶质的成分为________
(3)废液中氯化钙的质量分数为多少?________________

(1)分析图像可知,开始加入碳酸钠溶液至10克,没有产生沉淀的原因
(2)如图在a点时溶液中的溶质的成分为
(3)废液中氯化钙的质量分数为多少?
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】实验小组在实验室找到一瓶含有铜和铁的均匀混合物。为测定该混合物中铁的质量分数,分别取一定质量的混合物与稀硫酸进行反应,实验分四组,所得数据如下表所示:

请分析数据,回答下列问题:
(1)该混合物中铁的质量分数为多少_____ ?
(2)表中的W=________ (填数值);
(3)第1组实验中所得滤液中的溶质是________ (用化学式表示);
(4)计算第4组实验中所得溶液溶质的质量分数_____ 。(写出计算过程,结果精确到0.1%)

请分析数据,回答下列问题:
(1)该混合物中铁的质量分数为多少
(2)表中的W=
(3)第1组实验中所得滤液中的溶质是
(4)计算第4组实验中所得溶液溶质的质量分数
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐3】某同学在实验室进行有关浓硫酸的实验,观察瓶上的标签(如下表所示)。
(1)他从瓶中倒出100毫升用于配制成稀硫酸,这100毫升浓硫酸含溶质________ 克,他将这100毫升浓硫酸与500克水均匀混合,所得稀硫酸的质量分数是_____ 。(结果保留二位小数)
(2)若实验室要配制630g溶质质量分数28%的稀硫酸,则需要这瓶溶质质量分数为98%的浓硫酸多少毫升?_______ (结果保留二位小数)
(1)他从瓶中倒出100毫升用于配制成稀硫酸,这100毫升浓硫酸含溶质
| 浓硫酸(H2SO4) 500毫升 | |
| 浓度(质量分数) | 98% |
| 密度 | 1.84克/厘米-3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封贮藏 | |
(2)若实验室要配制630g溶质质量分数28%的稀硫酸,则需要这瓶溶质质量分数为98%的浓硫酸多少毫升?
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】固体铵盐A的成分可能是(NH4)2SO4、NH4HSO4或是两者的混合物。实验小组的同学取了数份不同质量的样品A,他们将不同质量的铵盐分别加入到500.0mLNaOH溶液中(含48.0gNaOH),水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用足量浓硫酸完全吸收,测定结果如下。
①求实验编号为Ⅱ的实验125.2g铵盐中各成分的质量。
②求a的值以及b的取值范围(b≠0)。
| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 铵盐的质量(g) | 62.6 | 125.2 | 250.4 | b |
| 浓硫酸增加的质量(g) | 13.6 | 13.6 | a | 0 |
②求a的值以及b的取值范围(b≠0)。
您最近一年使用:0次
解答题
|
较难
(0.4)
名校
【推荐2】现有含NaCl、Na2SO4、NaNO3的混合溶液,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、NO3-的相互分离.相应的实验过程可用下列流程图表示:
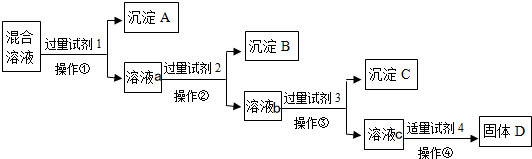
(1)写出上述实验过程中所用试剂、沉淀的化学式:试剂1:______ 沉淀C:__________
(2)写出溶液a中所含有的阳离子_________ ;
(3)恰当地控制试剂4的加入量的方法是__________________ .

(1)写出上述实验过程中所用试剂、沉淀的化学式:试剂1:
(2)写出溶液a中所含有的阳离子
(3)恰当地控制试剂4的加入量的方法是
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐3】现有HCl与CaCl2的混合溶液,为了分析混合溶液中HCl和CaCl2的质量分数,设计了如图实验方案:
实验数据:实验共记录了两组数据:第①组,气体吸收完全后,NaOH溶液质量增加4.4g;第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g。
根据实验设计及有关数据进行分析与计算:
(1)混合溶液中CaCl2的质量分数为多少?(写出计算过程)
(2)实验中混合溶液与Na2CO3溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为?(不考虑过滤中的损失。只写结果,保留小数点后一位)(Na23;Ca-40;Cl-35.5;O-16;H-1C-12)
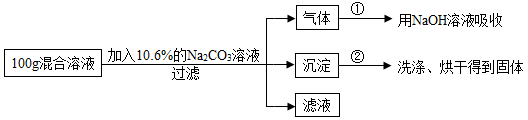
实验数据:实验共记录了两组数据:第①组,气体吸收完全后,NaOH溶液质量增加4.4g;第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g。
根据实验设计及有关数据进行分析与计算:
(1)混合溶液中CaCl2的质量分数为多少?(写出计算过程)
(2)实验中混合溶液与Na2CO3溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为?(不考虑过滤中的损失。只写结果,保留小数点后一位)(Na23;Ca-40;Cl-35.5;O-16;H-1C-12)

您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】用“盐酸—硫化钡法”生产 BaCl2 会放出有毒气体 H2S(其水溶液有酸性)可用 NaOH吸收 H2S 制取 Na2S 进行处理。下表为 H2S 回收工艺的各项生产成本:

(1)工业处理尾气需考虑经济效益和社会效益,根据上述资料分析,单从经济效益考虑这种处理 H2S 的方法是________ (选填“盈利”或“亏损”)的。
(2)若某化工厂每天要处理 10 吨 H2S,需消耗 NaOH 多少吨?(写出计算过程,结果保留1 位小数)________

(1)工业处理尾气需考虑经济效益和社会效益,根据上述资料分析,单从经济效益考虑这种处理 H2S 的方法是
(2)若某化工厂每天要处理 10 吨 H2S,需消耗 NaOH 多少吨?(写出计算过程,结果保留1 位小数)
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】利用下图的实验装置,测定某氧化铜试样中氧化铜的质量分数。根据实验装置回答问题:
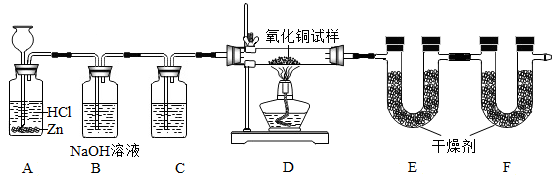
(1)装置B的作用是________ ,装置F的作用是________ 。
(2)装置C中盛放的试剂是_______ 。
(3)假设试样中的杂质不反应,且B、C、E装置吸收均完全。取20克试样,若实验前称得U型管E和其中的氯化钙质量为100.8克,充分反应后称得U型管E总质量为104.4克,则试样中氧化铜的质量分数为________ 。
(4)若取消F装置,那么测得的试样中氧化铜的质量分数比实际试样中氧化铜的质量分数________ (填偏大或偏小)。

(1)装置B的作用是
(2)装置C中盛放的试剂是
(3)假设试样中的杂质不反应,且B、C、E装置吸收均完全。取20克试样,若实验前称得U型管E和其中的氯化钙质量为100.8克,充分反应后称得U型管E总质量为104.4克,则试样中氧化铜的质量分数为
(4)若取消F装置,那么测得的试样中氧化铜的质量分数比实际试样中氧化铜的质量分数
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐3】大理石是含杂质的碳酸钙, 因具有美丽花纹而被广泛用于建筑物外墙、内壁的贴面和地面铺设。某同学想测出大理石样品中碳酸钙的含量, 进行了如下实验和分析。

(1)取一定量的大理石样品置于图甲的发生装置中,用分液漏斗向下滴加盐酸(方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑,杂质不参加反应) ,产生的二氧化碳气体用含有碱性物质的吸收装置充分吸收。分液漏斗中所加液体不选用硫酸,理由是________ 。
(2)反应前, 测得图甲中锥形瓶内物质的总质量和吸收装置的总质量都为 m 克。实验后, 根据实验数据绘制了图乙, 曲线 a 、b 分别表示锥形瓶内物质的总质量和吸收装置的总质量随反应时间变化的情况。请根据曲线 b 分析计算出大理石样品中碳酸钙的质量。____
(3)请综合分析曲线 a 、b , 计算出实验中所用盐酸的溶质质量分数。___

(1)取一定量的大理石样品置于图甲的发生装置中,用分液漏斗向下滴加盐酸(方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑,杂质不参加反应) ,产生的二氧化碳气体用含有碱性物质的吸收装置充分吸收。分液漏斗中所加液体不选用硫酸,理由是
(2)反应前, 测得图甲中锥形瓶内物质的总质量和吸收装置的总质量都为 m 克。实验后, 根据实验数据绘制了图乙, 曲线 a 、b 分别表示锥形瓶内物质的总质量和吸收装置的总质量随反应时间变化的情况。请根据曲线 b 分析计算出大理石样品中碳酸钙的质量。
(3)请综合分析曲线 a 、b , 计算出实验中所用盐酸的溶质质量分数。
您最近一年使用:0次



