下列框图中的物质均为初中化学常见的物质,其中A是建筑材料的主要成分,B属于氧化物,下图是它们之间的相互转化关系。请回答:
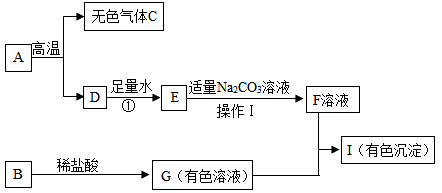
(1)得到F溶液的操作Ⅰ的名称为:________ 。
(2)若I是红褐色沉淀,请写出G+F→I的化学方程式:________ 。
(3)指出反应①的基本类型是________ 反应。

(1)得到F溶液的操作Ⅰ的名称为:
(2)若I是红褐色沉淀,请写出G+F→I的化学方程式:
(3)指出反应①的基本类型是
更新时间:2019/12/10 08:08:33
|
相似题推荐
解答题
|
适中
(0.65)
【推荐1】有一新闻报道:王先生家里的新房刚刚装修完,他便和妻子大扫除。当打扫到卫生间时,他便将“洁厕灵”和“漂白精”一起倒进了坐便器。然而刚放进去,一股刺激性气体便冒了出来,呛得他眼红流泪,嗓子发痛,呼吸困难,随后家人赶紧把他送到了医院。医院呼吸内科医生建议:在不了解各种洗涤剂和清洁剂的化学成分时,不要混合使用!下表是几种家用清洁剂的功能、有效成分。
据表回答下列问题:
(1)“洁厕灵”不能用于大理石清洁的理由______ (用化学方程式表示);
(2)在盛有少量“活氧彩漂”液体的试管中,加少量二氧化锰,反应的化学方程式为______ ;
(3)“洁厕灵”与“漂白精”不能混用。二者若混合易产生一种有毒气体,反应的化学方程式为:Ca(ClO)2+4HCl=CaCl2+2X+2H2O,则X的化学式为______ 。
| 清洁剂名称 | 洁厕灵 | 含氧漂白剂 | 漂白精 |
| 功能 | 有效清除污垢,除异味 | 漂洗衣物,使色彩更鲜艳 | 快速漂除衣物污渍 |
| 有效成分 | HCl | H2O2 | Ca(ClO)2 |
据表回答下列问题:
(1)“洁厕灵”不能用于大理石清洁的理由
(2)在盛有少量“活氧彩漂”液体的试管中,加少量二氧化锰,反应的化学方程式为
(3)“洁厕灵”与“漂白精”不能混用。二者若混合易产生一种有毒气体,反应的化学方程式为:Ca(ClO)2+4HCl=CaCl2+2X+2H2O,则X的化学式为
您最近一年使用:0次
解答题
|
适中
(0.65)
名校
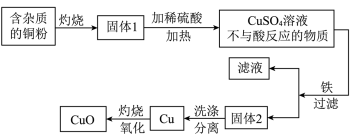
【推荐2】如图是用铜粉氧化法生产氧化铜的流程图。据图回答下列问题:
(1)铜粉灼烧后可能有氧化铜和氧化亚铜两种物质。氧化亚铜(Cu2O)中铜元素的化合价是______ 价。
(2)已知氧化亚铜和稀硫酸反应可生成硫酸铜和铜,假如固体1中只含有铜的氧化物,下列推理合理的是______ (填序号)。
①固体1中加入稀硫酸,若溶液呈蓝色,说明该固体中一定有氧化铜
②固体1中加入稀硫酸,若有红色沉淀物,说明该固体中一定有氧化亚铜
(3)将得到的1.6吨氧化铜全部转化为硫酸铜;可得硫酸铜多少吨?_________
(1)铜粉灼烧后可能有氧化铜和氧化亚铜两种物质。氧化亚铜(Cu2O)中铜元素的化合价是
(2)已知氧化亚铜和稀硫酸反应可生成硫酸铜和铜,假如固体1中只含有铜的氧化物,下列推理合理的是
①固体1中加入稀硫酸,若溶液呈蓝色,说明该固体中一定有氧化铜
②固体1中加入稀硫酸,若有红色沉淀物,说明该固体中一定有氧化亚铜
(3)将得到的1.6吨氧化铜全部转化为硫酸铜;可得硫酸铜多少吨?
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】某石化厂的一种石油产品中,残余硫酸质量分数为4.9%,工作人员用NaOH溶液来清洗这些残余硫酸。请计算:
(1)若要清洗100kg的这种石油产品,需要多少千克的NaOH?
(2)石化厂进行了技术改造,采用Ca(OH)2代替NaOH清洗这些残余硫酸。通过技术改造,每清洗处理100kg这种石油产品,可以节约多少经费?
NaOH和Ca (OH)2的市场价格
(1)若要清洗100kg的这种石油产品,需要多少千克的NaOH?
(2)石化厂进行了技术改造,采用Ca(OH)2代替NaOH清洗这些残余硫酸。通过技术改造,每清洗处理100kg这种石油产品,可以节约多少经费?
NaOH和Ca (OH)2的市场价格
名称 | Ca(OH)2 | NaOH |
价格(元/千克) | 6.00 | 24.00 |
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】农技人员采用“测土配方”技术对一片果园进行了土壤检测,结果显示该果园需要补充一定量的氮元素和钾元素.

(1)氮是植物生长的重要元素,果园土壤中缺少氮元素,需要用氮肥来补充,下列属于氮肥的是(填序号)_____
①KCl; ②NH4NO3 ③ Ca3(PO4)2
(2)“测土配方”可以实现“缺什么、补什么”.小明同学想利用已有的知识点弄清上述氮肥的成分,他看到袋中化肥是白色晶体,用少量肥料跟熟石灰一起研磨,有浓烈的刺激性气味,初步判断是一种氮肥。请用化学方程式解释上述实验现象:_____________________________________
(3)某同学取丰收牌钾肥(如图甲)样品2.0g,溶于足量的水中,滴加过量氯化钡溶液,产生沉淀质量与所加氯化钡溶液质量的关系如图乙.试通过计算判断该钾肥中硫酸钾的质量分数是否符合产品外包装说明?(杂质不参加反应.)___________________________

(1)氮是植物生长的重要元素,果园土壤中缺少氮元素,需要用氮肥来补充,下列属于氮肥的是(填序号)
①KCl; ②NH4NO3 ③ Ca3(PO4)2
(2)“测土配方”可以实现“缺什么、补什么”.小明同学想利用已有的知识点弄清上述氮肥的成分,他看到袋中化肥是白色晶体,用少量肥料跟熟石灰一起研磨,有浓烈的刺激性气味,初步判断是一种氮肥。请用化学方程式解释上述实验现象:
(3)某同学取丰收牌钾肥(如图甲)样品2.0g,溶于足量的水中,滴加过量氯化钡溶液,产生沉淀质量与所加氯化钡溶液质量的关系如图乙.试通过计算判断该钾肥中硫酸钾的质量分数是否符合产品外包装说明?(杂质不参加反应.)
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐3】宇宙飞船内,宇航员呼出的气体要通过盛有氢氧化锂的过滤网,以除去所含的二氧化碳,如下式所示:2LiOH(固)+CO2(气)=Li2CO3(固)+H2O(液)
(1)试计算5kg氢氧化锂所能吸收的二氧化碳的质量。
(2)通过计算解释为什么宇宙飞船选用氢氧化锂来吸收二氧化碳较用氢氧化钾为佳。
(3)神舟七号载人飞船于2008年9月25日21点10分左右从中国酒泉卫星发射中心载人航天发射场用长征二号F火箭发射升空。飞船于2008年9月28日17点40分左右成功着陆于中国内蒙古四子王旗主着陆场。神舟七号飞船载有三名宇航员分别为翟志刚、刘伯明和景海鹏。若每位宇航员每天所呼出的二氧化碳平均是502L,试计算在神舟七号宇宙飞船上至少应携带氢氧化锂多少千克?(在宇宙飞船内的温度和气压下,二氧化碳气体的密度位1.833g/L)。
(相对原子质量:L i—7 O—16 H—1 K—39 C—12)
(1)试计算5kg氢氧化锂所能吸收的二氧化碳的质量。
(2)通过计算解释为什么宇宙飞船选用氢氧化锂来吸收二氧化碳较用氢氧化钾为佳。
(3)神舟七号载人飞船于2008年9月25日21点10分左右从中国酒泉卫星发射中心载人航天发射场用长征二号F火箭发射升空。飞船于2008年9月28日17点40分左右成功着陆于中国内蒙古四子王旗主着陆场。神舟七号飞船载有三名宇航员分别为翟志刚、刘伯明和景海鹏。若每位宇航员每天所呼出的二氧化碳平均是502L,试计算在神舟七号宇宙飞船上至少应携带氢氧化锂多少千克?(在宇宙飞船内的温度和气压下,二氧化碳气体的密度位1.833g/L)。
(相对原子质量:L i—7 O—16 H—1 K—39 C—12)
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】某固体混合物由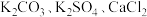 和
和 中的一种或几种组成。小王和小李同学准备通过实验确定该混合物的组成,实验记录如下:
中的一种或几种组成。小王和小李同学准备通过实验确定该混合物的组成,实验记录如下:
①取该样品溶于水,得到无色溶液;②取适量上述溶液加过量的 溶液,出现白色沉淀,过滤;③向步骤②所得沉淀中加入过量的稀
溶液,出现白色沉淀,过滤;③向步骤②所得沉淀中加入过量的稀 ,沉淀部分消失并产生气泡;④取步骤②后的滤液加入
,沉淀部分消失并产生气泡;④取步骤②后的滤液加入 溶液生成白色沉淀,再加入稀
溶液生成白色沉淀,再加入稀 ,振荡,沉淀不消失。
,振荡,沉淀不消失。
两位同学由此推断:该固体混合物中一定含有_____ ;写出步骤③中白色沉淀部分消失的反应方程式_____ 。但是上述实验方案还是不能确定一个物质是否存在,于是小王和小李又经过讨论得出:只需改动上述某一步骤中的一个试剂,就能确定该物质是否存在。请你写出他们想要改动的那一步实验方案:_____ 。
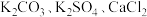 和
和 中的一种或几种组成。小王和小李同学准备通过实验确定该混合物的组成,实验记录如下:
中的一种或几种组成。小王和小李同学准备通过实验确定该混合物的组成,实验记录如下:①取该样品溶于水,得到无色溶液;②取适量上述溶液加过量的
 溶液,出现白色沉淀,过滤;③向步骤②所得沉淀中加入过量的稀
溶液,出现白色沉淀,过滤;③向步骤②所得沉淀中加入过量的稀 ,沉淀部分消失并产生气泡;④取步骤②后的滤液加入
,沉淀部分消失并产生气泡;④取步骤②后的滤液加入 溶液生成白色沉淀,再加入稀
溶液生成白色沉淀,再加入稀 ,振荡,沉淀不消失。
,振荡,沉淀不消失。两位同学由此推断:该固体混合物中一定含有
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】某白色固体甲的主要成分为NaCl,可能含有MgCl2、BaCl2和NaOH中的一种或几种杂质,为检验白色固体甲的成分并除去其中杂质,进行如下实验:
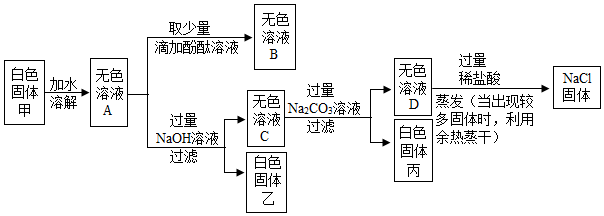
(1)写出生成白色固体丙的化学方程式:________________ 。
(2)向无色溶液D中加入过量稀盐酸的目的是______________ 。
(3)分析上述实验可知,白色固体甲中一定没有的物质是______________ 。
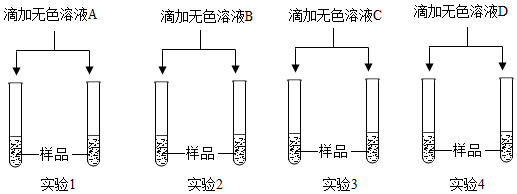
(4)若用上述实验中的A、B、C、D四种溶液鉴别稀H2SO4和NaOH溶液,分别取样后,按如图所示操作进行实验,就能达到鉴别目的的是实验____________ 。

(1)写出生成白色固体丙的化学方程式:
(2)向无色溶液D中加入过量稀盐酸的目的是
(3)分析上述实验可知,白色固体甲中一定没有的物质是
(4)若用上述实验中的A、B、C、D四种溶液鉴别稀H2SO4和NaOH溶液,分别取样后,按如图所示操作进行实验,就能达到鉴别目的的是实验

您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐3】听说墨鱼骨能治疗胃酸过多,好学的小科和小妍想探个究竟。查阅资料,墨鱼骨含碳酸钙80%~85%以上,还含有多种氨基酸。墨鱼骨能治疗胃酸过多的原因是:________________ (用化学方程式表示)。为了测定墨鱼骨中碳酸钙的含量,他们先将墨鱼骨洗净晒干,并按各自设计实验方法进行研究。
(1)小科称取10克洗净晒干的墨鱼骨,高温灼烧至质量不变,冷却后称得剩余固体质量为5.4克。处理如下: CO2 质量 = 10克 - 5.4克 = 4.6克,设碳酸钙质量为M
CaCO3 ═ CO2↑ + CaO
100 44
M 4.6克
100/M=44/4.6克 所以M = 10.5克
(2)小研用如图所示的实验装置进行实验,其中浓硫酸的作用是______ 。
(3)小妍将30mL稀盐酸分3次加入到3克样品中,每次加入盐酸后充分反应,待量筒内的水的体积不再变化时,读出水的体积,结果见下表。已知本实验条件下CO2 的密度为2.0克/升,求:该墨鱼骨粉样品中CaCO3的质量分数。_______
(1)小科称取10克洗净晒干的墨鱼骨,高温灼烧至质量不变,冷却后称得剩余固体质量为5.4克。处理如下: CO2 质量 = 10克 - 5.4克 = 4.6克,设碳酸钙质量为M
CaCO3 ═ CO2↑ + CaO
100 44
M 4.6克
100/M=44/4.6克 所以M = 10.5克
CaCO3% =10.5克/10克×100%=105%
小科的计算结果与事实不符,产生错误的原因是:
(2)小研用如图所示的实验装置进行实验,其中浓硫酸的作用是
(3)小妍将30mL稀盐酸分3次加入到3克样品中,每次加入盐酸后充分反应,待量筒内的水的体积不再变化时,读出水的体积,结果见下表。已知本实验条件下CO2 的密度为2.0克/升,求:该墨鱼骨粉样品中CaCO3的质量分数。
| 第一次 | 第二次 | 第三次 | |
| 加入稀盐酸的体积(毫升) | 10 | 10 | 10 |
| 进入量筒内水的体积(毫升) | 220 | 220 | 110 |
您最近一年使用:0次




