在完成实验“二氧化碳的制取”后,废液桶中倾倒了含有较多盐酸的混合溶液。为避免酸液污染环境,化学兴趣小组做了如下实验:取废液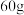 ,向其中加入溶质质量分数为21.2%的碳酸钠溶液。所得溶液
,向其中加入溶质质量分数为21.2%的碳酸钠溶液。所得溶液 与加入的碳酸钠溶液的质量关系如右图所示:(不考虑
与加入的碳酸钠溶液的质量关系如右图所示:(不考虑 溶于水对溶液酸碱性的影响)
溶于水对溶液酸碱性的影响)
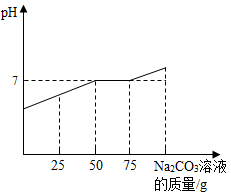
(1)通过右图可知,当碳酸钠溶液质量加到_____  时,废液中的盐酸恰好处理完。
时,废液中的盐酸恰好处理完。
(2)计算废液中氯化钙的质量分数_____ 。
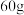 ,向其中加入溶质质量分数为21.2%的碳酸钠溶液。所得溶液
,向其中加入溶质质量分数为21.2%的碳酸钠溶液。所得溶液 与加入的碳酸钠溶液的质量关系如右图所示:(不考虑
与加入的碳酸钠溶液的质量关系如右图所示:(不考虑 溶于水对溶液酸碱性的影响)
溶于水对溶液酸碱性的影响)
(1)通过右图可知,当碳酸钠溶液质量加到
 时,废液中的盐酸恰好处理完。
时,废液中的盐酸恰好处理完。(2)计算废液中氯化钙的质量分数
20-21九年级上·浙江·期末 查看更多[1]
(已下线)【新东方】【初中科学2438】初三上
更新时间:2020-03-04 22:49:28
|
相似题推荐
解答题
|
较难
(0.4)
名校
【推荐1】有部分氧化的镁样品6.4克与200克稀硫酸恰好完全反应,反应后所得溶液质量为206.2克。
(1)6.4克样品中镁元素的质量是多少?_______
(2)所用稀硫酸溶液溶质质量分数是多少?____
(1)6.4克样品中镁元素的质量是多少?
(2)所用稀硫酸溶液溶质质量分数是多少?
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】向实验室制取 后的废液中逐滴加入溶质质量分数为10.0%的
后的废液中逐滴加入溶质质量分数为10.0%的 溶液,反应过程中加入的
溶液,反应过程中加入的 溶液的质量与产生沉淀或气体的质量关系如图所示:
溶液的质量与产生沉淀或气体的质量关系如图所示:

(1)图中的Oa段表示生成________ 的过程(填“气体”或“沉淀”);
(2)该废液中存在的溶质有________ ;
(3)x值为多少?________ (请列式计算)
 后的废液中逐滴加入溶质质量分数为10.0%的
后的废液中逐滴加入溶质质量分数为10.0%的 溶液,反应过程中加入的
溶液,反应过程中加入的 溶液的质量与产生沉淀或气体的质量关系如图所示:
溶液的质量与产生沉淀或气体的质量关系如图所示:
(1)图中的Oa段表示生成
(2)该废液中存在的溶质有
(3)x值为多少?
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%。为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0 g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应。实验数据记录如下:

请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是 g。
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)计算盐酸的质量分数,并确定碳酸钠完全反应时消耗稀盐酸的质量,根据实验数据,在右边的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线。
| 所加盐酸的质量/g | 25 | 50 | 75 | 100 |
| 烧杯及所盛物质总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |

请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是 g。
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)计算盐酸的质量分数,并确定碳酸钠完全反应时消耗稀盐酸的质量,根据实验数据,在右边的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线。
您最近一年使用:0次
解答题
|
较难
(0.4)
名校
【推荐2】现有盐酸与氯化钙的混合溶液,为分析它们的质量分数,设计如下实验方案:
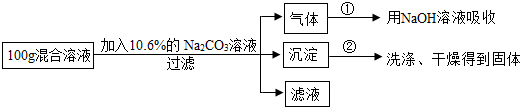
充分反应后,实验记录了两组数据:第①组NaOH溶液质量增加4.4g;第②组沉淀经过滤、洗涤、干燥后称得固体质量10g。根据实验设计及有关数据进行分析与计算:
(1)混合溶液中HCl的质量分数为___ (写出计算过程)。
(2)请你画出该实验过程中加入Na2CO3溶液的质量与产生沉淀的质量的关系图___ (注意标出数值)。

充分反应后,实验记录了两组数据:第①组NaOH溶液质量增加4.4g;第②组沉淀经过滤、洗涤、干燥后称得固体质量10g。根据实验设计及有关数据进行分析与计算:
(1)混合溶液中HCl的质量分数为
(2)请你画出该实验过程中加入Na2CO3溶液的质量与产生沉淀的质量的关系图
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】某兴趣小组在实验室发现一瓶敞口久置的氢氧化钠和一瓶未标浓度的稀盐酸,为测定氢氧化钠的变质情况和稀盐酸的浓度,他们取9.3g变质的氢氧化钠样品于锥形瓶中,加入50g水,充分溶解,再向锥形瓶中滴加未知浓度的稀盐酸,实验测得加入稀盐酸的质量与锥形瓶中物质的质量关系如图所示。求:

(1)9.3g样品中碳酸钠的质量;______ 。
(2)未知浓度的稀盐酸的溶质质量分数;______ 。
(3)加入50g稀盐酸时,溶液中溶质的质量分数。______ 。

(1)9.3g样品中碳酸钠的质量;
(2)未知浓度的稀盐酸的溶质质量分数;
(3)加入50g稀盐酸时,溶液中溶质的质量分数。
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】烧杯中装有硫酸和硫酸铜的混合溶液100克,小明将200克10%的 溶液分5次加入,得到沉淀的质量记录如表:
溶液分5次加入,得到沉淀的质量记录如表:
(1)第四次加入 溶液40克后,经充分反应后,这时烧杯中混合溶液的溶质是
溶液40克后,经充分反应后,这时烧杯中混合溶液的溶质是___________ 。
(2)求原混合溶液中硫酸铜的质量,写出计算过程___________ 。
(3)在下面坐标图中画出生成沉淀的质量和加入 溶液质量的关系图。
溶液质量的关系图。___________
 溶液分5次加入,得到沉淀的质量记录如表:
溶液分5次加入,得到沉淀的质量记录如表:加入 溶液的质量/g 溶液的质量/g | 40.0 | 80.0 | 120.0 | 160.0 | 200.0 |
| 生产沉淀的总质量/g | 0.0 | 2.45 | 7.35 | 9.8 | 9.8 |
(1)第四次加入
 溶液40克后,经充分反应后,这时烧杯中混合溶液的溶质是
溶液40克后,经充分反应后,这时烧杯中混合溶液的溶质是(2)求原混合溶液中硫酸铜的质量,写出计算过程
(3)在下面坐标图中画出生成沉淀的质量和加入
 溶液质量的关系图。
溶液质量的关系图。
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐3】用已知溶质质量分数的溶液可以测定未知溶液的溶质质量分数。实验室有一瓶标签模糊的稀盐酸,某同学为了测定其溶质质量分数,进行了如下实验:
①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴紫色石蕊试液(质量忽略不计),重新称量;
②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由红色恰好变为紫色时,停止滴加,再次称量。
数据如下表:
(1)若要配制500克16%的氢氧化钠溶液,需要氢氧化钠固体________ 克。
(2)本次实验中,实际消耗的氢氧化钠溶液质量为________ 克。
(3)该瓶稀盐酸的溶质质量分数为________ 。
(4)另有同学做了同样的实验,却得到了不同的结果。于是用精密pH试纸测得反应后锥形瓶内溶液的pH为8.2,则他测出的盐酸溶质质量分数________ (选填“偏大”或“偏小”)。
①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴紫色石蕊试液(质量忽略不计),重新称量;
②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由红色恰好变为紫色时,停止滴加,再次称量。
数据如下表:
锥形瓶 | 锥形瓶+稀盐酸 | 锥形瓶+反应后溶液 | |
质量(克) | 35.5 | 55.5 | 80.5 |
(1)若要配制500克16%的氢氧化钠溶液,需要氢氧化钠固体
(2)本次实验中,实际消耗的氢氧化钠溶液质量为
(3)该瓶稀盐酸的溶质质量分数为
(4)另有同学做了同样的实验,却得到了不同的结果。于是用精密pH试纸测得反应后锥形瓶内溶液的pH为8.2,则他测出的盐酸溶质质量分数
您最近一年使用:0次




