江苏省徐州市2022-2023学年九年级上学期第二次创新体验竞赛模拟化学试题
江苏
九年级
竞赛
2022-12-14
543次
整体难度:
适中
考查范围:
物质构成的奥秘、身边的化学物质、物质的化学变化、化学与社会发展、化学实验
江苏省徐州市2022-2023学年九年级上学期第二次创新体验竞赛模拟化学试题
江苏
九年级
竞赛
2022-12-14
543次
整体难度:
适中
考查范围:
物质构成的奥秘、身边的化学物质、物质的化学变化、化学与社会发展、化学实验
一、选择题 添加题型下试题
选择题-单选题
|
较难(0.4)
解题方法
1. 如下图是物质的分类及部分转化关系图,有关说法正确的是


| A.用自来水制取蒸馏水属于转化a | B.转化c可能是物理变化 |
| C.转化c中一定有元素的化合价发生改变 | D.转化b一定是化学变化 |
【知识点】 纯净物和混合物的判断解读 单质和化合物的判断解读 水的净化方法
您最近一年使用:0次
2018-01-29更新
|
592次组卷
|
7卷引用:南京市鼓楼区2017-2018学年度第一学期初三化学期末试卷
选择题-单选题
|
适中(0.65)
解题方法
2. “证据推理与模型认知”是化学学科核心素养的重要组成部分,以下说法正确的是
| A.某物质在O2中燃烧生成CO2和H2O,则该物质中一定含有碳、氢元素 |
| B.阴离子是带负电的微粒,所以带负电的粒子都是阴离子 |
| C.燃烧都伴随有发光放热现象,所以有发光放热现象的一定是燃烧 |
| D.同种元素的粒子质子数相同,则含有相同质子数的粒子一定属于同种元素 |
您最近一年使用:0次
2022-12-13更新
|
181次组卷
|
2卷引用:江苏省徐州市2022-2023学年九年级上学期第二次创新体验竞赛模拟化学试题
选择题-单选题
|
较难(0.4)
名校
解题方法
3. 植被丰富的公园中有丰富的负氧离子,空气中氧分子得到电子就能形成负氧离子( )。下列关于
)。下列关于 与O2的说法,错误的是
与O2的说法,错误的是
 )。下列关于
)。下列关于 与O2的说法,错误的是
与O2的说法,错误的是A. 与O2的化学性质不同 与O2的化学性质不同 |
B. 与O2的电子总数不同 与O2的电子总数不同 |
C. 与O2的质子数不同 与O2的质子数不同 |
D. 与O2的相对原子质量之和相同 与O2的相对原子质量之和相同 |
您最近一年使用:0次
2021-01-21更新
|
2088次组卷
|
14卷引用:云南民族大学附属中学2017-2018学年八年级上学期期末考试化学试题
云南民族大学附属中学2017-2018学年八年级上学期期末考试化学试题内蒙古呼和浩特市赛罕区2019届九年级第一学期期末调研考试化学试题广东省深圳市龙岗区百合外国语学校2020-2021学年九年级上学期12月月考化学试题江西省吉安市泰和县黄冈学校2021-2022学年九年级上学期期中化学试题四川省成都市初中化学创新能力培优竞赛题(二)安徽省合肥市第五十中学2022-2023学年九年级上学期教学质量检测化学试题3.2原子的结构基础过关练习—2022-2023学年九年级化学人教版上册江苏省徐州市2022-2023学年九年级上学期第二次创新体验竞赛模拟化学试题重庆市酉阳县四校2022-2023学年九年级上学期阶段性测试化学试题湖南省郴州市永兴县树德初级中学2022-2023学年九年级下学期学科知识竞赛初试化学试题湖南省衡阳市衡阳县五校联考2023-2024学年九年级上学期第三次月考化学试题(已下线)专题09 构成物质的微粒 元素(测试)-2024年中考化学一轮复习讲练测(全国通用)(已下线)专题09 构成物质的微粒 元素(练习)-2024年中考化学一轮复习讲练测(全国通用)2024年江苏省盐城市东台市中考一模化学试卷
选择题-单选题
|
适中(0.65)
解题方法
4. 在明代宋应星所著的《天工开物》中,有关火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石熔化成团。”(注:炉甘石的主要成分是碳酸锌)火法炼锌主要发生的化学反应是

 ,下列说法正确的是
,下列说法正确的是


 ,下列说法正确的是
,下列说法正确的是| A.X的化学式是CO2 | B.“逐层用煤炭饼垫盛”是为了燃烧提供高温 |
| C.反应前后固体的质量不变 | D.“罐中炉甘石熔化成团”,团的主要成分是锌 |
您最近一年使用:0次
2022-12-13更新
|
208次组卷
|
2卷引用:江苏省徐州市2022-2023学年九年级上学期第二次创新体验竞赛模拟化学试题
选择题-单选题
|
适中(0.65)
名校
解题方法
5. 某兴趣小组用如图所示装置测定本地石灰石中碳酸钙的质量分数,下列说法错误的是


| A.检查装置的气密性时,向上移动c管,观察b、c管中是否有稳定的液面差 |
| B.读取b管中的气体体积时,要移动c管,使b、c管中的液面保持同一高度 |
| C.a导管的作用是防止实验测定的结果偏小 |
| D.b管中油的作用是防止实验测定的结果偏小 |
【知识点】 二氧化碳物理性质及实验解读 气密性检测解读
您最近一年使用:0次
2022-01-17更新
|
639次组卷
|
7卷引用:福建省三明市2021-2022学年九年级上学期期末化学试题
福建省三明市2021-2022学年九年级上学期期末化学试题2022年广东省深圳市中考一模化学试题四川省成都市初中化学创新能力培优竞赛题(五)江苏省徐州市2022-2023学年九年级上学期第二次创新体验竞赛模拟化学试题(已下线)第03讲 二氧化碳-备战2023年中考化学一轮复习考点帮(广东专用)(已下线)金榜卷01-2023年中考化学考前一模名师押题金榜卷(深圳专用)2024年初中化学模拟试题00
选择题-单选题
|
较难(0.4)
6. 将CO和铁的氧化物FexOy置于密闭容器中,一定条件下充分反应至完全,反应过程中容器内部分物质的质量变化如图所示。下列说法正确的是

| A.m的值为12.6 | B.铁的氧化物中x:y=3:4 |
| C.参加反应的铁的氧化物的质量为16g | D.当CO2质量为4.4g时,容器内CO质量为14g |
您最近一年使用:0次
2021-06-20更新
|
2055次组卷
|
22卷引用:江苏省盐城市2021年中考化学试题
江苏省盐城市2021年中考化学试题(已下线)专题19 坐标图像题-2021年中考化学真题分项汇编(全国通用)(第01期)(已下线)考点09-质量守恒定律与化学方程式、方程式的配平-备战2022年中考化学一轮复习考点帮(上海专用)江苏省常州市2021-2022学年九年级上学期末模拟化学试题B(已下线)2022江苏中考风向标-质量守恒定律(已下线)2022江苏中考风向标-化学式、化学方程式分析2022年3月江苏省无锡市梁溪区无锡外国语学校中考一模化学试题2022年广西南宁地区中考三模化学试题四川省成都市初中化学创新能力培优竞赛题(七)(已下线)2023年中考风向标-江苏-图形、图像与流程分析江苏省苏州市常熟市实验中学2022-2023学年九年级上学期12月月考模拟化学试题江苏省徐州市2022-2023学年九年级上学期第二次创新体验竞赛模拟化学试题(已下线)考点13 质量守恒定律与化学方程式-备战2023年中考化学一轮复习考点帮 (人教版)(已下线)重难点11 计算题-2023年中考化学【热点·重点·难点】专练(上海专用)(已下线)黄金卷01-【赢在中考·黄金8卷】备战2023年中考化学全真模拟卷(无锡专用)2023年福建省龙岩市永定区九年级学生科学素养竞赛化学试题福建省泉州市南安市柳城中学2022-2023学年九年级下学期期中化学试题2023年湖北省武汉市江夏区中考三模化学试题(已下线)专题2.3 化学变化中的质量守恒(九大题型)-2023-2024学年九年级化学第一学期同步举一反三系列(沪教版·上海)湖南省衡阳市衡阳县五校联考2023-2024学年九年级上学期第三次月考化学试题(已下线)专题05? 质量守恒定律的应用(七大题型)-2024年中考化学二轮热点题型归纳与变式演练(江苏通用)(已下线)专题13 坐标图像题(七大题型)-2024年中考化学二轮热点题型归纳与变式演练(江苏通用)
选择题-单选题
|
适中(0.65)
解题方法
7. 某物质在点燃的条件下发生反应,甲、乙、丙、丁表示所有的反应物和生成物,它们的微观示意图和反应前后的质量如下表所示。
下列说法不正确的是( )
| 物质序号 | 甲 | 乙 | 丙 | 丁 |  |
| 微观示意图 |  |  | ? |  | |
| 反应前质量/g | 68 | 100 | 1 | 0 | |
| 反应后质量/g | 0 | 4 | 待测 | 128 |
| A.根据质量守恒,推测反应后丙物质的质量为37g |
| B.根据元素守恒,推测丙物质中一定含有氢元素 |
| C.根据原子守恒,甲和乙的化学计量数之比为1:1 |
| D.根据表中信息,参加反应的乙和反应生成的丁的质量比为3:4 |
【知识点】 有关质量守恒定律的计算解读 用质量守恒定律确定物质组成解读
您最近一年使用:0次
2021-04-23更新
|
282次组卷
|
2卷引用:2021年“金钥匙”科技竞赛初三学生CESL活动决赛化学试题
二、填空与简答 添加题型下试题
填空与简答-填空题
|
适中(0.65)
8. 2019年12月16日,在我国西昌卫星发射中心,以“一箭双星”方式成功将第52、53颗北斗导航卫星送上了太空。随着这两颗卫星的升空,我国北斗三号全球系统核心星座部署完成。
(1)“长征三号乙”火箭发动机在焊接时需要使用氩弧焊。氩弧焊(如图)是在氩气保护下,通过在钨电极与焊件间产生的高压电弧放热,熔化焊丝或焊件的一种焊接技术。

①金属钨作电极是利用了金属钨的导电性和____ ;用氩气作保护气,是因为氩气的化学性质____ 。
②如果在没有保护气的情况下焊接金属,可能导致焊接不牢,原因是_______ 。
(2)“长征三号乙”的第一、二级火箭用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)做推进剂,该反应的化学方程式为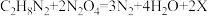 ,则X的化学式是
,则X的化学式是_______ 。
(3)“长征三号乙”的第三级火箭采用液氢、液氧做推进剂。实验室可通过电解水得到氢气和氧气,氢气在与直流电源_______ 极相连的电极上产生。氢能是未来最理想的能源,但目前应用并不广泛的原因是_______ (答一条即可)。
(4)北斗卫星的光伏发电板的主要构成材料是硅,单质硅由石英固体(SiO2)和碳在高温下反应制得,同时产生一种可燃性气体,该反应的化学方程式是_______ 。
(1)“长征三号乙”火箭发动机在焊接时需要使用氩弧焊。氩弧焊(如图)是在氩气保护下,通过在钨电极与焊件间产生的高压电弧放热,熔化焊丝或焊件的一种焊接技术。

①金属钨作电极是利用了金属钨的导电性和
②如果在没有保护气的情况下焊接金属,可能导致焊接不牢,原因是
(2)“长征三号乙”的第一、二级火箭用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)做推进剂,该反应的化学方程式为
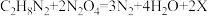 ,则X的化学式是
,则X的化学式是(3)“长征三号乙”的第三级火箭采用液氢、液氧做推进剂。实验室可通过电解水得到氢气和氧气,氢气在与直流电源
(4)北斗卫星的光伏发电板的主要构成材料是硅,单质硅由石英固体(SiO2)和碳在高温下反应制得,同时产生一种可燃性气体,该反应的化学方程式是
您最近一年使用:0次
填空与简答-流程题
|
较难(0.4)
解题方法
9. MnO2在工业生产中有广泛应用。制备MnO2是一项有意义的工作,某研究性学习小组对此展开了系列研究。
(1)用高锰酸钾制备。
已知:3K2MnO4+2H2SO4=2KMnO4+MnO2↓+2K2SO4+2H2O;KMnO4易溶于水。
实验室加热高锰酸钾制氧气,将反应后的固体剩余物用稀硫酸浸取一段时间后过滤、洗涤、烘干即得MnO2,用稀硫酸而不用水浸取的原因是___________ 。
(2)用硫酸锰制备。
电解MnSO4溶液可制得活性MnO2,同时生成氢气和硫酸,该反应的化学方程式为___________ 。
(3)用碳酸锰制备

①控制一定的温度,焙烧MnCO3,制备MnO2的装置如图-1。实验中观察到澄清石灰水变浑浊。焙烧MnCO3,制备MnO2的化学方程式为___________ 。
②MnCO3,在空气中加热易转化为锰的不同氧化物,残留固体质量随温度的变化如图-2所示。图中A、B、C点对应固体的成分的化学式依次为___________
(1)用高锰酸钾制备。
已知:3K2MnO4+2H2SO4=2KMnO4+MnO2↓+2K2SO4+2H2O;KMnO4易溶于水。
实验室加热高锰酸钾制氧气,将反应后的固体剩余物用稀硫酸浸取一段时间后过滤、洗涤、烘干即得MnO2,用稀硫酸而不用水浸取的原因是
(2)用硫酸锰制备。
电解MnSO4溶液可制得活性MnO2,同时生成氢气和硫酸,该反应的化学方程式为
(3)用碳酸锰制备

①控制一定的温度,焙烧MnCO3,制备MnO2的装置如图-1。实验中观察到澄清石灰水变浑浊。焙烧MnCO3,制备MnO2的化学方程式为
②MnCO3,在空气中加热易转化为锰的不同氧化物,残留固体质量随温度的变化如图-2所示。图中A、B、C点对应固体的成分的化学式依次为
您最近一年使用:0次
2022-04-09更新
|
437次组卷
|
3卷引用:2022年江苏省“金钥匙”科技竞赛(初三学生CESL活动)初赛化学试题
三、实验题 添加题型下试题
实验题
|
较难(0.4)
解题方法
10. 某化学兴趣小组同学探究环境湿度对过氧化钠(Na2O2)与CO2反应的影响。
【猜想与假设】猜想1:Na2O2与CO2在湿度较小的条件下不反应,只在湿度较大的条件下反应。猜想2:Na2O2与CO2在湿度较小和湿度较大的条件下均能反应。
【查阅资料】①常温下,过氧化钠是淡黄色粉末。②过氧化钠能与盐酸反应。③二氧化碳不溶于饱和碳酸氢钠溶液。④ppm是含量的一种表示方法。
【实验探究】(1)用图1装置制取并收集较潮湿的二氧化碳气体。其中饱和碳酸氢钠溶液的作用是______ 。

(2)如图2,在三颈烧瓶中分别插入湿度传感器、二氧化碳传感器、带铁丝的胶塞。
(3)待CO2传感器显示CO2读数稳定后,用铁丝戳破装有Na2O2的塑料袋,使Na2O2粉末与潮湿的CO2充分接触,打开数据采集器,得到图3、图4。

该实验可得出的结论是______ 。
(4)用图5装置制取并收集较干燥的二氧化碳气体,其中固体干燥剂的作用是______ 。

(5)装置同图2。待CO2传感器显示CO2读数稳定后,用铁丝戳破装有Na2O2的塑料袋,使过氧化钠粉末与较干燥的CO2充分接触,打开数据采集器,得到图6、图7。

【结论与反思】
(1)小组同学通过上述实验得出猜想______ (填“1”或“2”)是正确的。
(2)分析图3中相对湿度变化的原因是______ 。
【猜想与假设】猜想1:Na2O2与CO2在湿度较小的条件下不反应,只在湿度较大的条件下反应。猜想2:Na2O2与CO2在湿度较小和湿度较大的条件下均能反应。
【查阅资料】①常温下,过氧化钠是淡黄色粉末。②过氧化钠能与盐酸反应。③二氧化碳不溶于饱和碳酸氢钠溶液。④ppm是含量的一种表示方法。
【实验探究】(1)用图1装置制取并收集较潮湿的二氧化碳气体。其中饱和碳酸氢钠溶液的作用是

(2)如图2,在三颈烧瓶中分别插入湿度传感器、二氧化碳传感器、带铁丝的胶塞。
(3)待CO2传感器显示CO2读数稳定后,用铁丝戳破装有Na2O2的塑料袋,使Na2O2粉末与潮湿的CO2充分接触,打开数据采集器,得到图3、图4。

该实验可得出的结论是
(4)用图5装置制取并收集较干燥的二氧化碳气体,其中固体干燥剂的作用是

(5)装置同图2。待CO2传感器显示CO2读数稳定后,用铁丝戳破装有Na2O2的塑料袋,使过氧化钠粉末与较干燥的CO2充分接触,打开数据采集器,得到图6、图7。

【结论与反思】
(1)小组同学通过上述实验得出猜想
(2)分析图3中相对湿度变化的原因是
【知识点】 制取二氧化碳原理的拓展解读 设计实验探究物质的成分解读
您最近一年使用:0次
2021-04-23更新
|
429次组卷
|
4卷引用:2021年“金钥匙”科技竞赛初三学生CESL活动决赛化学试题
四、计算题 添加题型下试题
计算题
|
较难(0.4)
解题方法
11. 草酸钙晶体(CaC2O4·H2O,相对分子质量为146)在植物体内具有多种生理功能。某化学小组利用热分析仪对14.6g草酸钙晶体进行热分解,获得相关数据,绘制成如下图所示的固体质量一温度的关系曲线。

(1)草酸钙晶体由_____________ 种元素组成。
(2)温度为t1℃时,晶体全部失去结晶水,14.6g草酸钙晶体中结晶水的质量为_________ g。
(3)加热至t2℃时,CaC2O4开始分解,生成CaCO3与一种有毒气体,该气体的名称是__________ 。
(4)加热至t4℃时,CaCO3开始分解,计算图中x的值_________ 。(写出计算过程)
(5)温度在t0~t1之间时,剩余固体的成分为__________ 。

(1)草酸钙晶体由
(2)温度为t1℃时,晶体全部失去结晶水,14.6g草酸钙晶体中结晶水的质量为
(3)加热至t2℃时,CaC2O4开始分解,生成CaCO3与一种有毒气体,该气体的名称是
(4)加热至t4℃时,CaCO3开始分解,计算图中x的值
(5)温度在t0~t1之间时,剩余固体的成分为
【知识点】 有关质量守恒定律的计算解读 不含杂质的化学方程式计算解读
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:物质构成的奥秘、身边的化学物质、物质的化学变化、化学与社会发展、化学实验
试卷题型(共 11题)
题型
数量
选择题
7
填空与简答
2
实验题
1
计算题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.4 | 纯净物和混合物的判断 单质和化合物的判断 水的净化方法 | 单选题 |
| 2 | 0.65 | 质量守恒定律的微观解释 离子的概念及形成 元素的概念 燃烧的定义及条件 | 单选题 |
| 3 | 0.4 | 原子中各类微粒的数值关系 同一元素的离子与原子相互转化 | 单选题 |
| 4 | 0.65 | 根据方程式推测化学式 碳单质与某些氧化物的反应 金属冶炼的计算 | 单选题 |
| 5 | 0.65 | 二氧化碳物理性质及实验 气密性检测 | 单选题 |
| 6 | 0.4 | 有关质量守恒定律的计算 不含杂质的化学方程式计算 根据化学式计算元素质量比 根据化学式计算元素质量分数 | 单选题 |
| 7 | 0.65 | 有关质量守恒定律的计算 用质量守恒定律确定物质组成 | 单选题 |
| 二、填空与简答 | |||
| 8 | 0.65 | 化学方程式的书写 根据方程式推测化学式 金属与氧气反应 电解水实验的现象和结论 | 填空题 |
| 9 | 0.4 | 化学方程式的书写 不含杂质的化学方程式计算 高锰酸钾制取氧气实验 盐类参与的反应 | 流程题 |
| 三、实验题 | |||
| 10 | 0.4 | 制取二氧化碳原理的拓展 设计实验探究物质的成分 | |
| 四、计算题 | |||
| 11 | 0.4 | 有关质量守恒定律的计算 不含杂质的化学方程式计算 | |



