2023年广东省广州市荔湾区中考一模化学试题
广东
九年级
一模
2023-04-15
1793次
整体难度:
适中
考查范围:
身边的化学物质、化学与社会发展、物质构成的奥秘、物质的化学变化、化学实验
一、选择题 添加题型下试题
| A.氮气可用作焊接金属时的保护气 |
| B.氧气能够支持燃挠,可用作燃料 |
| C.二氧化碳是形成酸雨的污染物 |
| D.氢氧化钠可用作改良酸性土壤 |
| A.用玻璃钢制作的船体 | B.用青铜制作的东汉铜奔马 |
| C.用大理石制作的天安门华表 | D.用可降解塑料作手术缝合线 |
| A.组成:由C和O2组成 | B.性质:与CO相似,能与CuO反应 |
| C.用途:可用于生产碳酸型饮料 | D.制取:实验室采用木炭燃烧获得 |
| A.葡萄糖酸锌属于混合物 |
| B.葡萄糖酸锌中氧元素的质量分数最大 |
| C.葡萄糖酸锌的相对分子质量是455g |
| D.葡萄糖酸锌中C、H、O、Zn四种元素的质量比为12:22:14:1 |
| A.实验室制取氢气时,先装药品,后检查装置的气密性 |
| B.CO还原CuO实验开始时,先通入CO,再点燃酒精灯加热 |
| C.加热KMnO4并用排水法收集O2的实验结束时,先熄灭酒精灯,后移出导管 |
| D.稀释浓硫酸时,先把浓硫酸倒入烧怀中,后沿器壁缓慢注入水,边加边搅拌 |
年份 | 煤炭 | 石油 | 清洁能源 |
2015年 | 63.8% | 18.4% | 17.8% |
2018年 | 59.0% | 18.9% | 22.1% |
2021年 | 56.0% | 18.7% | 25.3% |
| A.水能、风能、煤类都是清洁能源 |
| B.我国能源结构中石油占比变化不明显 |
| C.石油主要含碳和氢元素,在空气中完全燃烧会产生二氧化碳和水 |
| D.氢气制取成本高和贮存困难,因此大量使用氢能源还存在一定的困难 |
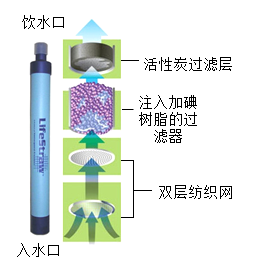
| A.生命吸管的活性炭能够降低水的硬度 |
| B.经过生命吸管净化后的水属于纯净物 |
| C.经过生命吸管净化后的水不含病毒和细菌 |
| D.生命吸管净水过程中发生了物理变化和化学变化 |
事实1:稀硫酸和氧化铜反应生成硫酸铜和水。
事实2:稀盐酸除铁锈时反应生成氯化铁和水。
| A.稀硫酸、稀盐酸均含有H+ |
| B.氧化铜、氧化铁均属于金属氧化物 |
| C.酸能与某些金属氧化物反应生成盐和水 |
| D.除锈时可将铁制品长时间浸泡在酸中 |
| A.245g | B.195 g | C.49 g | D.196 g |
【知识点】 有关溶液浓缩、稀释的计算解读
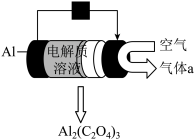
| A.利用该技术可捕捉大气中的二氧化碳 |
B.Al2(C2O4)3中酸根离子的符号为 |
| C.该反应中元素的化合价没有发生改变 |
D.该反应的化学方程式为: |
 (已知NH4HCO3在40℃受热易分解)反应中的四种物质溶解度曲线见图,下列说法正确的是
(已知NH4HCO3在40℃受热易分解)反应中的四种物质溶解度曲线见图,下列说法正确的是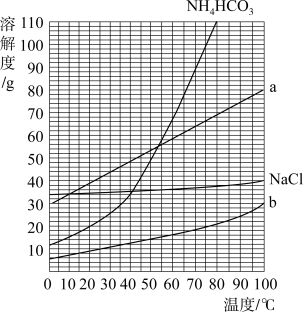
| A.在35℃时a的溶解度小于b的溶解度 |
| B.图中表示NaHCO3溶解度曲线的是a |
| C.析出NaHCO3固体是因为其溶解度变化受温度影响较小 |
| D.为提高NaHCO3的产率,反应需控制在40℃以下进行 |
【知识点】 复分解反应发生的条件解读 固体溶解度曲线的应用解读

A. 表示OH- 表示OH- |
| B.参加反应的H2SO4和NaOH的质量比为49:40 |
C.恰好完全反应后溶液中Na+和 的个数比为2:1 的个数比为2:1 |
| D.将NaOH溶液换成KOH溶液则不能产生类似的现象 |
| A.鉴别羊毛纤维和合成纤维:取样,灼烧闻气味 |
| B.鉴别NH4NO3和KC1固体:取样,加入CaCl2粉末,研磨、闻气味 |
| C.除去CuO中少量的MnO2:加入足量H2O2溶液充分反应后过滤 |
| D.除去KNO3中少量的MgSO4:加入足量蒸馏水,溶解后过滤 |
选项 | 实验操作 | 现象 | 结论 |
A | 将燃着的小木条分别插入空气样品和呼出气体的样品中 | 空气样品中木条继续燃烧,呼出气体样品中木条熄灭 | 呼出气体中不含氧气 |
B | 将白磷浸没在冷水中,再向冷水中的白磷通氧气 | 通氧气前白磷不燃烧,通氧气后白磷燃烧 | 氧气是燃烧需要的条件之一 |
C | 将石蕊染成紫色的干燥纸条放入充满HCl气体的试管中,无明显现象,再滴入水 | 紫色纸条变红色 | HCl气体溶于水后溶液的pH<7 |
D | 将电解器的两极玻璃管注满水,接通直流电源 | 两极玻璃管中有气体生成,体积比是1:2 | 水由氢原子和氧原子组成 |
| A.A | B.B | C.C | D.D |
二、填空与简答 添加题型下试题
I、2023年1月27日,中国科学院宣布经过科技攻关,在3nm光子芯片技术上取得重大突破。光子芯片的材料以第二代半导体InP、GaAs为主,传输速度比电子芯片快1000倍。
(1)铟元素(In)在元素周期表中的部分信息及原子结构示意图如图所示。
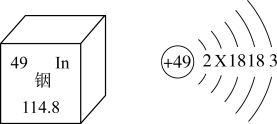
①下列说法不正确的是
A.铟元素属于金属元素B.铟的原子结构示意图中X=18
C.铟原子的中子数为49D.铟原子的核外电子分5层排布
②InP的名称是
(2)GaAs具有的性质是:①亮灰色,具有金属光泽;②性脆而硬;③加热到600℃时,外表开始被氧化膜包覆。其中属于物理性质的是
Ⅱ、2023年2月3日,中国首条量子芯片生产线在合肥正式建成投产,并用生产出来的量子芯片制造了世界上运算能力最强大的商用“悟空”量子计算机。量子芯片主要使用第三代半导体材料SiC和GnN制造,其运算速度是传统芯片的万倍,甚至亿倍。
(3)SiC中Si的化合价为+4价,则SiC中C的化合价为
(4)GaN的一种制备方法是利用Ga和NH3在一定条件下发生置换反应,该反应的化学方程式为
(1)从物质的类别来看,H2SiF6属于
(2)写出一种制备FeSiF6的方案:
(1)①向Co(NO3)2溶液中滴入少量氢氧化钠溶液,反应的化学方程式为
②向CoSO4溶液中加入足量锌粉,观察到的现象是
(2)将一段金属钴条(表面覆盖有CoCO3、Fe2O3等物质)放入过量的稀硫酸中,如图:
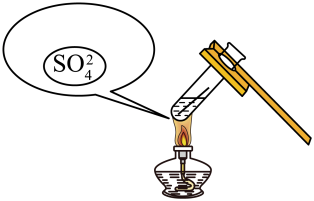
(3)四氧化三钴(Co3O4)是制备新能源汽车电池的原料之一,工业上可以将草酸钴晶体(CoC2O4·2H2O,相对分子质量为183)在空气中煅烧制得。实验室模拟其制备方法,测得煅烧过程中质量变化与温度的关系如图所示:
三、科学探究题 添加题型下试题
(1)①火法炼铜:古代人们就发现了在翠绿色的孔雀石【主要成分为Cu2(OH)2CO3】上燃烧木炭会有红色的铜生成。该过程通过两步反应生成Cu,请写出第二步的化学方程式。
第一步:
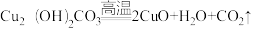
第二步:
②湿法炼铜:《梦溪笔谈》中记载“熬胆矾铁金,久之亦化为铜”。胆矾溶于水可得硫酸铜溶液,请写出“铁金化为铜”发生反应的化学方程式:
(2)铜在潮湿的空气中会生锈,产生铜锈【主要成分为Cu2(OH)2CO3】。为探究铜生锈的条件,某实验小组设计了以下所示实验。
【提出猜想】铜生锈可能与空气中的CO2、H2O、O2有关。
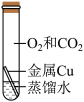
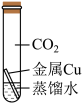
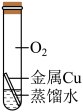
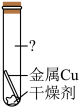
【进行实验】实验小组的同学取形状大小均相同的铜片,并打磨光亮。设计了如下图所示的4个实验并持续观察。
编号 | A | B | C | D |
实验 |
|
|
|
|
现象 | 铜丝表面出现铜锈 | 无明显现象 | 无明显现象 | 无明显现象 |
①为探究铜生锈是否与CO2有关,应选择的实验为
②有同学认为无需上述的实验也能推理出空气中的CO2和H2O肯定参加了铜生锈的反应,你认为该说法合理吗?说出你的观点并阐述理由:
(3)生活上常用醋酸(CH3COOH)浸泡法除去铜锈,其原理是:
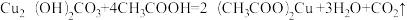
现将100g生锈的铜器放入10%的醋酸溶液(密度约为1g/cm3)中浸泡(假设其他杂质不反应),一段时间后取出铜器,清洗、烘干、称重,质量为95.56g。计算理论上至少消耗该醋酸溶液
四、综合应用题 添加题型下试题
(1)制取二氧化碳。
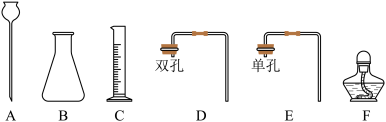
②实验室制备CO2的化学方程式为
③为了便于多次添加液体反应物,可从图中选择仪器
(2)验证碱的化学性质。完成图所示的实验1、实验2、实验3。
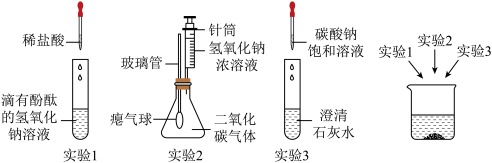
(3)探究混合溶液的组成。实验结束后,将三个实验的废液倒入同一个干净烧杯中如图,充分搅拌、静置。发现烧杯底部有白色沉淀,上层混合溶液呈红色。
①由此可初步判断上层混合溶液中肯定不含的阳离子是
②为进一步确定上层混合溶液的组成,进行以下实验探究:
步骤i:取少量上层混合溶液于试管中,加入过量碳酸钠溶液,振荡,静置。无沉淀产生,溶液呈红色。
步骤ⅱ:另取少量上层混合溶液于试管中,加入过量a溶液,振荡,静置。有白色沉淀产生,溶液呈红色。
步骤ii加入a溶液,a可选择
A.紫色石蕊B.Ba(NO3)2
C.Ba(OH)2D.CaCl2
③综合上述实验,上层混合溶液中肯定含有的离子是
五、填空与简答 添加题型下试题
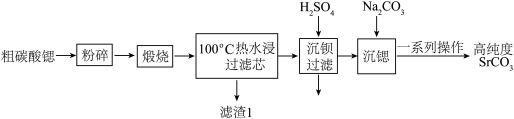
ⅱ、某些金属氧化物与水发生化合反应的条件是生成物为可溶性碱。
iii、可能用到某些物质的溶解度见下表:(g/100g水)
温度/℃ | 20 | 40 | 60 | 80 | 100 |
Sr(OH)2 | 0.81 | 1.77 | 3.68 | 8.30 | 27.9 |
Ca(OH)2 | 0.173 | 0.141 | 0.121 | 0.094 | 0.076 |
(1)将粗碳酸锶“粉碎”的目的是
(2)“煅烧”粗碳酸锶时,碳酸锶发生反应的化学方程式为
(3)滤渣1的主要成分是
(4)流程中需用温度为100℃热水浸的目的是
(5)“沉钡”过程中:
①写出含锶化合物与H2SO4反应的化学方程式
②下表为H2SO4溶液的加入量对溶液中Sr2+和Ba2+含量的影响情况:
H2SO4溶液加入量 | 过量10% | 过量20% | 过量30% |
Sr2+/(g/L) | 89.86 | 89.57 | 89.23 |
Ba2+/(g/L) | 0.21 | 0.13 | 0.11 |
(6)“沉锶”反应后的“一系列操作”为
试卷分析
试卷题型(共 20题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.65 | 空气中各成分的用途 氧气助燃性及实验 二氧化碳对生活环境的影响 中和反应的实际应用 | 单选题 |
| 2 | 0.85 | 金属材料和非金属材料 新型材料 常见物品质材的辨别 塑料、合成橡胶、合成纤维 | 单选题 |
| 3 | 0.65 | 化学式、分子式及涵义 制取二氧化碳原理的拓展 二氧化碳的用途 分子是保持物质化学性质的最小微粒 | 单选题 |
| 4 | 0.65 | 纯净物和混合物的判断 根据化学式计算相对分子质量 根据化学式计算元素质量比 根据化学式计算元素质量分数 | 单选题 |
| 5 | 0.65 | 高锰酸钾制取氧气实验 一氧化碳还原氧化铜实验 浓硫酸的稀释 氢气的制备及应用 | 单选题 |
| 6 | 0.85 | 氢气的制备及应用 资源综合利用和新能源开发的重要意义 化石燃料的形成及现状 | 单选题 |
| 7 | 0.65 | 化学变化与物理变化判断 纯净物和混合物的判断 常见几种净化水操作的比较 硬水的危害及软化方法 | 单选题 |
| 8 | 0.65 | 氧化物的定义 金属与酸反应原理 酸的通性 酸的通性的微观实质 | 单选题 |
| 9 | 0.65 | 有关溶液浓缩、稀释的计算 | 单选题 |
| 10 | 0.4 | 化学方程式的书写 离子符号的含义及书写 化合价代数和的计算与应用 空气各成分及其体积分数 | 单选题 |
| 11 | 0.4 | 复分解反应发生的条件 固体溶解度曲线的应用 | 单选题 |
| 12 | 0.65 | 根据化学方程式计算质量比 微粒图像的分析及应用 中和反应相关实验与计算 | 单选题 |
| 13 | 0.85 | 常见酸碱盐的溶解性 铵根离子的验证 羊毛、合成纤维、棉的鉴别 溶解过滤 | 单选题 |
| 14 | 0.65 | 电解水实验的现象和结论 常见的酸碱指示剂及其变色情况 实验探究燃烧条件 人体吸入空气和呼出气体实验结论 | 单选题 |
| 二、填空与简答 | |||
| 15 | 0.65 | 置换反应 化学方程式的书写 原子结构示意图含义及应用 化合价代数和的计算与应用 | 填空题 |
| 16 | 0.65 | 酸的定义 酸的通性 盐类参与的反应 | 填空题 |
| 17 | 0.4 | 有关质量守恒定律的计算 金属与盐溶液反应 酸的通性 盐类参与的反应 | 填空题 |
| 20 | 0.4 | 固体溶解度的影响因素 中和反应的概念及微观本质 盐类参与的反应 常见酸碱盐的溶解性 | 流程题 |
| 三、科学探究题 | |||
| 18 | 0.15 | 含杂质的化学方程式计算 金属与盐溶液反应 金属铜化学性质的探究 | |
| 四、综合应用题 | |||
| 19 | 0.4 | 制取二氧化碳的原理 碱的通性 盐类参与的反应 设计实验探究物质的成分 | |