2023-2024九化课后作业与单元测试 鲁教版 第五单元 单元测试A卷
全国
九年级
单元测试
2024-02-17
16次
整体难度:
适中
考查范围:
物质的化学变化、物质构成的奥秘、身边的化学物质、化学与社会发展
一、选择题 添加题型下试题
| A.原子数目 | B.原子种类 |
| C.物质种类 | D.反应前后物质的总质量 |
【知识点】 质量守恒定律内容及适用范围解读 质量守恒定律的微观解释解读
| A.离子都带电荷,则带电荷的粒子都是离子 |
| B.金属单质都能导电,则能导电的单质都是金属 |
| C.CO和CO2的组成元素相同,则它们的化学性质相同 |
| D.蜡烛充分燃烧生成H2O和CO2,则蜡烛组成里一定含有H和C |
 则x的化学式是
则x的化学式是| A.NH3 | B.NO | C.H2O | D.NO2 |
【知识点】 根据方程式推测化学式解读

| A.在化学变化中,分子可分解为原子 |
| B.在化学变化中,原子可重新组成新分子 |
| C.在化学反应前后,元素的种类发生改变 |
| D.在化学反应前后,原子的个数没有改变 |
【知识点】 质量守恒定律的微观解释解读 微粒图像的分析及应用解读
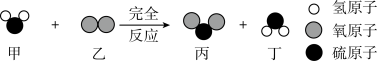
| A.反应前后原子种类不变 | B.反应前后分子个数减少 |
| C.甲和乙反应的分子个数比为1:1 | D.丙中两种元素的质量比1:1 |
| A.10克水受热变成10克水蒸气 |
| B.纸在空气中燃烧化为灰烬,灰烬的质量比纸的质量小 |
| C.10毫升水和10毫升酒精混合后,总体积小于20毫升 |
| D.蜡烛受热融化,冷却后质量不变 |
【知识点】 质量守恒定律内容及适用范围解读 用质量守恒定律解释现象解读
| A.172 | B.108 | C.70 | D.27 |
【知识点】 有关质量守恒定律的计算解读
| 物质 | A | B | C | D |
反应前质量 | 18 | 1 | 2 | 32 |
反应后质量 | 待测 | 26 | 2 | 12 |
| A.待测值是13 | B.该反应是分解反应 |
| C.D是生成物 | D.C一定是该反应的催化剂 |
| 物质质量 | A | B | C | D |
| 反应前质量/g | 2 | 28 | 2 | 1 |
| 反应后质量/g | 13 | 4 | 2 | 未知 |
则下列说法正确的是( )
| A.A和B的相对分子质量比一定为11:24 |
| B.B物质是生成物 |
| C.C物质一定是催化剂 |
| D.反应后D的质量是14g |
【知识点】 催化剂的概念、性质与用途解读 有关质量守恒定律的计算解读
 2HCl的认识中,不正确的是
2HCl的认识中,不正确的是| A.该反应的条件是点燃 | B.该反应前后原子种类和个数没变 |
| C.反应前后分子个数变了 | D.表示氢气在氯气中燃烧生成氯化氢 |

| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
【知识点】 化合反应解读 微粒图像的分析及应用解读
| A.20℃,1L水与1L酒精混合后的体积等于2L |
| B.20℃,1g二氧化锰和烧杯中1g过氧化氢溶液混合,烧杯中物质质量为2g |
| C.20℃,1g硫粉在1g氧气中完全燃烧后生成2g二氧化硫 |
| D.20℃,1g水加入1g氯化钠固体能得到2g食盐水 |
| A.小于 20 克 | B.等于 20 克 | C.大于 20 克 | D.以上情况都可能 |
【知识点】 不含杂质的化学方程式计算解读 镁在氧气中燃烧及其实验解读
| A.SiCl | B.SiH2Cl2 | C.SiHCl3 | D.SiH4 |
【知识点】 根据方程式推测化学式解读
| 序号 | 错误实例 | 错因分析 |
| A | 铁与硫酸铜溶液生成硫酸铁和铜 | 反应产物不正确 |
| B | FeCl3+3NaOH=Fe(OH)3+NaCl | 只缺少沉淀符号 |
| C | 2KMnO4=K2MnO4+MnO2+O2↑ | 反应条件不正确 |
| D | 用托盘天平、烧杯、盐酸、碳酸钠固体验证质量守恒定律 | 反应中有气体逸出 |
| A.A | B.B | C.C | D.D |
【知识点】 实验探究质量守恒定律解读 化学方程式的书写解读
| A.以客观事实为基础 | B.只要不是在常温、常压下发生的反应,均要注明反应的条件 |
| C.遵循质量守恒定律 | D.生成物中的气体一定要标注“↑” |
| 物质 | a | b | C | d |
| 反应前质量(g) | 1 | 30 | 17 | 2 |
| 反应后质量(g) | m | 39 | 0 | 10 |
| A.表中m为1g | B.a可能是该反应的催化剂 |
| C.该反应是化合反应 | D.反应中b与d的质量比为9:8 |
| 物质 | X | 氧气 | 二氧化碳 | 水 | 一氧化碳 |
| 反应前质量/g | 6.6 | 8.8 | 0 | 0 | 0 |
| 反应后质量/g | 2 | 0 | 6.6 | 5.4 | a |
| A.X中碳元素的质量分数为52.2% | B.X中只含有C、H两种元素 |
| C.表中a的值为3.4 | D.无法确定X中是否含有氧元素 |
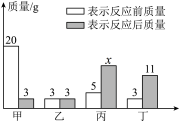
| A.x=9 | B.甲中元素种类与丙、丁中的元素种类之和相同 |
| C.甲可能是单质 | D.丙和丁的相对分子质量之比一定是9:8 |
| 物质 时刻 | 甲 | 乙 | 丙 | 丁 |
| 起始 | 80g | 5g | 100g | 5g |
| t1 | a | 55g | 60g | 5g |
| t2 | b | c | 40g | 5g |
| A.甲是反应物,乙是生成物 | B.丁可能是该反应的催化剂 |
| C.a = 70g,c = 80g | D.该反应可能是N2+3H2 2NH3 2NH3 |
二、填空与简答 添加题型下试题
(1)工业上高温煅烧石灰石制取二氧化碳和氧化钙:
(2)高温条件下,一氧化碳和氧化铁反应生成铁和二氧化碳:
(3)在溶液中,硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠:
(4)金属镁在二氧化碳中燃烧生成氧化镁和碳:
【知识点】 有关质量守恒定律的计算解读 化学方程式的书写解读
(1)对质量守恒定律的微观解释是:在化学反应中,反应前后原子的
(2)在一定条件下,将100 mL的CO2缓缓通过足量的淡黄色固体Na2O2,充分反应后,生成50mL纯净的气体X,X能使带火星的木条复燃,淡黄色固体部分变为白色固体Y。
友情提示:在同温同压下,气体的体积比等于分子个数比。
请回答:X气体是
(3)汽车安装安全气囊可以有效保护乘车人员,在车辆发生剧烈碰撞的瞬间,安全装置通电点火,使其中的粉末迅速分反应放出大量的氮气,形成气囊。该粉末由Fe2O3固体和化合物甲组成,加热13.0 g化合物甲,完全分解生成8.4 g氮气和单质乙。单质乙可在高温隔绝空气的条件下与Fe2O3发生置换反应生成Na2O。则化合物甲的化学式是

(1)物质A属于
(2)请写出该反应的化学方程式
【知识点】 化学方程式 质量守恒定律的微观解释解读
(1)两个碳酸根离子
(2)标出Cu2O中铜元素的化合价
(3)两个铜原子
(4)ZnCO3分解的化学方程式
减少CO2等温室气体排放,限制全球气温上升已成为全人类的共同目标。全球越来越多的国家开展“碳达峰、碳中和”研究。“碳达峰”是指某个地区或行业年度CO2排放量达到历史最高值,然后经历平台期进入持续下降的过程,达峰目标包括达峰年份和峰值。实现碳达峰的总体思路是以清洁低碳可持续发展为方向,加快实施“两个替代”,即能源开发实施清洁替代,能源使用实施电能替代。“碳中和”是指某个地区在一定时间内人为活动直接和间接排放的CO2与通过植树造林和碳捕获、利用与封存等吸收的CO2相互抵消,从而实现CO2“净零”排放。我国目前能源结构中,化石能源消费占比达85%,以燃煤发电和供热为主排放的CO2占总排放量的47%。因此,我国能源结构转型任重道远。2019~2030年间的部分年份,在现有模式和替代情景下我国煤电行业排放CO2如图所示。

回答下列问题:
(1)大气中CO2含量过高导致的环境问题是
(2)开发和利用新能源成为越来越迫切的要求。下列属于新能源的是______(填字母序号)。
| A.煤 | B.核能 | C.石油 | D.天然气 | E.风能 |
(3)根据图中信息,在“加快两个替代情景”下,我国煤电行业排放CO2于
(4)以CO2和NH3为原料生产尿素(CO(NH2)2)是实现“碳达峰、碳中和”的成功范例。该反应的化学方程式是

(1)该反应的化学方程式为
(2)参加反应的甲、乙两物质的质量比为
【知识点】 化学方程式的书写解读 根据化学方程式计算质量比解读

(1)图A为红磷燃烧测定空气中氧气含量的实验装置,有关的化学方程式为
(2)图B是除去水中不溶性固体杂质的过滤装置.浑浊的粗盐水过滤后发现仍然比较浑浊,可能的原因为
(3)图C是探究质量守恒定律的实验装置,反应停止后,发现天平不平衡了。该反应是否遵守质量守恒定律?
三、实验题 添加题型下试题

将锥形瓶倾斜,使稀盐酸和石灰石接触,待充分反应后,发现天平指针指向
【知识点】 实验探究质量守恒定律解读 用质量守恒定律解释现象解读
四、科学探究题 添加题型下试题


(1)镁跟氧气反应的符号表达式是
(2)小明通过称量发现:图1中石棉网上收集到产物的质量小于镁条的质量。你认为其原因可能是
(3)小红按图2装置改进实验,验证质量守恒定律,她却发现产物中还有一些黄色固体。
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水反应生成氨气,氨气能使酚酞溶液变红。
【做出猜想】黄色固体为Mg3N2。
【实验探究】
实验操作 | 实验现象及结论 |
| 如图23,取燃烧产物于烧杯B中,加入适量水,然后用大烧杯罩住小烧杯A和B | 现象: 结论:燃烧产物中含Mg3N2。 |
A.3.33g B.4.00g C.3.28g D.3.96g
【知识点】 实验探究质量守恒定律解读 不含杂质的化学方程式计算解读
五、计算题 添加题型下试题
 4Al+3O2↑,电解
4Al+3O2↑,电解 氧化铝最多可生产多少
氧化铝最多可生产多少 铝?(写出必要的计算过程,计算结果精确到
铝?(写出必要的计算过程,计算结果精确到 )
)
【知识点】 含杂质的化学方程式计算解读
计算:
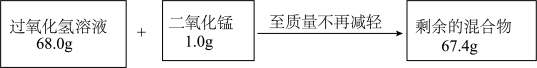
(1)反应生成氧气的质量______;
(2)该溶液中过氧化氢的质量.
【知识点】 质量守恒定律的应用 不含杂质的化学方程式计算解读
试卷分析
试卷题型(共 32题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 质量守恒定律内容及适用范围 质量守恒定律的微观解释 | 单选题 |
| 2 | 0.85 | 用质量守恒定律确定物质组成 离子的概念及形成 物质化学性质的决定因素 金属的物理通性与用途 | 单选题 |
| 3 | 0.65 | 根据方程式推测化学式 | 单选题 |
| 4 | 0.94 | 质量守恒定律的微观解释 微粒图像的分析及应用 | 单选题 |
| 5 | 0.85 | 质量守恒定律内容及适用范围 质量守恒定律的微观解释 根据化学式计算元素质量比 | 单选题 |
| 6 | 0.85 | 质量守恒定律内容及适用范围 用质量守恒定律解释现象 | 单选题 |
| 7 | 0.65 | 有关质量守恒定律的计算 | 单选题 |
| 8 | 0.65 | 催化剂的概念、性质与用途 分解反应 有关质量守恒定律的计算 | 单选题 |
| 9 | 0.65 | 催化剂的概念、性质与用途 有关质量守恒定律的计算 | 单选题 |
| 10 | 0.94 | 化学方程式含义 | 单选题 |
| 11 | 0.65 | 化合反应 微粒图像的分析及应用 | 单选题 |
| 12 | 0.94 | 质量守恒定律内容及适用范围 用质量守恒定律解释现象 不含杂质的化学方程式计算 | 单选题 |
| 13 | 0.94 | 不含杂质的化学方程式计算 镁在氧气中燃烧及其实验 | 单选题 |
| 14 | 0.85 | 根据方程式推测化学式 | 单选题 |
| 15 | 0.85 | 实验探究质量守恒定律 化学方程式的书写 | 单选题 |
| 16 | 0.94 | 化学方程式的书写 | 单选题 |
| 17 | 0.65 | 催化剂的概念、性质与用途 化合反应 有关质量守恒定律的计算 | 单选题 |
| 18 | 0.4 | 有关质量守恒定律的计算 用质量守恒定律确定物质组成 根据化学式计算元素质量分数 | 单选题 |
| 19 | 0.65 | 有关质量守恒定律的计算 用质量守恒定律确定物质组成 根据化学方程式计算质量比 单质和化合物的判断 | 单选题 |
| 20 | 0.4 | 质量守恒定律内容及适用范围 有关质量守恒定律的计算 根据化学方程式计算质量比 | 单选题 |
| 二、填空与简答 | |||
| 21 | 0.85 | 化学方程式的书写 碱的通性 盐类参与的反应 | 填空题 |
| 22 | 0.85 | 有关质量守恒定律的计算 化学方程式的书写 | 填空题 |
| 23 | 0.65 | 质量守恒定律的微观解释 用质量守恒定律确定物质组成 化学方程式含义 根据方程式推测化学式 | 填空题 |
| 24 | 0.65 | 化学方程式 质量守恒定律的微观解释 | 填空题 |
| 25 | 0.85 | 分解反应 化学方程式的书写 离子符号的含义及书写 化学符号周围数字的含义 | 填空题 |
| 26 | 0.85 | 化学方程式的书写 二氧化碳对生活环境的影响 资源综合利用和新能源开发的重要意义 化石燃料的形成及现状 | 科普阅读题 |
| 27 | 0.65 | 化学方程式的书写 根据化学方程式计算质量比 | 填空题 |
| 28 | 0.65 | 质量守恒定律内容及适用范围 化学方程式的书写 测定空气中氧气含量的实验误差分析 过滤操作问题分析 | 填空题 |
| 三、实验题 | |||
| 29 | 0.65 | 实验探究质量守恒定律 用质量守恒定律解释现象 | |
| 四、科学探究题 | |||
| 30 | 0.65 | 实验探究质量守恒定律 不含杂质的化学方程式计算 | |
| 五、计算题 | |||
| 31 | 0.85 | 含杂质的化学方程式计算 | |
| 32 | 0.65 | 质量守恒定律的应用 不含杂质的化学方程式计算 | |



