安徽省长丰县2018届九年级下学期第二次教学质量检测化学试题
安徽
九年级
二模
2018-05-07
292次
整体难度:
适中
考查范围:
物质的化学变化、身边的化学物质、化学与社会发展、物质构成的奥秘、化学实验
安徽省长丰县2018届九年级下学期第二次教学质量检测化学试题
安徽
九年级
二模
2018-05-07
292次
整体难度:
适中
考查范围:
物质的化学变化、身边的化学物质、化学与社会发展、物质构成的奥秘、化学实验
一、选择题 添加题型下试题
选择题-单选题
|
容易(0.94)
1. 下列是我省部分非物质文化遗产,其制作过程中涉及化学变化的是
A.  徽州竹雕 徽州竹雕 | B.  霍邱柳编 霍邱柳编 | C.  阜阳杜氏刻铜 阜阳杜氏刻铜 | D.  临泉葫芦烙画 临泉葫芦烙画 |
【知识点】 化学变化与物理变化判断解读
您最近一年使用:0次
选择题-单选题
|
容易(0.94)
2. 每年的3月12日是我国的植树节,植树造林可以保护环境,维持生态系统,改善人们的生活居住环境等。下列做法对自然环境不利的是
| A.研究、开发、利用氢能源 | B.乘坐公共交通工具出行 |
| C.垃圾集中露天焚烧处理 | D.城市禁止燃放烟花爆竹 |
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
4. 逻辑推理是化学学习中常用的思维方法,下列推理正确的是
| A.MnO2作催化剂能加快过氧化氢的分解,所以催化剂只加快反应速率 |
| B.煤不完全燃烧时会产生CO气体,所以物质不完全燃烧时均会产生CO气体 |
| C.化学变化过程中都伴随着能量变化,所以伴有能量变化的物质变化都是化学变化 |
| D.化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物 |
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
5. 羰(音tāng)基硫是一种与CO2结构相似的气体,化学式为COS,这种气体通常被视作生命迹象存在的反映。其组成元素的部分信息如图所示,下列有关说法正确的是
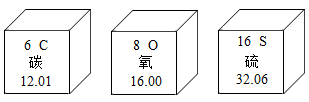

| A.羰基硫属于氧化物 | B.相对分子质量为60.07g |
| C.硫原子的质子数比氧原子的中子数多8 | D.3种元素的最外层电子数均不相同 |
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
6. 尿素是含氮量最高的常用氮肥,其化学式为:CO(NH2)2,下列有关说法正确的是
| A.尿素属于复合肥 | B.尿素中N元素的质量分数最大 |
| C.1分子尿素中含有2分子NH3 | D.尿素中C、H两种元素的质量比为1:4 |
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
8. 取两块大小相同的干冰,在一块干冰中央挖一个小穴,撒入一些镁粉,用红热的铁棒把镁点燃,将另一块干冰盖上,你会看到镁粉在干冰内继续燃烧,像冰灯中装进一个电灯泡一样,发出耀眼的白光,下列有关说法错误的是
| A.该实验说明金属Mg可与CO2反应 | B.该实验说明干冰易升华 |
| C.干冰中的分子间没有间隔 | D.干冰升华时,CO2分子间的距离变大 |
【知识点】 微粒的观点解释现象解读 二氧化碳物理性质及实验解读
您最近一年使用:0次
2018-05-07更新
|
90次组卷
|
2卷引用:安徽省长丰县2018届九年级下学期第二次教学质量检测化学试题
选择题-单选题
|
适中(0.65)
9. 二氧化硫和氧气在一定条件下可反应生成三氧化硫微观过程如图所示,下列说法中错误的是
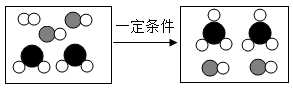

| A.该反应属于化合反应 |
| B.反应前后原子总数减少 |
C.“ ”分子可能是该反应的催化剂 ”分子可能是该反应的催化剂 |
| D.参加反应的SO2和O2的个数比为2:1 |
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
10. 如图是甲、乙两种物质(均不含结晶水)的溶解度曲线,下列有关说法正确的是
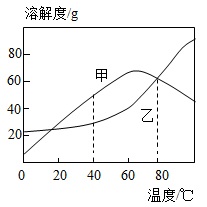

| A.两种物质的溶解度均随温度升高而增大 |
| B.40℃时,甲的饱和溶液比乙的饱和溶液质量大 |
| C.80℃时,两者的饱和溶液中,溶质的质量分数相等 |
| D.80℃时,加热两者的饱和溶液,均可变为不饱和溶液 |
您最近一年使用:0次
二、填空与简答 添加题型下试题
填空与简答-填空题
|
适中(0.65)
11. 电动平衡车是一种新型的交通工具。如图为一款电动平衡车的示意图。

(1)所标物质中,属于有机合成材料的是___________ (填一种即可,下同),属于金属材料的是___________ 。
(2)合金与纯金属相比,优点是___________ ;写出能表示铝和铁的金属活动性强弱的化学方程式___________________ 。
(3)电动平衡车是现代人用来作为代步工具、休闲娱乐的一种新型的绿色环保的产物。由此你对化学与人类生活的关系有何感想?_________________________________ 。

(1)所标物质中,属于有机合成材料的是
(2)合金与纯金属相比,优点是
(3)电动平衡车是现代人用来作为代步工具、休闲娱乐的一种新型的绿色环保的产物。由此你对化学与人类生活的关系有何感想?
您最近一年使用:0次
三、实验题 添加题型下试题
实验题
|
适中(0.65)
12. CO2是中学化学中常见的气体,请根据下列装置图回答问题:

(1)仪器a的名称是_________ ;实验室制取CO2时,选用B装置比选用A装置的好处是____________ ;实验室还可用B装置制取的气体有____________ 等(需体现出该装置的优点)
(2)稀盐酸能挥发出HCl气体,因此需要用饱和 NaHCO3溶液除去CO2中的HCl,用化学方程式表示其原理____________ ;收集CO2应选用的装置是_________ (填对应装置的序号)
(3)已知将CO2通入紫色石蕊试液中,溶液会变红,原因是_______________________ 。

(1)仪器a的名称是
(2)稀盐酸能挥发出HCl气体,因此需要用饱和 NaHCO3溶液除去CO2中的HCl,用化学方程式表示其原理
(3)已知将CO2通入紫色石蕊试液中,溶液会变红,原因是
您最近一年使用:0次
四、填空与简答 添加题型下试题
填空与简答-流程题
|
较难(0.4)
13. 随着环境问题的日益严重,垃圾的处理问题正日益被人们所重视。实验室模仿某垃圾处理厂对金属垃圾(主要成分是铁、铜、氧化铁、二氧化硅)处理及综合利用的部分工艺如图所示。
已知:FeSO4容易被空气中的O2氧化。请回答下列问题:

(1)从铜、铁混合物中分离出铁的物理方法为________________________ 。
(2)操作Ⅰ为____________ 操作,此操作中玻璃棒的作用是____________________ 。
(3)步骤②中所发生的反应为Fe+H2SO4=FeSO4+H2↑ 、_____________________ 、Fe2(SO4)2+Fe=3FeSO4等。
(4)操作Ⅱ是将FeSO4溶液在氮气环境中_________ 、冷却结晶、过滤,得到FeSO4晶体,其中氮气的作用是____________ 。
已知:FeSO4容易被空气中的O2氧化。请回答下列问题:

(1)从铜、铁混合物中分离出铁的物理方法为
(2)操作Ⅰ为
(3)步骤②中所发生的反应为Fe+H2SO4=FeSO4+H2↑ 、
(4)操作Ⅱ是将FeSO4溶液在氮气环境中
您最近一年使用:0次
五、科学探究题 添加题型下试题
科学探究题
|
较难(0.4)
14. 小明、小芳二位同学为探究盐酸的化学性质,,做了如下实验:

(1)若用pH试纸测该盐酸的pH值,则具体操作为___________ 。
(2)反应后试管C中一定含有的阳离子是___________ (写离子符号);试管D中反应的化学方程式为_________________________________ 。
(3)小芳同学把反应后D、E试管中的废液倒入一个洁净的烧杯中,观察到先有气泡产生,后有白色沉淀生成,过滤,得到白色沉淀和无色滤液。
小明同学欲探究无色滤液中的溶质成分:
小明同学分析得出无色滤液中一定不含HCl,理由是______________________ 。
(4)【提出问题】无色滤液的溶质是什么?
【作出猜想】①NaCl;②NaCl和CaCl2;③NaCl和Na2CO3。
【进行实验】

(1)若用pH试纸测该盐酸的pH值,则具体操作为
(2)反应后试管C中一定含有的阳离子是
(3)小芳同学把反应后D、E试管中的废液倒入一个洁净的烧杯中,观察到先有气泡产生,后有白色沉淀生成,过滤,得到白色沉淀和无色滤液。
小明同学欲探究无色滤液中的溶质成分:
小明同学分析得出无色滤液中一定不含HCl,理由是
(4)【提出问题】无色滤液的溶质是什么?
【作出猜想】①NaCl;②NaCl和CaCl2;③NaCl和Na2CO3。
【进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,滴加少量① | 无明显现象 | 猜想③成立 |
| 取少量滤液于试管中,滴加稀盐酸 | ② |
您最近一年使用:0次
科学探究题
|
适中(0.65)
解题方法
15. 化学反应速率是衡量化学反应进行快慢的物理量,为了探究影响化学反应速率的因素,以过氧化氢分解为研究对象进行实验。各小组均可采用如图装置进行实验,记录收集10mL氧气的时间,实验室可供选择的试剂有:2.5%、5%、10%三种浓度的H2O2溶液、MnO2、CuO、红砖粉末。

A组:探究催化剂对化学反应速率的影响;
取5mL10%H2O2溶液,三次实验分别加入0.5gMnO2、红砖粉末、CuO进行实验,记录数据如下:
由此得出结论:MnO2、CuO对H2O2分解有催化作用,红砖粉末无催化作用。
(1)你认为该结论是否正确,为什么?_________________________________________ 。
(2)经过补充对比实验,证明红砖粉末有催化作用,则三者的催化效率由高到低的顺序为___________ 。
B组:探究浓度对化学反应速率的影响
甲同学:取10mL5%H2O2溶液,加入0.5gMnO2为催化剂,,进行实验,记录时间t1。
(3)乙同学:取10mL2.5%H2O2溶液,加入__________ 为催化剂,进行实验,记录时间t2。
实验结果:_______________________________________________________
结论:___________________________________________________________
【拓展探究】
(4)C组:探究____________ 对化学反应速率的影响。
各取10mL5%H2O2溶液和0.5gCuO为催化剂进行实验,两次实验分别将试管置于冰水浴和50℃热水浴,记录时间t3、t4。
(5)实验结果:_________________________ ;
结论:当反应物浓度和催化剂相同时,__________________________________ 。
(6)以上三组实验说明,影响化学反应速率的因素有:________________________ 。

A组:探究催化剂对化学反应速率的影响;
取5mL10%H2O2溶液,三次实验分别加入0.5gMnO2、红砖粉末、CuO进行实验,记录数据如下:
| 试剂 | MnO2 | 红砖粉末 | CuO |
| t/s | 10 | 60 | 20 |
(1)你认为该结论是否正确,为什么?
(2)经过补充对比实验,证明红砖粉末有催化作用,则三者的催化效率由高到低的顺序为
B组:探究浓度对化学反应速率的影响
甲同学:取10mL5%H2O2溶液,加入0.5gMnO2为催化剂,,进行实验,记录时间t1。
(3)乙同学:取10mL2.5%H2O2溶液,加入
实验结果:
结论:
【拓展探究】
(4)C组:探究
各取10mL5%H2O2溶液和0.5gCuO为催化剂进行实验,两次实验分别将试管置于冰水浴和50℃热水浴,记录时间t3、t4。
(5)实验结果:
结论:当反应物浓度和催化剂相同时,
(6)以上三组实验说明,影响化学反应速率的因素有:
您最近一年使用:0次
六、计算题 添加题型下试题
计算题
|
较难(0.4)
16. 铁钉长期放置在潮湿的环境中会生锈(用Fe2O3表示铁锈)。取10g生锈的铁钉放入试管中,用CO还原,充分反应后,称得剩余固体质量为8.8g,请计算:
(1)生成CO2的质量为__________g;
(2)此铁钉中铁锈的质量分数为__________.
(1)生成CO2的质量为__________g;
(2)此铁钉中铁锈的质量分数为__________.
【知识点】 含杂质的化学方程式计算解读 工业炼铁的原理及装置解读
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:物质的化学变化、身边的化学物质、化学与社会发展、物质构成的奥秘、化学实验
试卷题型(共 16题)
题型
数量
选择题
10
填空与简答
2
实验题
1
科学探究题
2
计算题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 化学变化与物理变化判断 | 单选题 |
| 2 | 0.94 | 空气的污染与防治 | 单选题 |
| 3 | 0.85 | 蛋白质 维生素 油脂的来源 糖类的来源 | 单选题 |
| 4 | 0.65 | 催化剂的概念、性质与用途 用质量守恒定律确定物质组成 单质和化合物的判断 能量转化与化学变化的关系 | 单选题 |
| 5 | 0.65 | 氧化物的定义 核外电子排布规律的理解及应用 元素周期表信息示意图 化学式量及相对分子质量的定义 | 单选题 |
| 6 | 0.65 | 化学式、分子式及涵义 根据化学式计算元素质量比 根据化学式计算元素质量分数 常见化肥的种类及性质 | 单选题 |
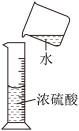
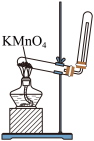
| 7 | 0.65 | 氧气的制取中装置的选择 浓硫酸的稀释 气密性检测 气体净化、干燥 | 单选题 |
| 8 | 0.65 | 微粒的观点解释现象 二氧化碳物理性质及实验 | 单选题 |
| 9 | 0.65 | 催化剂的概念、性质与用途 化合反应 质量守恒定律的微观解释 微粒图像的分析及应用 | 单选题 |
| 10 | 0.65 | 饱和溶液和不饱和溶液的转换 固体溶解度曲线的应用 溶解度的相关计算 | 单选题 |
| 二、填空与简答 | |||
| 11 | 0.65 | 化学方程式的书写 金属材料和非金属材料 合金的认识 常见物品质材的辨别 | 填空题 |
| 13 | 0.4 | 空气中各成分的用途 结晶分离混合物 酸的通性 过滤 | 流程题 |
| 三、实验题 | |||
| 12 | 0.65 | 化学方程式的书写 氧气的制取中装置的选择 二氧化碳与水的反应及实验 常见的酸碱指示剂及其变色情况 | |
| 四、科学探究题 | |||
| 14 | 0.4 | 酸的通性 溶液的酸碱性的判断与pH的测定 盐类参与的反应 几种常见阴、阳离子的鉴别 | |
| 15 | 0.65 | 催化剂的概念、性质与用途 过氧化氢制取氧气实验 控制变量法在实验设计中的应用 | |
| 五、计算题 | |||
| 16 | 0.4 | 含杂质的化学方程式计算 工业炼铁的原理及装置 | |