广东省佛山市南海区2019-2020学年九年级上学期期末化学试题
广东
九年级
期末
2020-02-06
411次
整体难度:
适中
考查范围:
物质的化学变化、化学实验、身边的化学物质、物质构成的奥秘、化学与社会发展
一、选择题 添加题型下试题
| A.灯泡充入稀有气体通电后显示不同的颜色 |
| B.工业制氧气 |
| C.多种金属加热融合制合金 |
| D.燃油产生动力使飞机升空 |
【知识点】 化学变化与物理变化判断解读
| A.活性炭可吸附水中的色素及异味 |
| B.用明矾可除去水中的悬浮物 |
| C.生活中常用蒸馏的方法降低水的硬度 |
| D.可用肥皂水鉴别硬水与软水 |
【知识点】 常见几种净化水操作的比较解读 硬水和软水定义及鉴别解读
| A.三种氧化物指二氧化硫、二氧化碳、二氧化氮 |
| B.燃放鞭炮只产生PM10,不会造成酸雨 |
| C.空气中的臭氧对身体有害,应把大气层中的臭氧全部除去 |
| D.保护空气的途径有加强大气监测和积极植树造林等 |
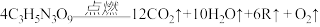 。下列说法错误的是
。下列说法错误的是| A.R的化学式是N2,属于单质 |
| B.三硝酸甘油酯爆炸产生大量气体 |
| C.三硝酸甘油酯的相对分子质量是227 |
| D.三硝酸甘油酯中C、H、N、O元素的质量比=3:5:3:9 |
A.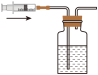 检查装置气密性 检查装置气密性 | B. 点燃酒精灯 点燃酒精灯 | C.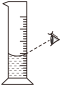 量取液体 量取液体 | D. 称量固体 称量固体 |
| A.木炭在氧气中燃烧,有无色刺激性气味气体产生 |
| B.纯净的氢气在空气中燃烧,发出淡蓝色火焰 |
| C.镁条在空气中剧烈燃烧发出耀眼强光,放出大量的热,生成大量白色气体 |
| D.接通直流电,电解水器正极端产生气泡速率比负极端快,气体体积比约为1:2 |
【知识点】 木炭在氧气中燃烧及其实验解读 镁在氧气中燃烧及其实验解读
| A.3个汞原子表示为3Hg |
| B.两个氨分子表示为2NH4 |
| C.4个亚铁离子表示为4Fe3+ |
| D.FeO,H2O2, H2SO4 中氧元素的化合价都是-2 |

| A.Uue元素属于金属元素 |
| B.Uue元素相对原子质量为319g |
| C.Uue原子核外电子数为119 |
| D.Uue元素的中子数为200 |
【知识点】 元素周期表信息示意图解读
| A.进入枯井或山洞前要进行灯火试验,所以进入地下煤矿前也要进行灯火试验 |
| B..铁生锈最终会导致铁制品全部被腐蚀,铝比铁活泼,所以铝在空气中也会全部被腐蚀 |
| C.生石灰与水混合放出大量热,因此石灰石与水混合也放出大量热 |
| D.煤的综合利用可以提高煤的利用率,石油分馏也可以提高石油的利用率 |
A. 验证合金和其成分中纯金属的硬度大小 验证合金和其成分中纯金属的硬度大小 |
B. 证明CO2水溶液呈酸性 证明CO2水溶液呈酸性 |
C. 实验室制取并收集少量氢气 实验室制取并收集少量氢气 |
D. 用带火星木条验证空气与人体呼出气中氧气含量多少 用带火星木条验证空气与人体呼出气中氧气含量多少 |
| A.在厨房里鉴别食盐和蔗糖的方法是尝味道 |
| B.鉴别氮气和二氧化碳,可以用燃着的木条,木条熄灭的是二氧化碳 |
| C.可用磁铁区别铁粉和镁粉 |
| D.可用二氧化锰区别水和过氧化氢 |
【知识点】 二氧化碳的检验、验满及净化解读
| 选项 | 物质 | 所含杂质 | 方案 |
| A | CO2 | CO | 点燃混合气体 |
| B | Zn | Cu | 加硫酸铜溶液后过滤 |
| C | MnO2 | KC1 | 加水溶解、过滤、洗涤、烘干 |
| D | FeC13 | CuCl2 | 加入过量的铁粉,过滤 |
| A.A | B.B | C.C | D.D |
| A化学与环境 | B性质与用途 |
| ①过量使用含磷洗衣粉会导致水体污染 ②二氧化碳的过量排放会加剧温室效应 | ①乙醇燃烧放出大量热,可与汽油混合作为汽车燃料 ②石墨有优良的导电性,可做电极 |
| C性质与现象 | D结构与性质 |
| ①因为分子不断运动,所以墙内开花墙外香 ②因为CO2密度比空气大且不能燃烧不支持燃烧,所以向燃着的高低蜡烛  中倾倒CO2,蜡烛自下而上熄灭 中倾倒CO2,蜡烛自下而上熄灭 | ①因碳原子排列方式不同,所以金刚石、石墨物理性质差异大 ②因  和 和 原子的最外层电子数相同,所以它们的化学性质相似 原子的最外层电子数相同,所以它们的化学性质相似 |
| A.A | B.B | C.C | D.D |
【知识点】 二氧化碳对生活环境的影响解读
 |  |  |  |
| A向a.b两支试管中分别加入等质量的样品,a中是氯酸钾,b中是氯酸钾和少量二氧化锰 | B利用红磷燃烧测定空气中氧气的含量(打开止水夹前) | C向一定质量AgNO3和Cu(NO3)2的混和溶液中逐渐加入足量的锌粒 | DCO和过量的氧气在密闭容器中完全反应 |
| A.A | B.B | C.C | D.D |
【知识点】 制取氧气实验的图像问题解读
二、填空与简答 添加题型下试题

(1)用氢气作燃料的优点是
(2)利用反应
 可除去氢燃料中混有的少量CO,使用某高效催化剂可大幅度降低该反应温度,微观过程如图(二)所示。请在图中最右方框处画出相应的分子微观图示
可除去氢燃料中混有的少量CO,使用某高效催化剂可大幅度降低该反应温度,微观过程如图(二)所示。请在图中最右方框处画出相应的分子微观图示(3)检验氢气中是否含有CO的操作是
三、科学探究题 添加题型下试题

(1)为了验证可燃物燃烧的条件,某同学设计了图(一)实验。装好药品后,操作顺序是
a.给燃烧管微热至46°C
b.滴入过氧化氢溶液
c.滴入盐酸
(2)如图(二)所示,分别把10mL水和澄清石灰水同时注入容器中,观察到中间U型管内的现象是
【知识点】 控制变量法在实验设计中的应用解读
四、填空与简答 添加题型下试题

(1)已知步骤②是置换反应,则水煤气中含有的有毒气体是
(2)写出步骤⑤的反应方程式
(3)若实验室模拟步骤⑧的操作,需用到的仪器有烧杯、玻璃棒、
(4)步骤⑧⑨都产生硫酸铁,但步骤
(5)该流程中可循环再用的物质是
【知识点】 常见金属矿石解读 一氧化碳还原氧化铁实验解读
五、实验题 添加题型下试题

(1)仪器①的名称是
(2)用高锰酸钾制取氧气可选用的发生装置是
(3)实验室制取二氧化碳若要随时使反应停止或发生,可选择的发生装置是
(4) 某同学利用下图装置做一氧化碳还原CuO实验。
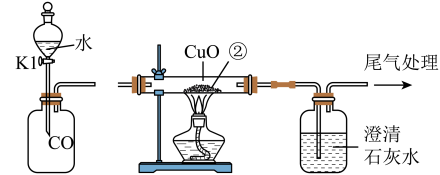
加热CuO,先打开K1, 目的是
六、科学探究题 添加题型下试题
K Ca Na Mg ① Al ② Zn ③ Fe Sn Pb (H) Cu ④ Hg Ag Pt Au
【查阅资料】
a 铬是银白色金属,常温下在空气中表面能形成致密的氧化膜;
b 锰是灰白色的金属;
c CrSO4溶液呈绿色,MnSO4溶液呈淡粉红色;
d Cr和Mn在下列反应形成的化合物中都显+2价;
通过阅读分析资料,我们知道铬的位置肯定不在
【设计实验】
| 操作 | 现象 | 分析及结论 |
| 在锰片中滴加适量的稀硫酸 | 锰是氢(H)前的金属 | |
| 在铬片和锰片中分别滴加硫酸铝溶液 | 铬片表面有固体析出,溶液变绿色,锰片表面没有明显变化 | 反应的化学方程式是 |
| 在锰片中滴加 | 锰片表面没有明显变化 | 锰的位置在 |
通过以上探究,同学们成功确定铬和锰在金属活动顺序表中的位置。
【拓展讨论】在锰片中滴加硝酸银和硝酸镁的混合溶液,充分反应后过滤,滤渣中一定有
【知识点】 金属活动顺序理解和判断解读 金属活动性强弱的探究解读
七、计算题 添加题型下试题
(1)若320g甲烷充分燃烧,消耗氧气的质量是多少克?(请写出计算过程)
(2)假设液化石油气只以丙烷(C3H8)计算,等质量的丙烷和甲烷充分燃烧,耗氧量更大的是_____,若从液化石油气改用天然气,则炉具的进风口要_____(选填“调大”或“调小”、“不改变”)。
(3)某同学想了解使用液化石油气和天然气哪个更划算,他查阅资料如下:
| 燃气 | 价格 | 热值 |
| 液化石油气 | 125元/瓶(13Kg/瓶) | 45兆焦/Kg |
| 天然气 | 4. 6元/立方米 | 33.4兆焦/立方米 |
由此可知使用_____更划算。
【知识点】 不含杂质的化学方程式计算解读
试卷分析
试卷题型(共 21题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 化学变化与物理变化判断 | 单选题 |
| 2 | 0.85 | 常用危险化学品标志 | 单选题 |
| 3 | 0.85 | 常见几种净化水操作的比较 硬水和软水定义及鉴别 | 单选题 |
| 4 | 0.85 | 空气质量报告 | 单选题 |
| 5 | 0.85 | 根据方程式推测化学式 化学式量及相对分子质量的定义 根据化学式计算元素质量比 | 单选题 |
| 6 | 0.65 | 量筒的正确使用方法和注意事项 托盘天平的正确使用方法和注意事项 酒精灯的正确使用方法和注意事项 气密性检测 | 单选题 |
| 7 | 0.85 | 木炭在氧气中燃烧及其实验 镁在氧气中燃烧及其实验 | 单选题 |
| 8 | 0.85 | 离子符号的含义及书写 元素符号书写及含义 常见元素、原子团的化合价 | 单选题 |
| 9 | 0.65 | 元素周期表信息示意图 | 单选题 |
| 10 | 0.65 | 钢铁的锈蚀 | 单选题 |
| 11 | 0.65 | 二氧化碳与水的反应及实验 探究人体吸入和呼出气体成分 | 单选题 |
| 12 | 0.65 | 二氧化碳的检验、验满及净化 | 单选题 |
| 13 | 0.65 | 常见酸碱盐的溶解性 气体净化、干燥 | 单选题 |
| 14 | 0.65 | 二氧化碳对生活环境的影响 | 单选题 |
| 15 | 0.4 | 制取氧气实验的图像问题 | 单选题 |
| 二、填空与简答 | |||
| 16 | 0.65 | 化学方程式的书写 | 填空题 |
| 18 | 0.4 | 常见金属矿石 一氧化碳还原氧化铁实验 | 流程题 |
| 三、科学探究题 | |||
| 17 | 0.65 | 控制变量法在实验设计中的应用 | |
| 20 | 0.85 | 金属活动顺序理解和判断 金属活动性强弱的探究 | |
| 四、实验题 | |||
| 19 | 0.65 | 高锰酸钾制取氧气实验 氧气的制取中装置的选择 一氧化碳还原氧化铜实验 | |
| 五、计算题 | |||
| 21 | 0.4 | 不含杂质的化学方程式计算 | |







