山东省日照市东港区日照市新营中学2020-2021学年九年级上学期期中化学试题
山东
九年级
期中
2021-04-15
292次
整体难度:
适中
考查范围:
物质构成的奥秘、身边的化学物质、化学实验、物质的化学变化、化学与社会发展
一、选择题 添加题型下试题
| A.水沸腾时可冲起壶盖,说明温度升高分子会变大 |
| B.煮沸可以给水杀菌消毒 |
| C.水的蒸发和水通电分解都属于物理变化 |
| D.将硬水过滤可得到软水 |
 ”“
”“ ”分别表示两种不同元素的原子,其中表示混合物的是
”分别表示两种不同元素的原子,其中表示混合物的是A.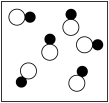 | B.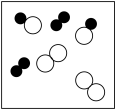 | C.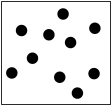 | D.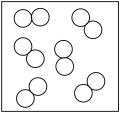 |
【知识点】 纯净物和混合物的判断解读 化学式图示的分析解读
 、
、 、
、 分别表示X、Y、Z三种不同的气体分子,其在一定条件下的变化如图所示,由图示获得的下列信息中正确的是( )
分别表示X、Y、Z三种不同的气体分子,其在一定条件下的变化如图所示,由图示获得的下列信息中正确的是( )
| A.反应前后分子的种类发生变化 |
| B.Z一定是氧化物 |
| C.该反应可表示为4X+Y=2Z |
| D.反应物和生成物都有单质 |
【知识点】 单质和化合物的判断解读 微粒图像的分析及应用解读
| A.单质 | B.化合物 | C.纯净物 | D.混合物 |
【知识点】 纯净物和混合物的判断解读 单质和化合物的判断解读

| A.丁一定是该反应的催化剂 |
| B.该反应的基本类型是分解反应 |
| C.物质丙中的元素种类一定等于甲和乙元素的种类之和 |
| D.该反应中甲、丙的质量比为7: 10 |
【知识点】 质量守恒定律内容及适用范围解读 用质量守恒定律解释现象解读
| A.氧气和臭氧、氯化钾、铁粉 | B.澄清石灰水、水蒸气、水银 |
| C.过氧化氢、四氧化三铁、氖气 | D.食盐水、氧化镁、二氧化碳 |
 中,A与B2反应的质量关系如图所示,现将6gA和8gB2充分反应,则生成AB的质量是 。
中,A与B2反应的质量关系如图所示,现将6gA和8gB2充分反应,则生成AB的质量是 。
| A.9g | B.11g |
| C.12g | D.14g |
【知识点】 有关质量守恒定律的计算解读 根据化学方程式计算质量比解读
| A.H2中H: +1价 | B.Hg2Cl2 中Hg:+1价 | C.LiCoO2中Co:+1价 | D. 中C:+1价 中C:+1价 |
【知识点】 化合价代数和的计算与应用解读
| A.都属于单质 | B.元素组成不同 |
| C.C60具有稳定结构,不能燃烧 | D.碳原子排列方式相同 |
| A.32 | B.16 | C.48 | D.64 |
【知识点】 有关质量守恒定律的计算解读
| A.10g酒精和50g水混匀后形成60g酒精溶液 |
| B.红磷在氧气中燃烧,反应后得到30g P2O5,则参加反应的O2和磷的总质量一定为30g |
| C.2L氢气和1L氧气反应,生成3L水,这符合质量守恒定律 |
| D.2g氢气和8g氧气完全反应,生成10g水,这符合质量守恒定律 |
【知识点】 质量守恒定律内容及适用范围解读
| A.洛匹那韦分子由碳、氢、氮、氧四种元素组成 |
| B.一个洛匹那韦分子含有37个碳原子、48个氢原子、4个氮原子和5个氧原子 |
| C.洛匹那韦中碳元素质量分数最大 |
| D.洛匹那韦属于化合物 |
| 物质 | 氧气 | 二氧化碳 | 水蒸气 | W |
| 反应前的质量/g | 50 | 1 | 1 | 23 |
| 反应后的质量/g | 2 | 45 | 28 | x |
| A.根据质量守恒定律,x的值应为2 |
| B.物质W只含有碳、氢元素 |
| C.该反应中的二氧化碳和水蒸气的质量比为44: 27 |
| D.反应生成二氧化碳和水的分子个数比为1: 1 |
【知识点】 有关质量守恒定律的计算解读 用质量守恒定律确定物质组成解读
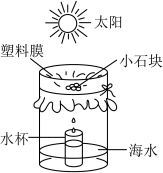
| A.水杯中的水是淡水 |
| B.从海水中获取淡水是物理变化 |
| C.海水通过活性炭吸附也能获取淡水 |
| D.获取淡水的快慢与温度有关 |
| A.化学变化中分子可以再分,但其数目不会变化 |
| B.根据元素周期表,可查找元素的原子序数、元素符号、相对原子质量 |
| C.由不同种元素组成的物质一定是化合物 |
| D.同种分子构成的物质一定是纯净物,则纯净物一定是由同种分子构成 |
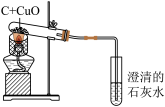
| A.该实验的条件需要高温 |
| B.木炭发生了还原反应 |
| C.该实验中网罩的作用集中火焰,提高温度 |
| D.该实验中的木炭粉可以换成活性炭 |
【知识点】 木炭还原氧化铜的实验解读

| A.甲中碳、氢元素质量比为3:8 | B.乙和丙的元素组成相同 |
| C.44g甲完全燃烧至少需160g乙 | D.生成的丙与丁的分子个数比为1:1 |
A.将水通直流电一段时间 |
B.用等质量、等浓度的双氧水制取氧气 |
C.加热一定量高锰酸钾过程中,固体中锰元素质量分数随反应时间变化关系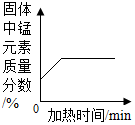 |
D.加热氯酸钾和二氧化锰的固体混合物过程中固体中氧元素质量随反应时间变化关系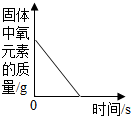 |
【知识点】 制取氧气实验的图像问题解读 电解水实验的现象和结论解读
二、填空与简答 添加题型下试题
(1)若“
 ”表示一个氮原子,则“
”表示一个氮原子,则“ ”表示:
”表示:(2)碳酸钠溶液中大量存在的阴离子:
(3)原子序数是7和14形成的化合物:
(4)写出硝酸的化学式并标出氮元素的化合价:
(5)某铁的氧化物,其中铁、氧元素的质量比为7:3,则该氧化物的化学式:
(1)加热黑白两种固体混合物产生氧气的反应:
(2)在汽车排气管上安装属气净化装置,可使尾气中的CO和NO在催化剂表面发生反应,产生两种组成空气的气体:
(3)在潜水艇里配备氧气再生装置,在常温下使过氧化钠固体(Na2O2)与二氧化碳反应生成碳酸钠和氧气:
(4)将CO2转化为甲醇(CH3OH),其反应的微观过程如图所示,该反应的化学方程式为:

(1)茶杯内的纯网,可将茶叶与茶水分离,便于饮用,该设计利用的化学原理是
(2)如图,图中缺少的一种仪器是

(3)自制净水器中常加入
(4)漂白粉中的Ca(ClO)2可用于饮用水消毒。工业上制备Ca(ClO)2的化学方程式2Cl2+Ca(OH)2=X+Ca(ClO)2+2H2O,X的化学式为
(5)下列有关过滤操作的叙述不正确的是
A 用少量水润湿滤纸,并使滤纸与漏斗壁之间留有气泡
B 漏斗下端的管口要紧靠烧杯内壁
C 玻璃棒要靠在三层滤纸的一边
D 滤纸边缘要低于漏斗口,液面要低于滤纸边缘
三、实验题 添加题型下试题

(1)气体a是
(2)负极产生的气体有
(3)电解水时,在水中加硫酸钠或氢氧化钠的目的:
(4)理论上电解水得到氧气和氢气的体积比为1:2,某同学用碳棒作电极进行电解水实验,得到氧气和氢气的体积比小于1:2,对产生此现象原因的猜想不合理的是
A 部分氧气溶于水 B 部分氧气与碳棒反应
C 部分氧气被碳棒吸附 D 部分氧气与氢气反应重新生成了水
四、填空与简答 添加题型下试题

(1)甲为
(2)甲→乙的化学方程式为
(3)乙→丙的化学方程式为
(4)从微观的角度解释甲、乙性质有差异的原因是
五、实验题 添加题型下试题

(1)白磷燃烧:白磷燃烧过程中看到的现象是
(2)若实验中所用白磷的量不足,对结果
【知识点】 实验探究质量守恒定律解读
六、计算题 添加题型下试题
(1)高锰酸钾中钾、锰、氧三种元素的质量比为_____;
(2)生成氧气的质量为_____;
(3)剩余固体中二氧化锰的质量。
【知识点】 不含杂质的化学方程式计算解读
试卷分析
试卷题型(共 27题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 微粒的观点解释现象 常见几种净化水操作的比较 硬水的危害及软化方法 电解水实验的现象和结论 | 单选题 |
| 2 | 0.94 | 过滤 | 单选题 |
| 3 | 0.65 | 纯净物和混合物的判断 化学式图示的分析 | 单选题 |
| 4 | 0.85 | 化学符号周围数字的含义 | 单选题 |
| 5 | 0.65 | 单质和化合物的判断 微粒图像的分析及应用 | 单选题 |
| 6 | 0.65 | 纯净物和混合物的判断 单质和化合物的判断 | 单选题 |
| 7 | 0.85 | 质量守恒定律内容及适用范围 用质量守恒定律解释现象 | 单选题 |
| 8 | 0.85 | 纯净物和混合物的判断 单质和化合物的判断 氧化物的定义 | 单选题 |
| 9 | 0.65 | 有关质量守恒定律的计算 根据化学方程式计算质量比 | 单选题 |
| 10 | 0.94 | 化合价代数和的计算与应用 | 单选题 |
| 11 | 0.94 | 同种元素组成的物质 C60的相关知识 结构、性质与用途的关系 碳单质的可燃性 | 单选题 |
| 12 | 0.85 | 有关质量守恒定律的计算 | 单选题 |
| 13 | 0.65 | 质量守恒定律内容及适用范围 | 单选题 |
| 14 | 0.85 | 单质和化合物的判断 化学式、分子式及涵义 根据化学式计算元素质量比 根据化学式计算元素质量分数 | 单选题 |
| 15 | 0.65 | 有关质量守恒定律的计算 用质量守恒定律确定物质组成 | 单选题 |
| 16 | 0.85 | 化学变化与物理变化判断 常见几种净化水操作的比较 海水淡化 | 单选题 |
| 17 | 0.65 | 纯净物和混合物的判断 单质和化合物的判断 元素周期表信息示意图 | 单选题 |
| 18 | 0.85 | 木炭还原氧化铜的实验 | 单选题 |
| 19 | 0.65 | 化学方程式含义 不含杂质的化学方程式计算 微粒图像的分析及应用 根据化学式计算元素质量比 | 单选题 |
| 20 | 0.65 | 制取氧气实验的图像问题 电解水实验的现象和结论 | 单选题 |
| 二、填空与简答 | |||
| 21 | 0.65 | 离子符号的含义及书写 化学式书写及读法 根据化学式计算元素质量比 常见元素、原子团的化合价 | 填空题 |
| 22 | 0.65 | 化学方程式的书写 | 填空题 |
| 23 | 0.85 | 用质量守恒定律确定物质组成 自来水厂净化过程 过滤操作要点 过滤操作问题分析 | 填空题 |
| 25 | 0.85 | 过氧化氢制取氧气实验 电解水原理 物质推断的综合应用 | 推断题 |
| 三、实验题 | |||
| 24 | 0.85 | 水的组成实验 电解水实验的现象和结论 电解水生成物的验证 | |
| 26 | 0.65 | 实验探究质量守恒定律 | |
| 四、计算题 | |||
| 27 | 0.85 | 不含杂质的化学方程式计算 | |




