Fe(OH)3 可用于制造医药、颜料等,其胶体可用于净水。某化学兴趣小组利用废铁屑来制备 Fe(OH)3 粉末的流程如下:

提示:①废铁屑主要为表面附有大量铁锈的铁。还有部分难溶于水,难溶于酸的杂质。
②Fe(OH)3难溶于水,加热时会分解生成氧化铁和水。
③反应Ⅱ中加入H2O2溶液的目的是将滤液Ⅰ中的FeSO4氧化成Fe2(SO4)3。
(1)操作a的名称为__________ 。
(2)滤液I中除了SO42-外,还存在着的离子是_________ 。(写离子符号)
(3)反应I中,需要_____ g 20%的H2SO4溶液与5.6g铁完全反应。
(4)反应Ⅲ中生成 Fe(OH)3 的化学方程式是_____ 。
(5)操作 b 后得到的 Fe(OH)3 经洗涤后只能放在阴凉处晾干,而不能用酒精灯烘干,原因是_____ 。

提示:①废铁屑主要为表面附有大量铁锈的铁。还有部分难溶于水,难溶于酸的杂质。
②Fe(OH)3难溶于水,加热时会分解生成氧化铁和水。
③反应Ⅱ中加入H2O2溶液的目的是将滤液Ⅰ中的FeSO4氧化成Fe2(SO4)3。
(1)操作a的名称为
(2)滤液I中除了SO42-外,还存在着的离子是
(3)反应I中,需要
(4)反应Ⅲ中生成 Fe(OH)3 的化学方程式是
(5)操作 b 后得到的 Fe(OH)3 经洗涤后只能放在阴凉处晾干,而不能用酒精灯烘干,原因是
更新时间:2020-05-03 10:34:26
|
相似题推荐
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】正确构建知识体系,可建立知识间的相互联系。下图是碳和碳的部分化合物间的转化关系(已知:Z物质常温时易分解),请你回答下列问题:
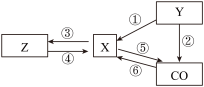
(1)写出X、Y、Z的化学式:X_______ ,Y_______ ,Z_______ 。
(2)反应①、②和⑥都属于基本反应类型中的_______ 。(填反应类型)
(3)冬天,使用煤炉取暖,在氧气充足的情况下,发生反应的化学方程式是_______ ,煤炉内的燃料燃烧正旺时,再加入一些煤炭(反应条件为高温),此时炉火的温度会降低,说明该反应会_______ 热量(填“吸收”或“放出”),写出该反应的化学方程式_______ 。
(4)写出反应③的化学方程式_______ ,若要证明该反应生成了Z,可向反应后的装置内滴加_______ ,观察到的现象是_______ ;若将上述溶液加热(或放置一段时间),观察到的现象是_______ ,反应的化学方程式是_______ 。

(1)写出X、Y、Z的化学式:X
(2)反应①、②和⑥都属于基本反应类型中的
(3)冬天,使用煤炉取暖,在氧气充足的情况下,发生反应的化学方程式是
(4)写出反应③的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】“凤凰”号火星探测器圆满完成任务,向地面发回数量堪称史无前例的图像和数据,为人类探索火星提供了宝贵的科学资料。请完成下面小题。
(1)“凤凰”号探测器发回的最新照片上显示,火星上确有液态水存在。下列微粒模型示意图可表示构成水的微粒的是____________ (填标号)。

(2)火星上含有丰富的二氧化碳和镁资源。科学家设想,镁可作为未来火星上的燃料,因为镁能在二氧化碳中燃烧放出大量的热,同时生成氧化镁和碳。该反应的化学方程式为____________________________ 。
(3)火星北极的土壤呈弱碱性。如果火星具备作物生长的条件,下表所列作物较适宜在火星北极种植的有___________________________________________ 。
(1)“凤凰”号探测器发回的最新照片上显示,火星上确有液态水存在。下列微粒模型示意图可表示构成水的微粒的是

(2)火星上含有丰富的二氧化碳和镁资源。科学家设想,镁可作为未来火星上的燃料,因为镁能在二氧化碳中燃烧放出大量的热,同时生成氧化镁和碳。该反应的化学方程式为
(3)火星北极的土壤呈弱碱性。如果火星具备作物生长的条件,下表所列作物较适宜在火星北极种植的有
| 作物名称 | 芦笋 | 草莓 | 萝卜 | 马铃薯 |
| 适宜生长的pH | 5.5~7.8 | 5.5~6.5 | 5~8 | 5.6~6 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐1】选择性催化还原(SCR)技术可有效降低柴油发动机的污染物排放,主要工作原理如下图所示:

(1)在发动机内的高温条件下,氮气可以通过化合反应转化成污染物NO,请在方框中补全相应微粒的图示。

_____________ ;
(2)在氧化催化转化器中,化合价升高的元素是_______ 。
(3)尿素[CO(NH2)2]溶液热分解时的反应方程式如下:CO(NH2)2 + H2O 2NH3↑+ CO2↑
2NH3↑+ CO2↑
若消耗60 g尿素,可以产生NH3的质量为________ g。
(4)从SCR催化转换器中排出的气体中有N2。下列推测合理的是_______ (填字母序号)
A.SCR催化转换器可能将NH3和NO2转化为N2
B.无污染的排出气中只有N2
C.进入SCR催化转换器的气体中可能含有N2

(1)在发动机内的高温条件下,氮气可以通过化合反应转化成污染物NO,请在方框中补全相应微粒的图示。

(2)在氧化催化转化器中,化合价升高的元素是
(3)尿素[CO(NH2)2]溶液热分解时的反应方程式如下:CO(NH2)2 + H2O
 2NH3↑+ CO2↑
2NH3↑+ CO2↑若消耗60 g尿素,可以产生NH3的质量为
(4)从SCR催化转换器中排出的气体中有N2。下列推测合理的是
A.SCR催化转换器可能将NH3和NO2转化为N2
B.无污染的排出气中只有N2
C.进入SCR催化转换器的气体中可能含有N2
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】2023年10月31日,神舟十六号载人飞船成功返回地面,圆满完成任务。氧气和水是保障航天员生命的重要物质。
“天宫”中水和氧气的最大化利用是保障生活的重要措施。如图是空间站资源再利用模拟图。

(1)在“水净化系统”中,活性炭可以除去色素和异味,是利用活性炭具有________ 性;用臭氧(O3)消毒,臭氧在一定条件下可以转化成氧气,该转化过程是__________ 变化(“填物理”或“化学”);高分子膜可以除去水中大分子杂质,与实验常用的_________ 操作原理相同,从微观角度分析水分子能透过高分子膜的原因_________ 。
(2)“氢氧燃料电池”中有催化剂,氢气与氧气在催化剂作用下能直接化合释放出电能,实现由化学能到电能的转化,该反应中不变的粒子是__________ ,该技术的优点:_________ 。
(3)“水电解系统”中产生氧气的电极应接在电源的________ (填“正”或“负”)极;在空间站失重状态下收集氧气可以选择下列什么装置_________ 。经换算可知理论上1个人一天约需要786克氧气,供给1个人一天用氧量至少电解水的质量是_________ 克。(保留整数)。
A. B.
B.  C.
C.  D.
D.  E.
E. 
(4)“萨巴蒂尔反应器”可以除去CO2,该反应的化学方程式是______ 。
“天宫”中水和氧气的最大化利用是保障生活的重要措施。如图是空间站资源再利用模拟图。

(1)在“水净化系统”中,活性炭可以除去色素和异味,是利用活性炭具有
(2)“氢氧燃料电池”中有催化剂,氢气与氧气在催化剂作用下能直接化合释放出电能,实现由化学能到电能的转化,该反应中不变的粒子是
(3)“水电解系统”中产生氧气的电极应接在电源的
A.
 B.
B.  C.
C.  D.
D.  E.
E. 
(4)“萨巴蒂尔反应器”可以除去CO2,该反应的化学方程式是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】用化学用语按照要求填空
(1)写出次磷酸H3PO2中磷元素的化合价_________________ ;
(2)铝离子为:Al3+,写出氢氧化铝的化学式____________________ ;写出Zn(ClO3)2的名称_______________ 。
(3)硝酸银(化学式:AgNO3)受热分解时产生三种物质,分别是银单质、氧气和一种有刺激性气味的有毒气体X,气体X可能是________________ (填字母)
A.NH3 B.SO2 C.N2 D.NO2
要得到46g气体X,需要加热_______________ g硝酸银
(1)写出次磷酸H3PO2中磷元素的化合价
(2)铝离子为:Al3+,写出氢氧化铝的化学式
(3)硝酸银(化学式:AgNO3)受热分解时产生三种物质,分别是银单质、氧气和一种有刺激性气味的有毒气体X,气体X可能是
A.NH3 B.SO2 C.N2 D.NO2
要得到46g气体X,需要加热
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿空气中易变质。CuCl 的制备流程如下:
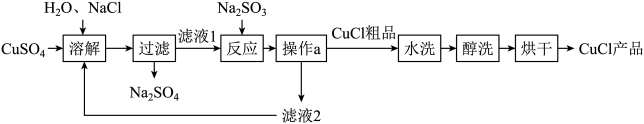
(1)“滤液 1”中除了Na+、SO42-外,还存在较多的离子是_____ 、_____ (写离子符号)。
(2)“反应”中发生的化学变化是 2CuCl2+Na2SO3=2CuCl +2NaCl+SO3
+2NaCl+SO3 ,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为
,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为_____ , 反应的基本类型为_____ 。
(3)“操作 a”的名称是_____ 。本流程中可以循环利用的物质(水除外)是_____ (写化学式)。
(4)可用“水洗”的原因是_________ ,“醇洗”的目的是_____ 。
(5)160g CuSO4与足量NaCl 经上述制备流程,可生成的 CuCl 最多是_____ g。

(1)“滤液 1”中除了Na+、SO42-外,还存在较多的离子是
(2)“反应”中发生的化学变化是 2CuCl2+Na2SO3=2CuCl
 +2NaCl+SO3
+2NaCl+SO3 ,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为
,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为(3)“操作 a”的名称是
(4)可用“水洗”的原因是
(5)160g CuSO4与足量NaCl 经上述制备流程,可生成的 CuCl 最多是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】如图1所示为粗盐提纯实验的部分操作。请回答下列问题:_______ (填字母)。
(2)改正操作后,粗盐提纯的正确操作顺序为_______ (填字母)。
(3)操作B中,玻璃棒的作用是_______ 。
(4)操作C中要将圆形滤纸折叠处理,图2步骤中,不该出现的是_______ (填字母)。
(5)操作D中称取10.0g粗盐,将该粗盐逐渐加入到盛有10mL水的烧杯中,边加边用玻璃棒搅拌,直到粗盐不再溶解为止,称得未溶解的粗盐的质量为2.0g,最终得到精盐的质量为6.4g,该实验精盐的产率是_______ 。
(6)制得精盐的产率偏低,可能的原因是_____(多选,填字母)。

(2)改正操作后,粗盐提纯的正确操作顺序为
(3)操作B中,玻璃棒的作用是
(4)操作C中要将圆形滤纸折叠处理,图2步骤中,不该出现的是
(5)操作D中称取10.0g粗盐,将该粗盐逐渐加入到盛有10mL水的烧杯中,边加边用玻璃棒搅拌,直到粗盐不再溶解为止,称得未溶解的粗盐的质量为2.0g,最终得到精盐的质量为6.4g,该实验精盐的产率是
(6)制得精盐的产率偏低,可能的原因是_____(多选,填字母)。
| A.过滤时滤纸有破损 | B.蒸发时有液体溅出 |
| C.所得精盐比较潮湿 | D.过滤时未进行洗涤操作 |
您最近一年使用:0次




