无水氯化镁是制备某种催化剂的中间体。某研究性学习小组设计实验方案进行制取无水氯化镁等实验。请填写下列空白。
(1)[实验一]
利用下图实验装置(夹持和加热装置省略) , 在HCl气流中小心加热MgCl2. 6H2O晶体制取无水氯化镁(无水氯化镁易吸水)。烧瓶中发生的反应为: 。
。
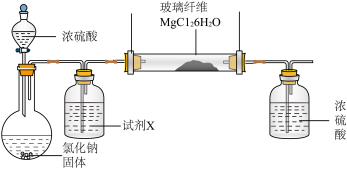
①试剂X是____ 。第二个洗气瓶中的浓硫酸的作用是_____ 。
②该实验装置存在一个缺陷是___ 。
(2)[实验二]
通过下列步骤,测定实验一所得产物中氯元素含量以确定产物是否含有结晶水:
称取m1 g样品置于烧杯中,充分溶解;加入足量硝酸银溶液,充分反应后,过滤;洗涤沉淀,干燥至恒重,称得沉淀质量为m2 g。
①若步骤③的操作中未洗涤沉淀,将导致测得的氯元素含量___ ( 填“偏高”或“偏低”)。
②若测得m1=10.40,m2=28.70,则所得产品MgCl2.nH2O中n的值为___ 。
(3)[实验三]
一定条件下,氯化镁与四氯化钛的混合物可作烯烃聚合反应的催化剂。为了探究温度、氯化镁固体的含水量以及粉碎方式对该催化剂催化效果的影响,设计如下对比实验:
注:催化效果用单位时间内每克催化剂得到产品的质量来表示
①表中ω=_____ 。
②从实验1、2可以得出的结论是_______ 。
③设计实验2、3的目的是___ 。
(1)[实验一]
利用下图实验装置(夹持和加热装置省略) , 在HCl气流中小心加热MgCl2. 6H2O晶体制取无水氯化镁(无水氯化镁易吸水)。烧瓶中发生的反应为:
 。
。
①试剂X是
②该实验装置存在一个缺陷是
(2)[实验二]
通过下列步骤,测定实验一所得产物中氯元素含量以确定产物是否含有结晶水:
称取m1 g样品置于烧杯中,充分溶解;加入足量硝酸银溶液,充分反应后,过滤;洗涤沉淀,干燥至恒重,称得沉淀质量为m2 g。
①若步骤③的操作中未洗涤沉淀,将导致测得的氯元素含量
②若测得m1=10.40,m2=28.70,则所得产品MgCl2.nH2O中n的值为
(3)[实验三]
一定条件下,氯化镁与四氯化钛的混合物可作烯烃聚合反应的催化剂。为了探究温度、氯化镁固体的含水量以及粉碎方式对该催化剂催化效果的影响,设计如下对比实验:
| 实验序号 | 氯化镁固体中氯元素含量/% | 温度/°C | 粉碎方式 | 催化效果/g.g-1 |
| 1 | 70.97 | 20 | 滚动球磨 |  |
| 2 | 74.45 | 20 | 滚动球磨 |  |
| 3 | 74.45 | 20 | 振动球磨 |  |
| 4 | ω | 100 | 振动球磨 |
①表中ω=
②从实验1、2可以得出的结论是
③设计实验2、3的目的是
更新时间:2020-05-03 09:44:07
|
相似题推荐
【推荐1】下图是实验室常用的实验仪器与装置,根据所学知识回答下列问题:

(1)仪器a的名称是_____ 。
(2)实验室用A装置制取氧气的化学方程式是__ ,收集较纯净的氧气可选用的装置是____ (填装置序号)。
(3)实验室常用B装置和______ 装置组合制取二氧化碳,反应的化学方程式是_____ 。
(4)小龙同学利用吃完的碎碎冰饮料包装袋设计了图F的发生装置来代替B装置制取氢气,其优点是______ ,他要制取并收集干燥的氢气,下列装置的连接顺序正确的是:___ (填序号)。

(5)小露同学利用草酸钠固体(化学式为Na2C2O4)加热分解制取一氧化碳,并用C还原氧化铁。他设计的实验装置图如下:

①一氧化碳的发生装置可以选择上述所给装置中的____ (填序号);
②硬质玻璃管中的反应现象是________ ;
③该装置中锥形瓶(足量澄清石灰水)的作用是:
Ⅰ.检验并吸收生成的CO2;Ⅱ.________ 。

(1)仪器a的名称是
(2)实验室用A装置制取氧气的化学方程式是
(3)实验室常用B装置和
(4)小龙同学利用吃完的碎碎冰饮料包装袋设计了图F的发生装置来代替B装置制取氢气,其优点是

| A.b→c→d | B.b→c→e |
| C.c→b→d | D.c→b→e |

①一氧化碳的发生装置可以选择上述所给装置中的
②硬质玻璃管中的反应现象是
③该装置中锥形瓶(足量澄清石灰水)的作用是:
Ⅰ.检验并吸收生成的CO2;Ⅱ.
您最近一年使用:0次
【推荐2】下列A~F是初中化学中的六个实验装置,请按要求填空:

(1)A实验试管2中产生的气体是_____ 。
(2)B实验中烧杯③的作用是_____ 。
(3)对于C实验,下列操作不妥的是_____ 。
①红磷要足量 ②实验前夹紧止水夹 ③冷却后再打开止水夹 ④用木炭代替红磷
(4)若用D装置除去O2中的水蒸气,该液体试剂为_____ 。
(5)E实验中,气球的变化情况是_____ 。写出导致气球变化的化学方程式 _____ 。

(1)A实验试管2中产生的气体是
(2)B实验中烧杯③的作用是
(3)对于C实验,下列操作不妥的是
①红磷要足量 ②实验前夹紧止水夹 ③冷却后再打开止水夹 ④用木炭代替红磷
(4)若用D装置除去O2中的水蒸气,该液体试剂为
(5)E实验中,气球的变化情况是
您最近一年使用:0次
实验题
|
较难
(0.4)
解题方法
【推荐1】某品牌纯碱中含有少量氯化钠.某化学探究小组欲测定该品牌纯碱的纯度(即碳酸钠的质量分数)。
Ⅰ.甲组同学设计如图所示实验:

【实验步骤】①组装好如图仪器,并_____ ;
②称取7.0g样品放入锥形瓶中,加入少量蒸馏水溶解,并在其他装置中加入相应的药品;
③称量装置C的质量;
④打开分液漏斗旋塞滴入稀硫酸,直到不再产生气泡为止;
⑤再次称量装置C 的总质量; ⑥计算出样品中碳酸钠的质量分数。
【实验分析】(1)A装置中反应的化学方程式为______________ ;
(2)B装置的作用是__________ ;
(3)如果没有D装置则所测样品中碳酸钠的质量分数偏大的原因是_________ ;
(4)称得纯碱样品的质量为7.0g,实验前、后C装置(包含药品)的质量分别为61.2g和63.4g,则该纯碱样品的纯度为________ (计算结果精确到0.1%)。
Ⅱ.乙组同学采用生成沉淀的方法来测定样品中纯碱的质量分数,设计了如下实验:

(1)判断加入氯化钡溶液是否过量的合适方法是______ (填编号),然后观察现象判断。
A.向混合物X中滴加稀硫酸,若有白色沉淀生成则说明氯化钡已经过量
B.静置混合物X,向上层清液中继续滴加氯化钡溶液,若无白色沉淀生成,则氯化钡已经过量
(2)判断滤渣是否洗涤干净,可以采取向最后的洗出液中滴加__________ ,然后观察现象判断。
(3)根据实验数据,乙组测得样品中碳酸钠的质量分数为______ (写出计算过程,计算结果精确到0.1%)。
【实验反思】乙组所测实验数据比甲组更准确,你认为甲组存在较大偏差的原因可能是________________ 。
Ⅰ.甲组同学设计如图所示实验:

【实验步骤】①组装好如图仪器,并
②称取7.0g样品放入锥形瓶中,加入少量蒸馏水溶解,并在其他装置中加入相应的药品;
③称量装置C的质量;
④打开分液漏斗旋塞滴入稀硫酸,直到不再产生气泡为止;
⑤再次称量装置C 的总质量; ⑥计算出样品中碳酸钠的质量分数。
【实验分析】(1)A装置中反应的化学方程式为
(2)B装置的作用是
(3)如果没有D装置则所测样品中碳酸钠的质量分数偏大的原因是
(4)称得纯碱样品的质量为7.0g,实验前、后C装置(包含药品)的质量分别为61.2g和63.4g,则该纯碱样品的纯度为
Ⅱ.乙组同学采用生成沉淀的方法来测定样品中纯碱的质量分数,设计了如下实验:

(1)判断加入氯化钡溶液是否过量的合适方法是
A.向混合物X中滴加稀硫酸,若有白色沉淀生成则说明氯化钡已经过量
B.静置混合物X,向上层清液中继续滴加氯化钡溶液,若无白色沉淀生成,则氯化钡已经过量
(2)判断滤渣是否洗涤干净,可以采取向最后的洗出液中滴加
(3)根据实验数据,乙组测得样品中碳酸钠的质量分数为
【实验反思】乙组所测实验数据比甲组更准确,你认为甲组存在较大偏差的原因可能是
您最近一年使用:0次
实验题
|
较难
(0.4)
解题方法
【推荐2】实验小组对久置生石灰的成分进行分析,实验操作及部分现象如图所示。

回答下列问题:
(1)若滤渣属于混合物,则滤渣的成分是______ ;
(2)样品加水放热,有关化学方程式是______ ;
(3)③中的实验现象是______ ;
(4)将混合物B、C、D倒入同一个洁净的烧杯中,发现烧杯中有白色沉淀且上层清液呈红色,过滤,得到滤液和滤渣,向滤液E中滴加过量氯化钙溶液,观察到产生白色沉淀,溶液呈红色,则滤液E中的一定含有的溶质是______ 。

回答下列问题:
(1)若滤渣属于混合物,则滤渣的成分是
(2)样品加水放热,有关化学方程式是
(3)③中的实验现象是
(4)将混合物B、C、D倒入同一个洁净的烧杯中,发现烧杯中有白色沉淀且上层清液呈红色,过滤,得到滤液和滤渣,向滤液E中滴加过量氯化钙溶液,观察到产生白色沉淀,溶液呈红色,则滤液E中的一定含有的溶质是
您最近一年使用:0次
实验题
|
较难
(0.4)
解题方法
【推荐3】化学是一门以实验为基础的科学,实验是科学探究的重要手段。下图所示实验,为了探究常见酸碱中和反应。

(1)方案1:通过反应发生的直接现象,证明酸与碱发生中和反应。
探究一:向图中氢氧化铜悬浊液中滴加稀硫酸,振荡并观察现象。可以作为证明稀硫酸和氢氧化铜发生反应的现象是______ 。
(2)方案2:通过间接现象,经推理证明酸与碱发生中和反应。
探究二:向图①稀硫酸中滴加碳酸钠溶液;向图②稀硫酸中滴加足量氢氧化钠溶液,充分反应后再滴加碳酸钠溶液如图③。图③中的现象是________ ,结合图①和图③中的现象说明_______ 。
(3)方案3:通过溶液中微观粒子变化证明酸与碱发生中和反应。
探究三:如图④所示,向氢氧化钠溶液中滴加稀硫酸,边滴边振荡,并测量pH变化绘制曲线如图⑤。
i.图⑤曲线显示随着将40g稀硫酸溶液逐渐加入,试管内的溶液PH逐渐减少,请分析图中曲线变化的本质:_______ 。
ⅱ.图⑤冲c、d两点所对应溶液所含溶质Na2SO4的质量大小关系是_______ 。
ⅲ.向图⑤d点所对应的溶液中滴加足量硝酸钡溶液,已知所用稀硫酸的溶质质量分数为4.9%,则生成的沉淀质量为_______ (结果可用比例式表示)。

(1)方案1:通过反应发生的直接现象,证明酸与碱发生中和反应。
探究一:向图中氢氧化铜悬浊液中滴加稀硫酸,振荡并观察现象。可以作为证明稀硫酸和氢氧化铜发生反应的现象是
(2)方案2:通过间接现象,经推理证明酸与碱发生中和反应。
探究二:向图①稀硫酸中滴加碳酸钠溶液;向图②稀硫酸中滴加足量氢氧化钠溶液,充分反应后再滴加碳酸钠溶液如图③。图③中的现象是
(3)方案3:通过溶液中微观粒子变化证明酸与碱发生中和反应。
探究三:如图④所示,向氢氧化钠溶液中滴加稀硫酸,边滴边振荡,并测量pH变化绘制曲线如图⑤。
i.图⑤曲线显示随着将40g稀硫酸溶液逐渐加入,试管内的溶液PH逐渐减少,请分析图中曲线变化的本质:
ⅱ.图⑤冲c、d两点所对应溶液所含溶质Na2SO4的质量大小关系是
ⅲ.向图⑤d点所对应的溶液中滴加足量硝酸钡溶液,已知所用稀硫酸的溶质质量分数为4.9%,则生成的沉淀质量为
您最近一年使用:0次




