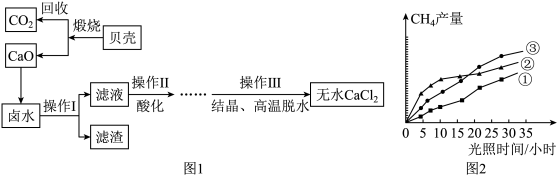
厦门是沿海城市,海水中蕴藏着丰富的资源,开发海水资源前景广阔.探究学习小组以含有Ca2+,Mg2+,Cl﹣离子的卤水和贝壳(主要成分为CaCO3)为主要原料在实验室制备无水CaCl2,流程如图1:
(1)操作Ⅰ的名称:__ .
(2)操作Ⅱ酸化时应选择的酸是__ (填写化学式).
(3)以MgCl2为例写出卤水中除去Mg2+时发生反应的化学方程式__ .
(4)回收的CO2在紫外线照射和催化剂作用下能与水蒸气反应,生成CH4和O2,该反应的化学方程式为__ ,紫外线照射时,在不同催化剂(①、②、③)的作用下,CH4产量随光照时间的变化如图2所示,在第10小时时CH4产量最高的是__ (填写“①”、“②”或“③”).

(1)操作Ⅰ的名称:
(2)操作Ⅱ酸化时应选择的酸是
(3)以MgCl2为例写出卤水中除去Mg2+时发生反应的化学方程式
(4)回收的CO2在紫外线照射和催化剂作用下能与水蒸气反应,生成CH4和O2,该反应的化学方程式为
更新时间:2020-05-08 16:35:58
|
相似题推荐
填空与简答-流程题
|
较易
(0.85)
解题方法
【推荐1】工业上以粗盐(含少量MgCl2、CaCl2杂质)为原料,利用电解饱和食盐水的方法制备NaOH,其简要工艺流程如下:

(1)步骤①中发生反应生成的沉淀是_____ (填化学式)。
(2)步骤③中加入适量稀盐酸的目的是_____ 。
(3)验证步骤②中CaCl2已完全转化为CaCO3的方法是_____ 。
(4)写出步骤④中反应的化学方程式:_____ 。

(1)步骤①中发生反应生成的沉淀是
(2)步骤③中加入适量稀盐酸的目的是
(3)验证步骤②中CaCl2已完全转化为CaCO3的方法是
(4)写出步骤④中反应的化学方程式:
您最近一年使用:0次
【推荐2】海水晒盐得到的粗盐中含有多种可溶性杂质(氯化镁、氯化钙、硫酸钠等)和泥沙等。提纯的流程如图所示:______ 。
(2)加入过量氢氧化钠溶液时发生反应的化学方程式为______ 。
(3)若A为氯化钡溶液,则加入B溶液的目的是除去______ (填离子符号)。

(2)加入过量氢氧化钠溶液时发生反应的化学方程式为
(3)若A为氯化钡溶液,则加入B溶液的目的是除去
您最近一年使用:0次




