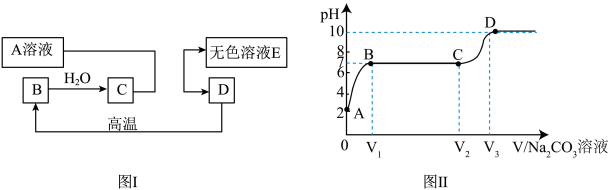
I中 A、B、C、D、E 为中学常见的物质,其中 A 为含钠元素的化合物,D 的相对分子质量为 100,E 溶液为无色,它们的相互转化的关系如图Ⅰ所示。小玉同学测得D 与稀盐酸反应后的溶液 pH 为 2,向适量该溶液中逐滴加入碳酸钠溶液,并测得溶液的 pH随加入碳酸钠溶液体积的变化曲线如图Ⅱ所示(此处的 A、B、C、D 均为曲线上的点),请回答下列问题:
请填写下列空白
(1)A:_____ C:_____
(2)图Ⅱ中,A 点处溶液中含有的主要离子有_____ (写离子符号);
(3)BC 段发生反应的化学方程式是________________ ;

请填写下列空白
(1)A:
(2)图Ⅱ中,A 点处溶液中含有的主要离子有
(3)BC 段发生反应的化学方程式是
更新时间:2020-05-10 11:39:46
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】现有两瓶失去标签的无色溶液,其中一瓶是氢氧化钙溶液,一瓶是稀盐酸。为了鉴别它们,同学们分别取少量溶液加到甲和乙两支试管中。进行如下实验。
(1)小强同学向两支试管分别加入碳酸钠溶液(如图)。

甲试管出现_______ (填实验现象),则甲溶液为氢氧化钙溶液;写出乙试管中反应的化学方程式:_________ 。
(2)实验结束后,小明同学进一步完成了下图所示的探究,他将滤液M和废液N混合,有气泡产生,完全反应后得到混合物Q。

①废液N的pH______ 7(填“>”“<”或“=”)。
②混合物Q的溶质组成有______ 种情况(不考虑二氧化碳溶于水等特殊情况)。
(1)小强同学向两支试管分别加入碳酸钠溶液(如图)。

甲试管出现
(2)实验结束后,小明同学进一步完成了下图所示的探究,他将滤液M和废液N混合,有气泡产生,完全反应后得到混合物Q。

①废液N的pH
②混合物Q的溶质组成有
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
【推荐2】了解物质的组成和结构,有助于认识物质的性质和变化。

(1)图甲表示核电荷数为11~17的元素最高和最低化合价和原子的最外层电子数。
①若某元素既可显正价,又可显负价,则最高正价与最低负价绝对值的代数和为_____ 。硫元素既可显正价,又可显负价,硫元素与钠元素形成的化合物由 _____ (填“分子”、“原子”或“离子”)构成,其化学式为 _____ 。
②铝原子失去最外层电子所形成的离子符号为_____ 。
③写出图中元素的化合价与最外层电子数有关的一条规律_____ 。
(2)将NaOH、KCl、MgCl2三种溶液按一定比例混合,微观变化情况如图乙。

①图中OH-的名称是_____ 。
②该反应的本质是_____ 结合生成沉淀。
③写出与上述反应本质相同的另一反应的化学方程式:_____ (反应物之一为MgCl2)。

(1)图甲表示核电荷数为11~17的元素最高和最低化合价和原子的最外层电子数。
①若某元素既可显正价,又可显负价,则最高正价与最低负价绝对值的代数和为
②铝原子失去最外层电子所形成的离子符号为
③写出图中元素的化合价与最外层电子数有关的一条规律
(2)将NaOH、KCl、MgCl2三种溶液按一定比例混合,微观变化情况如图乙。

①图中OH-的名称是
②该反应的本质是
③写出与上述反应本质相同的另一反应的化学方程式:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】我国航天员使用的“飞天”舱外服是目前世界上最先进的航天服之一、学习小组同学模仿航天服的外形,建立了如图所示常见物质类别之间化学反应的思维导图。

(1)反应①中遇酸变色的指示剂是___________ 。
(2)若图中金属氧化物为一种红棕色固体,则反应③在生产生活中的应用是___________ 。
(3)写出符合反应⑨的一个化学反应方程式:___________
(4)图中反应①~⑦中属于复分解反应的有___________ 个。

(1)反应①中遇酸变色的指示剂是
(2)若图中金属氧化物为一种红棕色固体,则反应③在生产生活中的应用是
(3)写出符合反应⑨的一个化学反应方程式:
(4)图中反应①~⑦中属于复分解反应的有
您最近一年使用:0次
【推荐2】KNO3和K2CO3的溶解度曲线如下表。
(1)KNO3和K2CO3的溶解度受温度影响较大的是_______________ 。
(2)某KNO3样品中含有少量K2CO3,为提纯KNO3,化学实验小组的同学取一定质量的固体样品,进行了如图所示的实验。_______________ 。
②溶液C是KNO3的_______________ (填“饱和”或“不饱和”)溶液。
③依据题目信息,_______________ (填“能”或“不能”)算出样品中KNO3的质量。
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 100 |
| K2CO3 | 110 | 114 | 117 | 121 | 126 | |
(1)KNO3和K2CO3的溶解度受温度影响较大的是
(2)某KNO3样品中含有少量K2CO3,为提纯KNO3,化学实验小组的同学取一定质量的固体样品,进行了如图所示的实验。

②溶液C是KNO3的
③依据题目信息,
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
名校
【推荐3】海水是名符其实的液体矿产,平均每立方公里的海水中有3570万吨的矿物质,世界上已知的 100 多种元素中,80%已经在海水中找到。海水是盐的“故乡”,海水中含有各种盐类,其中90%左右是氯化钠,也就是食盐。另外还含有MgCl2、MgSO4、CaCl2、KI及NaBr等各种盐类。氯化镁是点豆腐用的卤水的主要成分,味道是苦的,因此,海水晒盐后所得的母液中含有较多的氯化镁,也叫“苦卤”。根据上述阅读材料回答问题:
(1)海水中含有的阴离子包括Cl-、SO42-及_____ (写出一种微粒符号即可)等;
(2)苦卤中的溶质主要有:氯化镁、金属溴化物和_______ (写出一种物质);
(3)工业上把苦卤除钙后,再加入碱性沉淀剂可以制备氢氧化镁。若海水中钙离子含量太高,氢氧化钙会存在于氢氧化镁颗粒中,从而影响氢氧化镁的纯净度。某研究小组在控制反应温度是20~25℃和浓海水质量为1109g不变的条件下,进行下述对比实验,数据如下:
①该对比实验中发生反应的化学方程式是_____ ;
②进行实验a和b的目的是__________ 。
③该实验显示________ (填实验因素)对钙的除去率的影响很小;
④搅拌速率越快,反应时间越长则消耗能源越多。为了节约能源,获得较高的钙除去率,进一步优化“搅拌速率”和“反应时间”的反应条件。在其他实验条件不变情况下,设计对比实验,你应选择的反应条件是_____ (填选项)。
A 200r/min,3.5h B 200r/min,4.5h
C 175 r/min,4h D 225 r/min,4h
(1)海水中含有的阴离子包括Cl-、SO42-及
(2)苦卤中的溶质主要有:氯化镁、金属溴化物和
(3)工业上把苦卤除钙后,再加入碱性沉淀剂可以制备氢氧化镁。若海水中钙离子含量太高,氢氧化钙会存在于氢氧化镁颗粒中,从而影响氢氧化镁的纯净度。某研究小组在控制反应温度是20~25℃和浓海水质量为1109g不变的条件下,进行下述对比实验,数据如下:
| 实验 | 碳酸钠加入量/g | 搅拌速度 r/min | 反应时间/h | 钙除去率/% |
| a | 1.78 | 200 | 3 | 44.8 |
| b | 2.32 | 200 | 3 | 60.2 |
| c | 2.32 | 125 | 4 | 55.1 |
| d | 2.32 | 200 | 4 | 64.6 |
①该对比实验中发生反应的化学方程式是
②进行实验a和b的目的是
③该实验显示
④搅拌速率越快,反应时间越长则消耗能源越多。为了节约能源,获得较高的钙除去率,进一步优化“搅拌速率”和“反应时间”的反应条件。在其他实验条件不变情况下,设计对比实验,你应选择的反应条件是
A 200r/min,3.5h B 200r/min,4.5h
C 175 r/min,4h D 225 r/min,4h
您最近一年使用:0次

 CaO + CO2↑)
CaO + CO2↑)


