我国某科研团队以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料,制取高纯碳酸锰,工艺流程如下图:

已知:①SiO2不溶于水,不与稀H2SO4、SO2反应;②MnO2能将Fe2+氧化成Fe3+;③溶液中的Fe3+在 pH 大于或等于 3.2 时将完全转化为Fe(OH)3沉淀。
请回答:(1)滤渣Ⅰ、Ⅱ分别为_____ 、_____ (写化学式) ;
(2)浸锰过程中发生了 2 个化学反应,其中一个为Fe2O3与SO2反应,该反应的化学方 程式为Fe2O3+ SO2+H2SO4=2FeSO4+ H2O,另一个为MnO2和SO2按化学计量数为 1:1 发生化合反应,请写出该反应的化学方程式:_____ , 该反应中共有_____ 种元素的化合价发生了改变。
(3)“沉锰”:加入NH4HCO3溶液后,生成了 4 种产物,其中含有MnCO3沉淀和某种气 体,写出该反应的化学方程式:_____ 。
(4)取所得的高纯MnCO311.7g溶于足量的盐酸中,将产生的气体用足量的Ba(OH)2浓 溶液吸收,得到白色沉淀 19.7g,则所得产品的纯度为_____ %(保留一位小数)
(5)某研究小组用稀H2SO4与菱锰矿(含有MnCO3)反应来浸出Mn2+,该研究小组选 定两个因素作为研究条件进行对比实验,数据如下:
表中 X 最有可能的数值为_____ 。
a.79.7 b.80.8 c.87.6 d.92.8

已知:①SiO2不溶于水,不与稀H2SO4、SO2反应;②MnO2能将Fe2+氧化成Fe3+;③溶液中的Fe3+在 pH 大于或等于 3.2 时将完全转化为Fe(OH)3沉淀。
请回答:(1)滤渣Ⅰ、Ⅱ分别为
(2)浸锰过程中发生了 2 个化学反应,其中一个为Fe2O3与SO2反应,该反应的化学方 程式为Fe2O3+ SO2+H2SO4=2FeSO4+ H2O,另一个为MnO2和SO2按化学计量数为 1:1 发生化合反应,请写出该反应的化学方程式:
(3)“沉锰”:加入NH4HCO3溶液后,生成了 4 种产物,其中含有MnCO3沉淀和某种气 体,写出该反应的化学方程式:
(4)取所得的高纯MnCO311.7g溶于足量的盐酸中,将产生的气体用足量的Ba(OH)2浓 溶液吸收,得到白色沉淀 19.7g,则所得产品的纯度为
(5)某研究小组用稀H2SO4与菱锰矿(含有MnCO3)反应来浸出Mn2+,该研究小组选 定两个因素作为研究条件进行对比实验,数据如下:
矿酸比 | 温度/(℃) | 浸出率/(%) | |
1 | 1:0.5 | 60 | 80.2 |
2 | 1:0.5 | 80 | 83.8 |
3 | 1:0.6 | 60 | X |
4 | 1:0.6 | 80 | 91.8 |
a.79.7 b.80.8 c.87.6 d.92.8
更新时间:2020-06-04 09:16:05
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】氧化镁是医疗上的一种常用药剂,通常与氢氧化铝合用,主要用于治疗伴有便秘的胃酸过多等症,以镁矿石(主要成分MgCO3、SiO2)为原料生产氧化镁的工艺流程如图所示。已知SiO2难溶于水和常见的酸。


(1)酸浸前将镁矿石粉碎的目的是______ 。
(2)操作1的名称是______ ,滤渣X的主要成分是______ 。
(3)“沉镁”过程中硫酸镁与氨水( )发生复分解反应,生成物中有氢氧化镁沉淀,请写出此反应的化学方程式
)发生复分解反应,生成物中有氢氧化镁沉淀,请写出此反应的化学方程式______ 。
(4)请写出副产品Y的一种用途______ 。
(5)已知在不同温度下,充分加热等质量的氢氧化镁,加热温度与固体残留率的关系如图2所示,加热时温度至少要达到350℃,原因是______ 。


(1)酸浸前将镁矿石粉碎的目的是
(2)操作1的名称是
(3)“沉镁”过程中硫酸镁与氨水(
 )发生复分解反应,生成物中有氢氧化镁沉淀,请写出此反应的化学方程式
)发生复分解反应,生成物中有氢氧化镁沉淀,请写出此反应的化学方程式(4)请写出副产品Y的一种用途
(5)已知在不同温度下,充分加热等质量的氢氧化镁,加热温度与固体残留率的关系如图2所示,加热时温度至少要达到350℃,原因是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐2】金属材料在我国建设中起着重要的作用。
(1)铜可以做导线,主要利用了金属铜的延展性和___________ ;
(2)回收利用是保护金属资源的一条有效途径。某工业废料含氧化铜和氧化铁,经过处理后可得到铜和硫酸亚铁溶液,已知:Fe Fe2(SO4)3
Fe2(SO4)3 3FeSO4。
3FeSO4。

①过程I中氧化铁发生反应的化学方程式为_________________________ ;
②过程II、III充分反应后,还应有的实验操作是________________ ;
③过程III的反应除溶液颜色变化外,还能观察到_____________________________ ;
④A~E中含铁元素的有______________ (填序号)。
(1)铜可以做导线,主要利用了金属铜的延展性和
(2)回收利用是保护金属资源的一条有效途径。某工业废料含氧化铜和氧化铁,经过处理后可得到铜和硫酸亚铁溶液,已知:Fe
 Fe2(SO4)3
Fe2(SO4)3 3FeSO4。
3FeSO4。
①过程I中氧化铁发生反应的化学方程式为
②过程II、III充分反应后,还应有的实验操作是
③过程III的反应除溶液颜色变化外,还能观察到
④A~E中含铁元素的有
您最近一年使用:0次
【推荐3】抗“疫”期间,酒精发挥了至关重要的作用。
(1)居家消毒时不要喷洒高浓度酒精,因为挥发出的酒精蒸气遇到明火易发生燃烧和爆炸。从燃烧的条件分析,明火的作用是:_______________ ;
(2)等质量的①氢气②碳单质③一氧化碳在空气中完全燃烧,消耗氧气质量由大到小的顺序为______________ (填序号)。在一定条件下,6.4g甲烷与一定质量的氧气恰好完全反应,生成14.4g的水,5.6gCO和8.8gCO2,需要消耗氧气的质量为_______________ g,则该反应的化学方程式为_______________ 。
(1)居家消毒时不要喷洒高浓度酒精,因为挥发出的酒精蒸气遇到明火易发生燃烧和爆炸。从燃烧的条件分析,明火的作用是:
(2)等质量的①氢气②碳单质③一氧化碳在空气中完全燃烧,消耗氧气质量由大到小的顺序为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】将12克CO和CO2的混合气体通过足量灼热的氧化铜后,得到气体的总量为18克,原混合气体中CO的质量分数为______ 。
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】金属和金属材料在生产、生活中应用广泛。
(1)日常生活中常用铝合金制作门窗而不用纯铝制作门窗。请写出铝合金门窗相比纯铝门窗具有的一个优点_________ 。
(2)实验室某废液缸内含硝酸银和硝酸铜两种溶质,某同学欲分别回收银和铜,进行了如下实验。
步骤Ⅰ:向废液中加入适量的金属A粉末,充分反应后过滤,得到银和滤液1。
步骤Ⅱ:向滤液1中加入适量的金属B粉末,充分反应后过滤,得到铜和滤液2。
①写出步骤Ⅰ中发生反应的化学方程式_________ 。
②若滤液2的质量大于滤液1,则金属B是________ ;请写出加入B后的实验现象_________ 。
(3)某兴趣小组同学为了探究金属与酸反应的规律,进行了如下实验:取等量、形状相同的铁片、镁片,分别与足量、等浓度的稀盐酸反应,用温度传感器测定的溶液温度变化曲线如图所示。
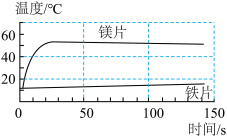
①写出铁与稀盐酸反应的化学方程式_________ 。
②请分析反应中溶液温度升高的原因_________ 。
③根据所学知识及曲线图写出镁与稀盐酸反应时的现象_________ 。
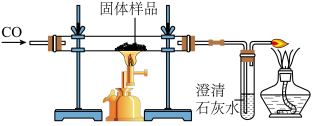
(4)该小组的同学对某生锈铁钉样品(只含氧化铁和铁单质)中铁单质的含量进行测定。称取13.6 g样品研磨成粉末,用如图所示的装置进行实验,充分反应后称得剩余固体的质量为11.2 g。计算原样品中铁单质的质量分数。(结果保留至0.1%)
(1)日常生活中常用铝合金制作门窗而不用纯铝制作门窗。请写出铝合金门窗相比纯铝门窗具有的一个优点
(2)实验室某废液缸内含硝酸银和硝酸铜两种溶质,某同学欲分别回收银和铜,进行了如下实验。
步骤Ⅰ:向废液中加入适量的金属A粉末,充分反应后过滤,得到银和滤液1。
步骤Ⅱ:向滤液1中加入适量的金属B粉末,充分反应后过滤,得到铜和滤液2。
①写出步骤Ⅰ中发生反应的化学方程式
②若滤液2的质量大于滤液1,则金属B是
(3)某兴趣小组同学为了探究金属与酸反应的规律,进行了如下实验:取等量、形状相同的铁片、镁片,分别与足量、等浓度的稀盐酸反应,用温度传感器测定的溶液温度变化曲线如图所示。

①写出铁与稀盐酸反应的化学方程式
②请分析反应中溶液温度升高的原因
③根据所学知识及曲线图写出镁与稀盐酸反应时的现象
(4)该小组的同学对某生锈铁钉样品(只含氧化铁和铁单质)中铁单质的含量进行测定。称取13.6 g样品研磨成粉末,用如图所示的装置进行实验,充分反应后称得剩余固体的质量为11.2 g。计算原样品中铁单质的质量分数。(结果保留至0.1%)

您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
解题方法
【推荐3】过氧化钙晶体(CaO2·8H2O)较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒。以贝壳为原料制备CaO2流程如下:

(1)气体X是CO2,其名称是__________ ;将过氧化钙晶体与溶液分离的方法是_____ 。
(2)反应Y需控制温度在0~5℃,可将反应容器放在__________ 中,该反应是化合反应,反应产物是CaO2·8H2O,请写出化学方程式______________________ 。获得的过氧化钙晶体中常含有Ca(OH)2杂质,原因是_________________________ 。
(3)CaO2的相对分子质量为______ ,过氧化钙晶体(CaO2·8H2O)中H、O元素的质量比为________ 。
(4)为测定制得的过氧化钙晶体中CaO2·8H2O的质量分数,设计的实验如下:称取晶体样品50g,加热到220℃充分反应(方程式为 ,杂质不发生变化),测得生成氧气的质量为3.2g,请计算样品中CaO2·8H2O的质量分数
,杂质不发生变化),测得生成氧气的质量为3.2g,请计算样品中CaO2·8H2O的质量分数________ (CaO2·8H2O相对分子质量为216),写出必要的计算过程。

(1)气体X是CO2,其名称是
(2)反应Y需控制温度在0~5℃,可将反应容器放在
(3)CaO2的相对分子质量为
(4)为测定制得的过氧化钙晶体中CaO2·8H2O的质量分数,设计的实验如下:称取晶体样品50g,加热到220℃充分反应(方程式为
 ,杂质不发生变化),测得生成氧气的质量为3.2g,请计算样品中CaO2·8H2O的质量分数
,杂质不发生变化),测得生成氧气的质量为3.2g,请计算样品中CaO2·8H2O的质量分数
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】天然气中常含有少量H2S。脱硫是资源利用和环境保护的重要研究课题。
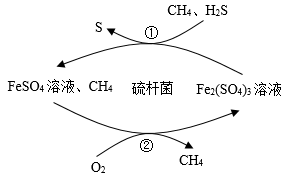
(1)生物脱H2S。反应的原理如图所示:
①该脱硫过程在_______ 条件下进行(填“酸性”或“碱性”)。
②硫杆菌存在时,FeSO4与氧气反应的速度是无菌时的5×105的倍,该菌的作用是_______ 。依据图1和图2判断,使用硫杆菌的最适宜条件为_______ 。若温度过高,反应速度下降,其可能原因是_______ 。


(2)H2O2脱H2S。随着参加反应的分子数之比【N(H2O2):N(H2S)】变化,反应产物发生变化。当N(H2O2):N(H2S)=4:1时,除生成H2O外,另一种产物的分子式为_______ 。
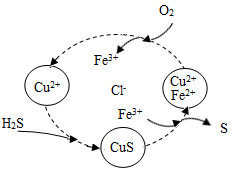
(3)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如下图所示。其中化合价不变的元素是_______ (填元素符号)。
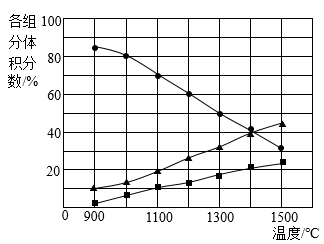
(4)高温分解H2S生成硫蒸气和H2.若在不同温度下反应足够长的时间,混合气体中各组分的体积分数(即各组分所占气体分子个数百分比)如图所示,则H2S在高温下分解反应的化学方程式为_______ 。

(1)生物脱H2S。反应的原理如图所示:
①该脱硫过程在
②硫杆菌存在时,FeSO4与氧气反应的速度是无菌时的5×105的倍,该菌的作用是


(2)H2O2脱H2S。随着参加反应的分子数之比【N(H2O2):N(H2S)】变化,反应产物发生变化。当N(H2O2):N(H2S)=4:1时,除生成H2O外,另一种产物的分子式为
(3)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如下图所示。其中化合价不变的元素是

(4)高温分解H2S生成硫蒸气和H2.若在不同温度下反应足够长的时间,混合气体中各组分的体积分数(即各组分所占气体分子个数百分比)如图所示,则H2S在高温下分解反应的化学方程式为

您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】物质丙是重要的化工产品,在国民经济中占有重要地位。工业上用甲和乙合成丙。甲、乙、丙的微观示意图见下表。请完成下列空白。
(1)甲、乙、丙3种物质都是由(填“分子”“原子”或“离子”) _______ 构成的。
(2)甲、乙、丙中属于化合物的是_______ 。
(3)已知物质丙中氢元素的化合价为+1,则另一种元素的化合价为_______ 。
(4)丙中氮、氢元素的质量比为_______ 。
(5)写出甲和乙在高温、高压、催化剂的条件下合成丙的化学方程式:______________ 。
| 物质 | 甲 | 乙 | 丙 |  |
| 微观示意图 |  |  |  |
(2)甲、乙、丙中属于化合物的是
(3)已知物质丙中氢元素的化合价为+1,则另一种元素的化合价为
(4)丙中氮、氢元素的质量比为
(5)写出甲和乙在高温、高压、催化剂的条件下合成丙的化学方程式:
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐3】生产、生活中铝及其合金制品是现代文明不可缺少的物质基础。
I.金属的冶炼
(1)某铝矿石中含氧化铝的质量分数为65%(杂质不含铝),该铝矿石中铝元素的质量分数为______ (结果精确至0.1%)。
(2)近代工业上采用电解熔融氧化铝的方法冶炼铝,分解后得到两种单质,该反应的化学方程式为________ 。
II.金属的性质
(3)向铝中加入不同的金属可以提高其性能,某铝合金中铝的含量约为97%,还含有镁、锰、铁、锢(In)等。打磨后与纯铝片相互刻画,发现仅纯铝片表面有划痕,说明___________ 。
(4)结合如图推测金属铟与铝的化学性质相似,理由是___________ 。实验证明,铟可以与稀盐酸反应,其反应的化学方程式为___________ 。
(5)储氢材料的研发是氢能源技术的关键之一、金属铝可用作储氢材料,储氢后生成氢化铝 ,其释氢原理为氢化铝与水反应释放氢气,同时生成一种碱。
,其释氢原理为氢化铝与水反应释放氢气,同时生成一种碱。
①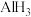 中铝元素的化合价是+3,则氢元素的化合价为
中铝元素的化合价是+3,则氢元素的化合价为___________ 。
②生成的碱的化学式为___________ 。
(6)铝系金属复合材料能有效去除水体中的硝酸盐污染。铝系金属复合材料的组分和含量会影响硝酸盐的去除效果。在相同实验条件下,分别使用纯铝粉和Cu含量为3%、4%、5%的Al/Cu二元金属复合材料对硝酸盐的去除效果如图所示。___________ 。
②Al/Cu二元金属复合材料去除水体中硝酸盐效果优于铝粉,可能的原因是___________ 。
I.金属的冶炼
(1)某铝矿石中含氧化铝的质量分数为65%(杂质不含铝),该铝矿石中铝元素的质量分数为
(2)近代工业上采用电解熔融氧化铝的方法冶炼铝,分解后得到两种单质,该反应的化学方程式为
II.金属的性质
(3)向铝中加入不同的金属可以提高其性能,某铝合金中铝的含量约为97%,还含有镁、锰、铁、锢(In)等。打磨后与纯铝片相互刻画,发现仅纯铝片表面有划痕,说明
(4)结合如图推测金属铟与铝的化学性质相似,理由是

(5)储氢材料的研发是氢能源技术的关键之一、金属铝可用作储氢材料,储氢后生成氢化铝
 ,其释氢原理为氢化铝与水反应释放氢气,同时生成一种碱。
,其释氢原理为氢化铝与水反应释放氢气,同时生成一种碱。①
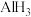 中铝元素的化合价是+3,则氢元素的化合价为
中铝元素的化合价是+3,则氢元素的化合价为②生成的碱的化学式为
(6)铝系金属复合材料能有效去除水体中的硝酸盐污染。铝系金属复合材料的组分和含量会影响硝酸盐的去除效果。在相同实验条件下,分别使用纯铝粉和Cu含量为3%、4%、5%的Al/Cu二元金属复合材料对硝酸盐的去除效果如图所示。

②Al/Cu二元金属复合材料去除水体中硝酸盐效果优于铝粉,可能的原因是
您最近一年使用:0次



