由含铜废料制铜的一种方案是:
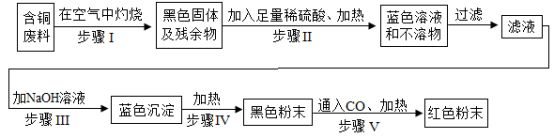
(1)写出下列步骤中的化学方程式:
步骤Ⅲ:_____ 。
步骤V:_____ 。
(2)步骤II后形成的蓝色溶液中的溶质是_____ 。
(3)上述方案中可能造成空气污染的步骤是_____ 。

(1)写出下列步骤中的化学方程式:
步骤Ⅲ:
步骤V:
(2)步骤II后形成的蓝色溶液中的溶质是
(3)上述方案中可能造成空气污染的步骤是
更新时间:2020-05-27 23:46:52
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】人类文明进步与金属材料发展关系十分密切。
(1)炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)空气等为主要原料炼铁,反应过程如下:
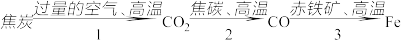
请写出步骤2反应的化学方程式:_____ 。在该反应中体现出焦炭的_____ 性。
(2)工业上用铝土矿(含有A12O3和SiO2,不考虑其它杂质)制取金属铝的基本流程如图所示:
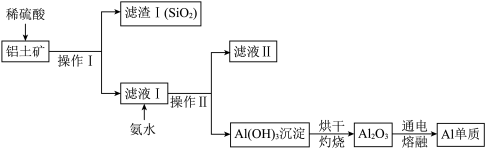
①通过该流程可得出SiO2的性质有_____ (填序号)。
A 难溶于水
B 不能与稀硫酸反应
C 能与氢氧化钠溶液反应
②铝土矿中氧化铝与稀硫酸反应的化学方程式为_____ ,该反应属于_____ (基本反应类型)。
③操作Ⅰ、操作Ⅱ的名称是_____ 。
④将熔融状态的氧化铝通电分解得到单质铝的反应方程式为_____ 。
(1)炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)空气等为主要原料炼铁,反应过程如下:
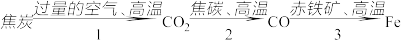
请写出步骤2反应的化学方程式:
(2)工业上用铝土矿(含有A12O3和SiO2,不考虑其它杂质)制取金属铝的基本流程如图所示:

①通过该流程可得出SiO2的性质有
A 难溶于水
B 不能与稀硫酸反应
C 能与氢氧化钠溶液反应
②铝土矿中氧化铝与稀硫酸反应的化学方程式为
③操作Ⅰ、操作Ⅱ的名称是
④将熔融状态的氧化铝通电分解得到单质铝的反应方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】我国煤炭资源丰富。某实验室设计的利用水煤浆(由煤和水混合而成)制备氢气的生产工艺如图流程一
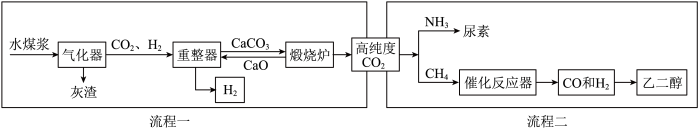
【流程一】制备氢气。
(1)气化器中发生的主要反应为:Ⅰ: 、Ⅱ:
、Ⅱ: (反应条件省略),在这两个反应中,具有还原性的物质是
(反应条件省略),在这两个反应中,具有还原性的物质是_______ 。
(2)重整器的作用是_______ 。重整器中发生反应的化学方程式是_______ 。
【流程二】为充分利用流程一产生的高纯度二氧化碳,该实验室又设计了如图中流程二所示的两种工艺分别制备尿素和乙二醇。
(1)在高温高压下,CO2和NH3可合成尿素【CO(NH2)2】,该反应____ (填“是”或“否”)属于化合反应类型。
(2)以CO和H2为原料生产乙二醇(C2H6O2)时,按照“绿色化学”的原则,应调节原料中CO和H2的分子个数比为_______ 。
(3)近年,中科院大连化学物理研究所研制出一种新型多功能复合催化剂,通过下图示意的Ⅰ、Ⅱ、Ⅲ三个环节,将二氧化碳成功转化为汽油(图中A、B是最终制得的汽油中所含物质的分子结构模型)。
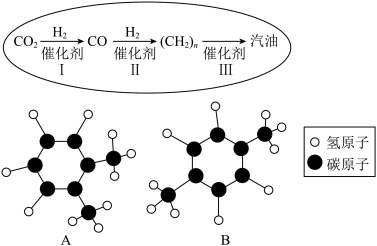
①在一定条件下,环节I除生成CO外,还生成了一种氧化物,该反应的化学方程式为_______ 。
②观察图中A和B两种物质的分子结构模型,A分子和B分子的_______ 构成相同(选填“元素”“原子”“离子”),但其分子结构不同。你认为A和B的化学性质_______ (填“是”或“否”)完全相同。

【流程一】制备氢气。
(1)气化器中发生的主要反应为:Ⅰ:
 、Ⅱ:
、Ⅱ: (反应条件省略),在这两个反应中,具有还原性的物质是
(反应条件省略),在这两个反应中,具有还原性的物质是(2)重整器的作用是
【流程二】为充分利用流程一产生的高纯度二氧化碳,该实验室又设计了如图中流程二所示的两种工艺分别制备尿素和乙二醇。
(1)在高温高压下,CO2和NH3可合成尿素【CO(NH2)2】,该反应
(2)以CO和H2为原料生产乙二醇(C2H6O2)时,按照“绿色化学”的原则,应调节原料中CO和H2的分子个数比为
(3)近年,中科院大连化学物理研究所研制出一种新型多功能复合催化剂,通过下图示意的Ⅰ、Ⅱ、Ⅲ三个环节,将二氧化碳成功转化为汽油(图中A、B是最终制得的汽油中所含物质的分子结构模型)。

①在一定条件下,环节I除生成CO外,还生成了一种氧化物,该反应的化学方程式为
②观察图中A和B两种物质的分子结构模型,A分子和B分子的
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室废液中含有硝酸银、硝酸铜,实验小组利用稀硫酸和铁粉分离回收银和铜,设计如下方案。先在废液中加入过量的铁粉,充分反应后过滤得到滤渣A,其成分为银、铜和铁。再对滤渣A按如下流程图处理:
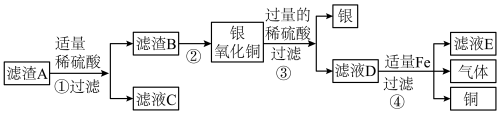
(1)步骤①加入稀硫酸的目的是______ ,可观察到的现象有______ 。
(2)经过步骤②的处理,滤渣的质量______ (填“增大”“减小”或“不变”)。
(3)写出步骤④中发生的一个化学反应方程式______ 。
(4)与将废液直接例入下水道相比,该实验小组做法的优点是______ 。

(1)步骤①加入稀硫酸的目的是
(2)经过步骤②的处理,滤渣的质量
(3)写出步骤④中发生的一个化学反应方程式
(4)与将废液直接例入下水道相比,该实验小组做法的优点是
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
名校
解题方法
【推荐2】阅读科普短文回答相关问题。
钠元素在自然界中分布很广,储量极为丰富,常以氯化钠、碳酸钠、硫酸钠等物质存在。
19世纪初,英国化学家戴维在实验室中首次制得了金属钠。
钠是一种银白色金属,质软,密度为0.97g·cm-3,熔点为97.8℃,金属钠的性质很活泼,能与许多物质发生化学反应。钠暴露在空气中,与氧气反应生成氧化钠(Na2O),钠在空气中燃烧,生成淡黄色的过氧化钠(Na2O2);钠遇水立即发生剧烈反应,生成氢氧化钠和氢气。因此,实验室常将钠保存在煤油中。
金属钠的用途广泛。钠和钾形成的合金熔点低,常温下呈液态,可用作快中子反应堆的热交换剂。利用钠的强还原性,在一定条件下可以将钛(Ti)、锆(Zr)等稀有金属从其氯化物中置换出来。
工业上通常采用电解熔融氯化钠的方法制取单质钠。
(1)自然界中钠元素以__________ (填“单质”或“化合物”)形式存在。
(2)钠保存在煤油中,是为了防止钠与空气中__________ 反应而变质。
(3)过氧化钠中的阴离子为 ,1个
,1个 离子含有的电子数为
离子含有的电子数为____________ 。
(4)钠钾合金用作快中子反应堆的热交换剂、利用钠钾合金良好的 (填字母)。
(5)写出钠与水反应化学方程式_______________________ 。
钠元素在自然界中分布很广,储量极为丰富,常以氯化钠、碳酸钠、硫酸钠等物质存在。
19世纪初,英国化学家戴维在实验室中首次制得了金属钠。
钠是一种银白色金属,质软,密度为0.97g·cm-3,熔点为97.8℃,金属钠的性质很活泼,能与许多物质发生化学反应。钠暴露在空气中,与氧气反应生成氧化钠(Na2O),钠在空气中燃烧,生成淡黄色的过氧化钠(Na2O2);钠遇水立即发生剧烈反应,生成氢氧化钠和氢气。因此,实验室常将钠保存在煤油中。
金属钠的用途广泛。钠和钾形成的合金熔点低,常温下呈液态,可用作快中子反应堆的热交换剂。利用钠的强还原性,在一定条件下可以将钛(Ti)、锆(Zr)等稀有金属从其氯化物中置换出来。
工业上通常采用电解熔融氯化钠的方法制取单质钠。
(1)自然界中钠元素以
(2)钠保存在煤油中,是为了防止钠与空气中
(3)过氧化钠中的阴离子为
 ,1个
,1个 离子含有的电子数为
离子含有的电子数为(4)钠钾合金用作快中子反应堆的热交换剂、利用钠钾合金良好的 (填字母)。
| A.导电性 | B.导热性 | C.延展性 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】1637年(明崇祯十年)宋应星的《天工开物》一书刻板刊行,书中全面系统地总结了明代农业和手工业领域内的生产技术,蕴涵的化学史料极为丰富。下表列出了《天工开物》中物质名称对应的主要成分,请你回答下列问题:
从化学的角度对以上物质进行分类,属于有机物的是___________ (填化学式对应的名称,下同);属于盐的是___________ 。若把“密陀僧”与碳粉混合后加热,可生成银白色的金属和“能使澄清的石灰水变浑浊”的气体,写出相应的化学方程式___________ ;若把“倭铅”放入硫酸中,有关反应的化学方程式为___________ 。
| 物质名称 | 主要成分 | 主要名称 | 主要成分 |
| 苦卤 | MgCl2 | 砒霜 | As2O3 |
| 石灰 | CaO | 密陀僧、黄丹 | PbO |
| 倭铅 | Zn | 井火 | CH4 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】合金是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质。一般来说,合金的熔点低于其中任何一个组成金属的熔点。下表是一些金属熔点的数据。
(1)铅锡合金中某种金属的质量分数与合金的熔点有如如图所示的关系,其中横坐标表示的是________ 的质量分数;当合金熔点最低时,合金中铅与锡的质量比为____________ 。
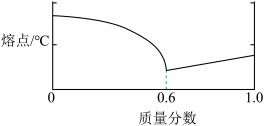
(2)保险丝由铋、铅、锡、镉等金属组成,其熔点约为________ 。
A.20-40℃ B.60-80℃ C.230-250℃ D.300-320℃
(3)青铜器的主要成分是铜锡合金。崭新的青铜器呈土黄色。当青铜器长期埋在地下,逐渐形成了绿色的铜绿【主要成分Cu2(OH)2CO3】,从其化学式可知,铜绿是铜与___________ 、___________ 和___________ (填物质的化学式)长期作用的结果。
(4)通常情况下铁的合金制品也比较容易生锈,请写出工业上用稀盐酸除去铁锈(Fe2O3)的化学方程式_______________________________ 。
| 金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
| 熔点/℃ | 1083 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |

(2)保险丝由铋、铅、锡、镉等金属组成,其熔点约为
A.20-40℃ B.60-80℃ C.230-250℃ D.300-320℃
(3)青铜器的主要成分是铜锡合金。崭新的青铜器呈土黄色。当青铜器长期埋在地下,逐渐形成了绿色的铜绿【主要成分Cu2(OH)2CO3】,从其化学式可知,铜绿是铜与
(4)通常情况下铁的合金制品也比较容易生锈,请写出工业上用稀盐酸除去铁锈(Fe2O3)的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐3】已知A~F为初中化学中常见物质,它们之间的关系如图所示,“→”表示转化关系,“﹣”表示相互之间能反应(部分反应物、生成物以及反应条件省略)。其中A是使用最广泛的金属;B的溶液呈蓝色,可用于配制波尔多液;C常用于改良酸性土壤;D常温下为液体;固态E可用于人工降雨;F为汽车常用的电瓶中的酸。
回答下列问题:
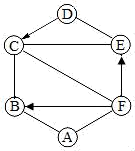
(1)B的化学式为___ ,E的化学式为___ 。
(2)C俗称___ ;如图转化中没有涉及到的基本反应类型为___ 反应。
(3)写出下列反应的化学方程式:A与F___ ;B与C___ ;D→C___ 。
回答下列问题:

(1)B的化学式为
(2)C俗称
(3)写出下列反应的化学方程式:A与F
您最近一年使用:0次
【推荐1】某化学兴趣小组同学对实验室里的粗盐样品进行了如下实验探究:
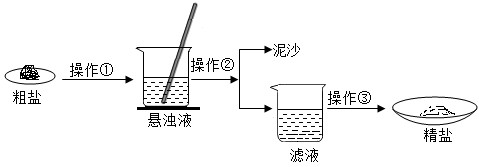
(1)实验多次用到玻璃棒,操作②中玻璃棒的作用是______ 。
(2)查阅资料得知:粗盐中除含少量泥沙等不溶性杂质外,还含有少量的可溶性杂质。为了得到较纯净的氯化钠,小组同学将所得的“精盐”(假定可溶性杂质只有MgCl2一种) 又做了如下处理:
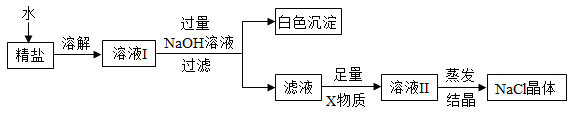
①实验中加入过量的氢氧化钠溶液,发生反应的化学方程式为____________ 。
②在得到的滤液中加入足量的X物质,该物质的化学式为____________________ 。
③若实验过程中不考虑损耗,最终到的NaCl固体的质量将___________ (填 “大于”“小于”或“等于”)原精盐中NaCl的质量。

(1)实验多次用到玻璃棒,操作②中玻璃棒的作用是
(2)查阅资料得知:粗盐中除含少量泥沙等不溶性杂质外,还含有少量的可溶性杂质。为了得到较纯净的氯化钠,小组同学将所得的“精盐”(假定可溶性杂质只有MgCl2一种) 又做了如下处理:

①实验中加入过量的氢氧化钠溶液,发生反应的化学方程式为
②在得到的滤液中加入足量的X物质,该物质的化学式为
③若实验过程中不考虑损耗,最终到的NaCl固体的质量将
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某实验小组的甲、乙两同学围绕酸碱盐的化学性质进行了如图一所示的实验。实验结束后,丙同学把A、B两支试管中过滤后的溶液倒入同一洁净的烧杯中(如图二),充分混合后发现产生了气泡。
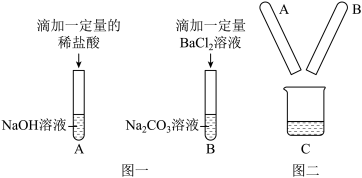
(1)甲同学的实验完成后,A试管一定有剩余的物质是______ 。
(2)乙同学的实验发生的化学方程式是______ 。

(1)甲同学的实验完成后,A试管一定有剩余的物质是
(2)乙同学的实验发生的化学方程式是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
【推荐3】有一包白色固体粉末可能由NH4Cl、 Na2CO3 、BaCl2、CuSO4、NaCl中的一种或几种组成。为了确定其组成,小东做了以下实验:
①取少量白色粉末于研钵中,加入少量的熟石灰粉末混合,研磨,没有闻到氨味;
②另取少量白色粉末加入到适量的水中,出现白色浑浊,静置后,上层清液无色;
③小心倒掉上层清液,向沉淀中加入稀硝酸,白色沉淀完全溶解,并有无色无味的气体产生。由以上实验可推断:
(1)这包白色固体中肯定存在_________________ ,肯定不存在__________________ ;
(2)写出②中出现白色浑浊的化学方程式___________________________________ 。
①取少量白色粉末于研钵中,加入少量的熟石灰粉末混合,研磨,没有闻到氨味;
②另取少量白色粉末加入到适量的水中,出现白色浑浊,静置后,上层清液无色;
③小心倒掉上层清液,向沉淀中加入稀硝酸,白色沉淀完全溶解,并有无色无味的气体产生。由以上实验可推断:
(1)这包白色固体中肯定存在
(2)写出②中出现白色浑浊的化学方程式
您最近一年使用:0次



