中和反应是化学核心概念之一。某化学兴趣小组对中和反应展开了探究。
【实验目的】证明氢氧化钠溶液与盐酸发生化学反应。
【实验步骤】
步骤一:取一定量稀氢氧化钠溶液于烧杯中,滴加2滴酚酞试液,溶液呈红色。
步骤二:用仪器A吸取稀盐酸向烧杯中逐滴加入,边滴加边用玻璃棒搅拌,红色变浅直至消失。
步骤三:向溶液中继续滴加稀盐酸至溶液呈酸性,用玻璃棒蘸取其中溶液,在酒精灯上加热至蒸干,有白色固体产生。
【思考拓展】
(1)从下列仪器中选择步骤二中的“仪器A”,名称是_________ 。
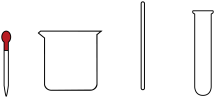
(2)兴趣小组认为仅从上述步骤二的现象,难以证明盐酸与氢氧化钠发生了反应。
查阅资料:(i)酚酞试液在不同的pH时变化情况如下:
(ⅱ)氢氧化钠溶液的pH随浓度的降低而减小。
兴趣小组据此形成了对比实验方案以排除干扰,该对比实验方案是_____ 。
(3)为确认步骤三中的白色固体是氯化钠而不是氢氧化钠,进行如下实验:
【继续探究】
(4)如图是氢氧化钠与盐酸反应的微观示意图。从微观角度分析,氢氧化钠溶液和盐酸反应的实质是__________ 。

(5)兴趣小组认为上述实验对反应实质缺少直观的验证。
查阅资料:(ⅲ)变色硅胶为蓝色,吸水后呈红色。(ⅳ)变色硅胶与NaOH固体充分混合,无明显现象;变色硅胶与无水醋酸(CH3COOH)充分混合,无明显现象。
兴趣小组据此设计了如图实验,验证中和反应有水生成:将无水醋酸迅速倒入装有NaOH固体和变色硅胶的试管中,并用玻璃棒在试管中不断搅拌,观察到变色硅胶由蓝色逐渐变为红色,U型管内液面左低右高。

①U型管内液面左低右高说明该反应____ 热量(填写“放出”或“吸收”)。
②无水醋酸由CH3COO-和H+构成。变色硅胶由蓝色变成红色的原因是______ (用化学方程式表示)。
【实验目的】证明氢氧化钠溶液与盐酸发生化学反应。
【实验步骤】
步骤一:取一定量稀氢氧化钠溶液于烧杯中,滴加2滴酚酞试液,溶液呈红色。
步骤二:用仪器A吸取稀盐酸向烧杯中逐滴加入,边滴加边用玻璃棒搅拌,红色变浅直至消失。
步骤三:向溶液中继续滴加稀盐酸至溶液呈酸性,用玻璃棒蘸取其中溶液,在酒精灯上加热至蒸干,有白色固体产生。
【思考拓展】
(1)从下列仪器中选择步骤二中的“仪器A”,名称是

(2)兴趣小组认为仅从上述步骤二的现象,难以证明盐酸与氢氧化钠发生了反应。
查阅资料:(i)酚酞试液在不同的pH时变化情况如下:
| pH | 0~8.2 | 8.2~10.0 | 10.0~14.0 |
| 颜色 | 无色 | 粉红色 | 红色 |
(ⅱ)氢氧化钠溶液的pH随浓度的降低而减小。
兴趣小组据此形成了对比实验方案以排除干扰,该对比实验方案是
(3)为确认步骤三中的白色固体是氯化钠而不是氢氧化钠,进行如下实验:
| 步骤 | 现象 | 结论 | |
| 将白色固体溶于水形成溶液,均分成两等份 | 向其中一份滴加CuSO4溶液,振荡、静置 | ①无 | 白色固体不是NaOH。 |
| 向另一份滴加AgNO3溶液,振荡、静置 | 出现白色沉淀 | ②白色固体是NaCl,反应的化学方程式为 | |
【继续探究】
(4)如图是氢氧化钠与盐酸反应的微观示意图。从微观角度分析,氢氧化钠溶液和盐酸反应的实质是

(5)兴趣小组认为上述实验对反应实质缺少直观的验证。
查阅资料:(ⅲ)变色硅胶为蓝色,吸水后呈红色。(ⅳ)变色硅胶与NaOH固体充分混合,无明显现象;变色硅胶与无水醋酸(CH3COOH)充分混合,无明显现象。
兴趣小组据此设计了如图实验,验证中和反应有水生成:将无水醋酸迅速倒入装有NaOH固体和变色硅胶的试管中,并用玻璃棒在试管中不断搅拌,观察到变色硅胶由蓝色逐渐变为红色,U型管内液面左低右高。

①U型管内液面左低右高说明该反应
②无水醋酸由CH3COO-和H+构成。变色硅胶由蓝色变成红色的原因是
2020·江苏连云港·中考真题 查看更多[9]
江苏省连云港市2020年中考化学试题(已下线)专题08 中和反应及反应后溶液成分的确定(考点专练)-备战2021年中考化学考点微专题(已下线)专题08:常见的酸和碱(测试)--2021年中考化学一轮复习讲练测(人教版)甘肃省武威市第九中学,爱华育新学校,新起点学校2020-2021学年九年级下学期第一次月考化学试题(已下线)【万唯原创】2021年河南省中考化学试题研究卷练习册九年级第十单元(已下线)(苏州卷)2021年中考化学第二次模拟考试2022年河北省石家庄市平山县营里中学中考模拟化学试题(已下线)第14课 课题2酸和碱的中和反应-2022-2023学年九年级化学下学期课后培优分级练(人教版)(已下线)7.2.3中和反应-【帮课堂】2022-2023学年九年化学下册同步精品讲义(沪教版 )
更新时间:2020-07-17 12:14:38
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组的同学做“铁与稀硫酸反应”实验时,误用了浓硫酸,发现无明显现象,加热后闻到刺激性的气味。带着疑问,该小组同学进行了以下探究活动。
【温故知新】
(1)一般来说,铁、铝等金属在常温下不能与浓硫酸反应放出氢气,说明浓硫酸具有特殊的性质。铁与稀硫酸反应的化学方程式是___________________________ ;
【查阅资料】
①在加热的条件下铁与浓硫酸反应有无色气体 生成。
生成。
② 与
与 具有某些相似的化学性质,都能与NaOH溶液反应。但
具有某些相似的化学性质,都能与NaOH溶液反应。但 能使品红溶液褪色,
能使品红溶液褪色, 不能使品红溶液褪色。
不能使品红溶液褪色。
【设计方案】
为了验证足量的铁和浓硫酸在加热条件下反应所得气体的成分,该小组同学在老师的帮助下设计了如下实验装置和探究方案:
(2)
【拓展应用】
某同学用上述浓硫酸配制质量分数为15%的稀硫酸处理某造纸厂含NaOH的碱性废水:
(3)用9.2g质量分数为98%的浓硫酸能配制上述稀硫酸_________ g(计算结果保留整数)。
(4)若上述造纸厂废水75g能与9.8g15%的稀硫酸恰好反应(设只发生NaOH与硫酸的反应),试计算该废水中NaOH的质量分数(写出计算过程,结果精确到0.1%)。
【反思评价】
(5)足量的铁和浓硫酸在加热的条件下反应产生 气体,随着反应的进行,硫酸的浓度逐渐变稀,铁与稀硫酸反应产生氢气,请写出试管④中气体燃烧的化学方程式
气体,随着反应的进行,硫酸的浓度逐渐变稀,铁与稀硫酸反应产生氢气,请写出试管④中气体燃烧的化学方程式_________________________ ;
(6)实验过程中两次用到品红溶液,品红溶液的作用分别是:_______________ ,_______________ ;
(7) 是导致硫酸型酸雨的主要气体,写出
是导致硫酸型酸雨的主要气体,写出 与水反应生成亚硫酸的化学方程式:
与水反应生成亚硫酸的化学方程式:____________________ ;
(8)铁和硫酸反应所得气体的成分与下列____________ 因素有关(填序号)。
①温度 ②浓度 ③压强 ④硫酸体积
【温故知新】
(1)一般来说,铁、铝等金属在常温下不能与浓硫酸反应放出氢气,说明浓硫酸具有特殊的性质。铁与稀硫酸反应的化学方程式是
【查阅资料】
①在加热的条件下铁与浓硫酸反应有无色气体
 生成。
生成。②
 与
与 具有某些相似的化学性质,都能与NaOH溶液反应。但
具有某些相似的化学性质,都能与NaOH溶液反应。但 能使品红溶液褪色,
能使品红溶液褪色, 不能使品红溶液褪色。
不能使品红溶液褪色。【设计方案】
为了验证足量的铁和浓硫酸在加热条件下反应所得气体的成分,该小组同学在老师的帮助下设计了如下实验装置和探究方案:

(2)
实验步骤 | 实验现象 | 实验结论 |
| (1)如图,先将适量浓硫酸加入试管中,再将可抽动的铁丝放入浓硫酸中,观察实验现象。然后加热,继续观察实验现象。 | 加热时铁丝表面有无色气泡产生,①中品红溶液 | 无色气体中一定含有 |
| ②中无明显现象。 | ②中NaOH溶液的作用是 | |
| ③中品红溶液不褪色。 | ③可得出的结论是 | |
| (2)点燃④中收集的无色气体 | 气体能燃烧,发出淡蓝色火焰。 | 该气体是 |
【拓展应用】
某同学用上述浓硫酸配制质量分数为15%的稀硫酸处理某造纸厂含NaOH的碱性废水:
(3)用9.2g质量分数为98%的浓硫酸能配制上述稀硫酸
(4)若上述造纸厂废水75g能与9.8g15%的稀硫酸恰好反应(设只发生NaOH与硫酸的反应),试计算该废水中NaOH的质量分数(写出计算过程,结果精确到0.1%)。
【反思评价】
(5)足量的铁和浓硫酸在加热的条件下反应产生
 气体,随着反应的进行,硫酸的浓度逐渐变稀,铁与稀硫酸反应产生氢气,请写出试管④中气体燃烧的化学方程式
气体,随着反应的进行,硫酸的浓度逐渐变稀,铁与稀硫酸反应产生氢气,请写出试管④中气体燃烧的化学方程式(6)实验过程中两次用到品红溶液,品红溶液的作用分别是:
(7)
 是导致硫酸型酸雨的主要气体,写出
是导致硫酸型酸雨的主要气体,写出 与水反应生成亚硫酸的化学方程式:
与水反应生成亚硫酸的化学方程式:(8)铁和硫酸反应所得气体的成分与下列
①温度 ②浓度 ③压强 ④硫酸体积
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下实验探究。(包括表中空格)。
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中。该反应的化学方程式为______ 。
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?
【猜想与假设】针对疑问,大家纷纷提出猜想。甲组同学的猜想如下,请你补上猜想四。
猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4、H2SO4和NaOH
猜想四:______ 。
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的。请指出不合理的猜想并说明理由,______ 。
【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有______ 。
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用了老师提供的pH试纸、Na2CO3溶液、BaC12溶液,进行如下三个方案的探究。请完成实验报告:
【得出结论】通过探究,全班同学一致确定猜想二是正确的。
【评价反思】(1)老师对同学们能用多种方法进行探究,并且得出正确结论给予了肯定。同时指出[实验探究](2)中存在两处明显错误,请大家反思。同学们经过反思发现了如下两处错误:
①实验操作中的错误是______ ;
②实验方案中也有一个是错误的,错误的原因是______ 。
(2)在分析反应后所得溶液中溶质成分时,除了考虑生成物外,还需要考虑______ 。
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中。该反应的化学方程式为
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?
【猜想与假设】针对疑问,大家纷纷提出猜想。甲组同学的猜想如下,请你补上猜想四。
猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4、H2SO4和NaOH
猜想四:
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的。请指出不合理的猜想并说明理由,
【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用了老师提供的pH试纸、Na2CO3溶液、BaC12溶液,进行如下三个方案的探究。请完成实验报告:
| 实验方案 | 测溶液的pH | 滴加Na2CO3溶液 | 滴加BaC12溶液 |
| 实验操作 |  |  | 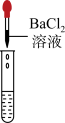 |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 产生白色沉淀 | |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【得出结论】通过探究,全班同学一致确定猜想二是正确的。
【评价反思】(1)老师对同学们能用多种方法进行探究,并且得出正确结论给予了肯定。同时指出[实验探究](2)中存在两处明显错误,请大家反思。同学们经过反思发现了如下两处错误:
①实验操作中的错误是
②实验方案中也有一个是错误的,错误的原因是
(2)在分析反应后所得溶液中溶质成分时,除了考虑生成物外,还需要考虑
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】为探究酸与碱能否发生反应,同学们进行如下实验:
(1)取少量氢氧化钠溶液,滴加酚酞试液,再逐滴加入稀硫酸并振荡,观察到________ 现象,证明氢氧化钠和稀硫酸发生了反应,有关的化学方程式是_______ 。
(2)取少量氢氧化钠溶液,用 试纸测出其
试纸测出其 为a,然后边滴加稀盐酸边振荡,再测溶液的
为a,然后边滴加稀盐酸边振荡,再测溶液的 为b.下列认识正确的是________。
为b.下列认识正确的是________。
向氢氧化钾溶液中滴加了一些稀硫酸,观察不到明显现象发生。接下来,对所得溶液的溶质成分进行探究。
【提出猜想】
(3)猜想①:溶质只有硫酸钾;猜想②:溶质有________ ;猜想③:溶质有硫酸钾和硫酸;猜想④:溶质有硫酸钾、氢氧化钾和硫酸.其中不合理猜想是________ 。
【实验验证】
(4)请回答下列问题。
【反思拓展】
(5)探究反应后物质成分时,不仅要考虑生成物,还需考虑________ 。
(6)在“实验验证”中,要证明猜想③正确,步骤b所滴加的溶液还可用________ 来代替(要求“实验现象”没有气体产生)。
(1)取少量氢氧化钠溶液,滴加酚酞试液,再逐滴加入稀硫酸并振荡,观察到
(2)取少量氢氧化钠溶液,用
 试纸测出其
试纸测出其 为a,然后边滴加稀盐酸边振荡,再测溶液的
为a,然后边滴加稀盐酸边振荡,再测溶液的 为b.下列认识正确的是________。
为b.下列认识正确的是________。A.若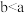 ,则证明氢氧化钠和稀盐酸发生了反应 ,则证明氢氧化钠和稀盐酸发生了反应 |
B.若 ,则证明氢氧化钠和稀盐酸发生了反应 ,则证明氢氧化钠和稀盐酸发生了反应 |
C.从微观角度分析,该反应实质是 与 与 结合成水 结合成水 |
向氢氧化钾溶液中滴加了一些稀硫酸,观察不到明显现象发生。接下来,对所得溶液的溶质成分进行探究。
【提出猜想】
(3)猜想①:溶质只有硫酸钾;猜想②:溶质有
【实验验证】
(4)请回答下列问题。
| 实验步骤 | 实验现象 | 实验结论 |
| a.取样,滴入酚酞试液 | 猜想②错误 | |
| b.再取样,滴加 | 有气体产生 | 猜想③正确 |
【反思拓展】
(5)探究反应后物质成分时,不仅要考虑生成物,还需考虑
(6)在“实验验证”中,要证明猜想③正确,步骤b所滴加的溶液还可用
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】请你参与某学习小组研究性学习的过程,并协助完成相关任务。
【研究课题】探究X物质的成分。
【查阅资料】(1)X物质可能由Ca(HCO3)2、Mg(HCO3)2、Ca(OH)2、Mg(OH)2、CaCO3、BaCO3中的一种或几种组成。
(2)X物质是通过过滤水溶液得到的沉淀。
(3)相关物质的溶解性如下表:
【设计并实施方案】
(1)由查阅资料可知X物质肯定不含可溶性的Ca(HCO3)2、Mg(HCO3)2。
(2)甲同学在烧杯中放入少量研碎的X物质,加入足量蒸馏水充分搅拌,静置。取上层清液滴入Na2CO3溶液,没有白色沉淀,说明X物质中无_______ (填化学式)。
(3)乙同学设计了下列实验装置,想进一步确定X物质的成分。
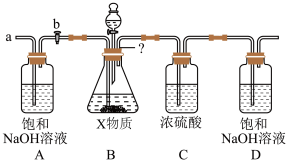
其主要实验步骤如下:
①按图组装仪器,关闭活塞b,将50gX物质的粉末放入锥形瓶中,逐滴加入足量稀硫酸,充分反应。
②待锥形瓶中不再产生气泡时,打开活塞b,从导管a处缓缓鼓入一定量的空气;
③称量D瓶内物质明显增加的质量;
④继续鼓入空气,直至D瓶内物质质量不变;
⑤经称量,D瓶内物质增加的质量为20g。
【评价】(1)A瓶中的NaOH溶液起到____________ 作用。若A瓶中无NaOH溶液,D瓶中的质量将 __________ (填“增大”、“不变”或“减小”)。
(2)分析X物质的可能组成是___________ (有几种写几种)。
【研究课题】探究X物质的成分。
【查阅资料】(1)X物质可能由Ca(HCO3)2、Mg(HCO3)2、Ca(OH)2、Mg(OH)2、CaCO3、BaCO3中的一种或几种组成。
(2)X物质是通过过滤水溶液得到的沉淀。
(3)相关物质的溶解性如下表:
| 物 质 | Ca(HCO3)2 | Mg(HCO3)2 | Ca(OH)2 | Mg(OH)2 | CaCO3 | BaCO3 |
| 溶解性 | 可溶 | 可溶 | 微溶 | 不溶 | 不溶 | 不溶 |
(1)由查阅资料可知X物质肯定不含可溶性的Ca(HCO3)2、Mg(HCO3)2。
(2)甲同学在烧杯中放入少量研碎的X物质,加入足量蒸馏水充分搅拌,静置。取上层清液滴入Na2CO3溶液,没有白色沉淀,说明X物质中无
(3)乙同学设计了下列实验装置,想进一步确定X物质的成分。

其主要实验步骤如下:
①按图组装仪器,关闭活塞b,将50gX物质的粉末放入锥形瓶中,逐滴加入足量稀硫酸,充分反应。
②待锥形瓶中不再产生气泡时,打开活塞b,从导管a处缓缓鼓入一定量的空气;
③称量D瓶内物质明显增加的质量;
④继续鼓入空气,直至D瓶内物质质量不变;
⑤经称量,D瓶内物质增加的质量为20g。
【评价】(1)A瓶中的NaOH溶液起到
(2)分析X物质的可能组成是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某化学小组在一次查阅资料时得知:二氧化碳与氢氧化钠反应,若二氧化碳过量,生成的碳酸钠会继续与二氧化碳反应生成碳酸氢钠,反应原理为:Na2CO3+CO2+H2O=2NaHCO3。
出于好奇,同学们一起向一定量的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后,低温蒸发结晶,得到了白色固体。
【提出问题】白色固体是什么?
【作出猜想】
猜想Ⅰ:只有Na2CO3; 猜想Ⅱ:可能是Na2CO3和NaOH的混合物;猜想Ⅲ:___________
【查阅资料】
(1)碳酸氢钠不稳定受热易分解2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
(2)Na2CO3与NaOH的热稳定性较好
(3)CaCl2和NaCl的水溶液呈中性
【实验探究】白色固体中是否有氢氧化钠?
【反思拓展】
由于氢氧化钠能与二氧化碳反应,所以实验室保存氢氧化钠一定要注意密封。
出于好奇,同学们一起向一定量的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后,低温蒸发结晶,得到了白色固体。
【提出问题】白色固体是什么?
【作出猜想】
猜想Ⅰ:只有Na2CO3; 猜想Ⅱ:可能是Na2CO3和NaOH的混合物;猜想Ⅲ:
【查阅资料】
(1)碳酸氢钠不稳定受热易分解2NaHCO3
 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O(2)Na2CO3与NaOH的热稳定性较好
(3)CaCl2和NaCl的水溶液呈中性
【实验探究】白色固体中是否有氢氧化钠?
| 实验操作 | 实验现象 | 目的/结论 |
| ①取白色固体适量配制成溶液。往所得溶液中滴加过量的 | 有白色沉淀生成 | 除去白色固体中的 |
| ②取滤液,往滤液中滴入几滴 | 白色固体中没有氢氧化钠 |
由于氢氧化钠能与二氧化碳反应,所以实验室保存氢氧化钠一定要注意密封。
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】经过多年的发展,黄州市的部分县区使用上了天然气,天然气的主要成分是甲烷(CH4),某校化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,请你参与:
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4遇水变蓝。
【猜想与假设】甲:CO2、H2O;乙:CO、H2O;丙:NH3、CO2、H2O;丁:CO2、CO、H2O
你认为________ 同学的猜想是错误的,理由是_____ 。
【实验探究】为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过下列装置:

(1)实验中观察到A中无水CuSO4变蓝,B、D中澄清石灰水变浑浊,C中红色粉末变成黑色,由此推断________ 同学猜想成立。其中D种澄清石灰水的作用是_________ 。
(2)请写出C中红色粉末变成黑色的化学方程式:_________ 。
【反思与交流】
(3)为避免有毒的CO污染环境,所以含碳元素的物质燃烧必须满足的条件是______ 。用气球收集气体的原因是_______ 。
(4)请写出甲烷完全燃烧的化学方程式________ 。
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4遇水变蓝。
【猜想与假设】甲:CO2、H2O;乙:CO、H2O;丙:NH3、CO2、H2O;丁:CO2、CO、H2O
你认为
【实验探究】为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过下列装置:

(1)实验中观察到A中无水CuSO4变蓝,B、D中澄清石灰水变浑浊,C中红色粉末变成黑色,由此推断
(2)请写出C中红色粉末变成黑色的化学方程式:
【反思与交流】
(3)为避免有毒的CO污染环境,所以含碳元素的物质燃烧必须满足的条件是
(4)请写出甲烷完全燃烧的化学方程式
您最近一年使用:0次



