镁是一种用途很广的金属,目前世界上60%的镁是从海水(溶质主要含NaCl和MgCl2等)中提取的,主要步骤如图:
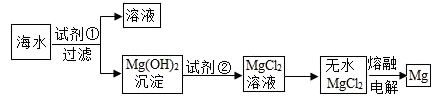
(1)工业生产中,加入试剂①应过量,原因是______________ 。发生反应的化学方程式为________ 。
(2)无水MgCl2在熔融状态下电解可制取金属镁同时生成一种气体,写出制取金属镁的化学方程式____________________ ,该反应属于基本反应类型中的______________ 反应。

(1)工业生产中,加入试剂①应过量,原因是
(2)无水MgCl2在熔融状态下电解可制取金属镁同时生成一种气体,写出制取金属镁的化学方程式
更新时间:2020-07-04 18:52:28
|
相似题推荐
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐1】在某些食品的包装袋内,有一个小纸袋,上面写着“干燥剂,主要成分为生石灰”。将干燥剂放入水中,充分搅拌后静置,得到上层清液和下层固体,取上层清液滴加紫色石蕊溶液,溶液变蓝,则下层固体中一定含有____ ,可能含有____ ,如何检验可能含有的物质,写出反应的化学方程式______ 。
您最近一年使用:0次
【推荐2】化学与生活、生产息息相关,请运用化学知识回答以下问题。
(1)用石灰浆粉刷墙壁,干燥后墙面变硬的原因是_______ 。(用化学方程式表示)。
(2)服用含有氢氧化铝的药物可以治疗胃酸过多症,这是因为(用化学方程 式表示)_______ 。
(1)用石灰浆粉刷墙壁,干燥后墙面变硬的原因是
(2)服用含有氢氧化铝的药物可以治疗胃酸过多症,这是因为(用化学方程 式表示)
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
真题
【推荐3】利用能源、节约能源、保护环境是我们大家共同关注的问题.

(1)充分燃烧1000g天然气和煤所产生的CO2和SO2气体的质量如图所示,则__________ 燃烧对环境影响较小,1000g煤中硫元素的质量为__________ (假设硫元素完全转化为SO2).
(2)SO2的大量排放能形成酸雨,pH__________ 5.6(填写“<”、“>”或“=”)的降雨称为酸雨,在煤燃烧后将烟气通入吸收塔并“喷淋”石灰水进行“脱硫”可减少SO2的排放,石灰水需要“喷淋”的目的是__________ ,石灰水与SO2反应的化学方程式为__________ (SO2和碱反应与CO2相似).
(3)目前,在汽车尾气系统中安装催化转化器可将污染物CO,NO转化为无毒的CO2和N2, ,请根据“在化学反应过程中有元素化合价变化的化学反应,叫做氧化还原反应”判断,该反应
,请根据“在化学反应过程中有元素化合价变化的化学反应,叫做氧化还原反应”判断,该反应__________ (填写“是”或“不是”)氧化还原反应.

(1)充分燃烧1000g天然气和煤所产生的CO2和SO2气体的质量如图所示,则
(2)SO2的大量排放能形成酸雨,pH
(3)目前,在汽车尾气系统中安装催化转化器可将污染物CO,NO转化为无毒的CO2和N2,
 ,请根据“在化学反应过程中有元素化合价变化的化学反应,叫做氧化还原反应”判断,该反应
,请根据“在化学反应过程中有元素化合价变化的化学反应,叫做氧化还原反应”判断,该反应
您最近一年使用:0次
填空与简答-流程题
|
较易
(0.85)
解题方法
【推荐1】镁及其合金是一种用途广泛的金属材料,大量的金属镁是从海水或卤水中提取的,其主要步骤见下图:

(1)加入试剂①后,分离得到Mg(OH)2沉淀的方法是_______ ;
(2)试剂②可以选用_______ ;
(3)通电后,MgCl2分解生成Mg和Cl2的化学反应方程式______ 。

(1)加入试剂①后,分离得到Mg(OH)2沉淀的方法是
(2)试剂②可以选用
(3)通电后,MgCl2分解生成Mg和Cl2的化学反应方程式
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐2】我国海洋化学资源十分丰富。探索海洋是我们人类永恒的使命。海洋占了地球的三分之二,调查利用深海资源是我们整个经济社会持续发展的需要,也是我们国家建设海洋强国的必然选择。
(1)海水晒盐的基本原理为______ (填“蒸发结晶”“降温结晶”之一)。
(2)海水淡化可采用膜分离技术,如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各种离子不能透过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是 (填选项序号)。

(3)海水制镁的工艺流程如图,其中发生的中和反应的化学方程式为______ 。

(4)海水制碱:化学科学家侯德榜创立的侯氏制碱法,就是以食盐溶液、二氧化碳、氨气为原料制得纯碱的工艺。其生产过程中有下列反应:
①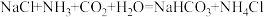 ;
;
②2NaHCO3 Na2CO3+H2O+CO2↑。
Na2CO3+H2O+CO2↑。
碳酸氢钠和氯化铵的溶解度曲线如图所示。请回答下列问题:

①30℃时,NH4Cl的溶解度________ NaHCO3的溶解度(填“大于“小于”“等于”之一)。
②30℃时,将10 gNaHCO3加入50g水中,所得溶液的溶质质量分数为________ (计算结果精确到0.1%)。
③氨盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,从溶解度角度分析,________ 首先结晶析出(填“碳酸氢钠”“氯化铵”之一)。
(1)海水晒盐的基本原理为
(2)海水淡化可采用膜分离技术,如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各种离子不能透过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是 (填选项序号)。

| A.溶质质量减少 | B.溶剂质量减少 | C.溶液质量减少 | D.溶质质量分数减小 |
(3)海水制镁的工艺流程如图,其中发生的中和反应的化学方程式为

(4)海水制碱:化学科学家侯德榜创立的侯氏制碱法,就是以食盐溶液、二氧化碳、氨气为原料制得纯碱的工艺。其生产过程中有下列反应:
①
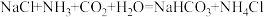 ;
;②2NaHCO3
 Na2CO3+H2O+CO2↑。
Na2CO3+H2O+CO2↑。碳酸氢钠和氯化铵的溶解度曲线如图所示。请回答下列问题:

①30℃时,NH4Cl的溶解度
②30℃时,将10 gNaHCO3加入50g水中,所得溶液的溶质质量分数为
③氨盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,从溶解度角度分析,
您最近一年使用:0次




