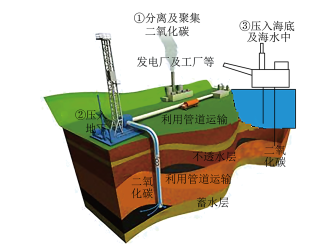
碳捕捉与封存技术 “碳捕捉与封存”是我国的一项先进技术(如图所示)。
(1)“碳捕捉与封存”技术有利于控制________ 的加剧。
(2)煤在极高的温度下充分燃烧,主要发生反应的化学方程式为________ 。
(3)将CO2封入蓄水层中发生反应的化学方程式为________ 。
(4)被封存起来的CO2用于冷藏食物的原理是________ 。
(1)“碳捕捉与封存”技术有利于控制
(2)煤在极高的温度下充分燃烧,主要发生反应的化学方程式为
(3)将CO2封入蓄水层中发生反应的化学方程式为
(4)被封存起来的CO2用于冷藏食物的原理是
20-21九年级上·全国·单元测试 查看更多[3]
(已下线)《单元测试定心卷》第二单元 身边的化学物质(基础过关)-2020-2021学年九年级化学上册单元测试定心卷(沪教版)江苏省苏州市常熟市实验中学2020-2021学年九年级上学期10月月考化学试题(已下线)2024-2025年同步单元讲练测(人教版)第六单元 碳和碳的氧化物-巩固练
更新时间:2020/09/08 14:54:51
|
相似题推荐
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐1】【科普阅读】
石墨烯
石墨烯是从石墨中剥离出来的单层碳原子晶体,是目前为止最薄的二维纳米碳材料,1mm厚的石墨大约包含300万层石墨烯,因其结构特殊,具有很多优异性能,如极高的导热性、导电性及高强度等,被誉为“新材料之王”。
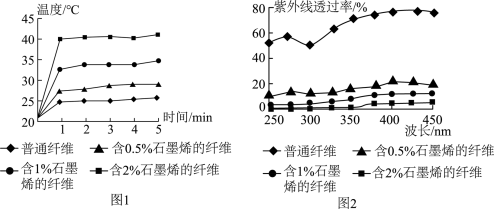
近年来,石墨烯在纺织领域的应用日益广泛,冬季体有比赛时制服就使用了石墨烯材料,其优异性能,为运动员和工作人员保暖护航。石墨烯的远红外升温特性,能瞬间升温,高效蓄热,达到超强保暖的效果。如图1为石墨烯含量对升温效果影响的测试结果。石墨烯还具有良好的防紫外线性能,可有效防止人体皮肤晒伤老化,如图2为不同石墨烯含量的纤维对紫外线透过率影响的测试结果。
(1)“1mm厚的石墨大约包含300万层石墨烯”,说明构成物质的微粒___________ 。
(2)写出石墨烯(主要成分为碳)完全燃烧的化学方程式___________ ,可以用___________ 验证该反应的生成物。
(3)对比图1中四条曲线,得到的结论是___________ ,分析图2,为防止人体皮肤被紫外线晒伤老化,最好选择含___________ 石墨烯的纤维。
(4)石墨烯因为___________ 所以可用于制作衣服,石墨烯具有良好的导电性,它还可能的用途有___________ (写一种)。
石墨烯
石墨烯是从石墨中剥离出来的单层碳原子晶体,是目前为止最薄的二维纳米碳材料,1mm厚的石墨大约包含300万层石墨烯,因其结构特殊,具有很多优异性能,如极高的导热性、导电性及高强度等,被誉为“新材料之王”。
近年来,石墨烯在纺织领域的应用日益广泛,冬季体有比赛时制服就使用了石墨烯材料,其优异性能,为运动员和工作人员保暖护航。石墨烯的远红外升温特性,能瞬间升温,高效蓄热,达到超强保暖的效果。如图1为石墨烯含量对升温效果影响的测试结果。石墨烯还具有良好的防紫外线性能,可有效防止人体皮肤晒伤老化,如图2为不同石墨烯含量的纤维对紫外线透过率影响的测试结果。
(1)“1mm厚的石墨大约包含300万层石墨烯”,说明构成物质的微粒
(2)写出石墨烯(主要成分为碳)完全燃烧的化学方程式
(3)对比图1中四条曲线,得到的结论是
(4)石墨烯因为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
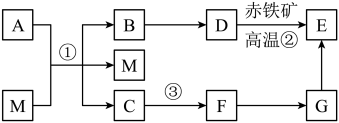
【推荐2】A--H是初中常见的物质,A、D、G为单质,其余物质均为化合物.其中D是一种红色固体单质;E是一种有特殊气味的液体,通过某反应可同时生成H和F.(反应条件和某些反应物、生成物已省略)
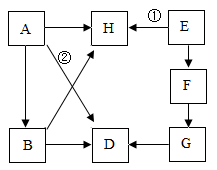
试写出下列物质的化学式:
(1)B___________ G__________
(2)写出下列反应的方程式
E→H+F_____________________
A→D+H_____________________

试写出下列物质的化学式:
(1)B
(2)写出下列反应的方程式
E→H+F
A→D+H
您最近一年使用:0次
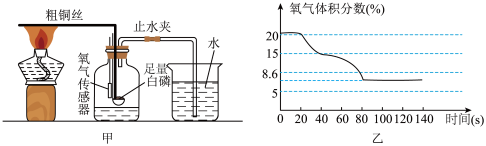
【推荐1】【空气主题学习】小金利用如图甲所示装置(气密性良好)和试剂测定空气中氧气含量,集气瓶中空气的体积为200mL,氧气传感器测得集气瓶内氧气的体积分数变化曲线如图乙所示。___________ 。
(2)反应开始到止水夹打开前,集气瓶内可观察到的现象是___________ 。
(3)小金提出“倒吸入集气瓶中水的体积除以200mL等于空气中氧气的含量”。据图乙分析,此说法___________ (选填“正确”或“错误”),说明理由:___________ 。
【二氧化碳主题学习】同学们设计实验探究二氧化碳的性质,请你参与探究并回答下列问题:___________ (填“A”或“B”),说明二氧化碳具有的性质是___________ 。
(5)实验二:拧紧盖振荡,软塑料瓶变瘪因为___________ 。
(6)实验三:实验的目的是___________ 。一段时间后,观察到Y型管右侧湿润的紫色石蕊试纸___________ 。
(2)反应开始到止水夹打开前,集气瓶内可观察到的现象是
(3)小金提出“倒吸入集气瓶中水的体积除以200mL等于空气中氧气的含量”。据图乙分析,此说法
【二氧化碳主题学习】同学们设计实验探究二氧化碳的性质,请你参与探究并回答下列问题:
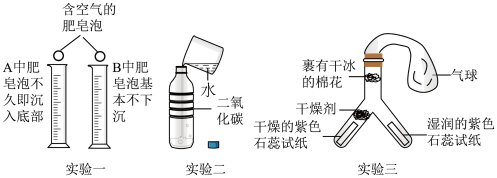
(5)实验二:拧紧盖振荡,软塑料瓶变瘪因为
(6)实验三:实验的目的是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
名校
解题方法
【推荐2】下列是与二氧化碳有关的一些实验,请用你学过的化学知识回答问题。____ 。
(2)图B所示实验,①、④是用紫色石蕊溶液湿润的棉球,②、③是用紫色石蕊溶液染成紫色的干燥棉球。实验过程中能观察到的现象是____ 。
(3)用图C所示矿泉水瓶可以证明CO2与澄清石灰水确实发生了反应,振荡后,其现象是___ ,涉及的化学反应方程式是____ 。
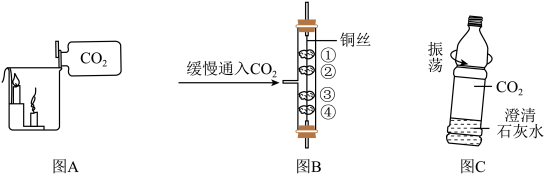
(2)图B所示实验,①、④是用紫色石蕊溶液湿润的棉球,②、③是用紫色石蕊溶液染成紫色的干燥棉球。实验过程中能观察到的现象是
(3)用图C所示矿泉水瓶可以证明CO2与澄清石灰水确实发生了反应,振荡后,其现象是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】2024年4月20日,我国第二艘国产大邮轮开始总装搭载,建造进入加速期,制造邮轮需要大量钢材。
(1)生铁和钢都是铁的合金,其性能不同的本质原因是_______ 不同。
(2)如图是实验室模拟炼铁的微型装置。
(3)某化学小组用一定量AgNO3溶液进行了如图实验,已知溶液甲呈蓝色,其呈蓝色的原因是______ (用化学方程式表示)。向固体乙中滴加盐酸时_______ (填“有”或“没有”)气泡产生。
(1)生铁和钢都是铁的合金,其性能不同的本质原因是
(2)如图是实验室模拟炼铁的微型装置。
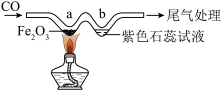
A.a处发生反应的化学方程式为3CO+Fe2O3 2Fe+3CO2 2Fe+3CO2 |
| B.b处可观察到紫色石蕊试液变红 |
| C.实验结束后先停止通入CO再熄灭酒精喷灯 |
| D.可用点燃的方法进行尾气处理 |
(3)某化学小组用一定量AgNO3溶液进行了如图实验,已知溶液甲呈蓝色,其呈蓝色的原因是

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】请在 ①氢气、②石墨、③干冰、④酒精几种物质中选择适当物质填空(填化学式):
(1)写字用的铅笔中含__________ ; (2)司机驾机动车前饮用的饮料不能含有_________ ;
(3)属于未来新型能源的是________ ; (4)可以用作制冷剂的是__________ 。
(1)写字用的铅笔中含
(3)属于未来新型能源的是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】A~F 和 X 是初中化学常见的六种物质,其中 D、F 是单质,A、C 是同种元素组成的无色气体,B、F 是红色固体,它们的转化关系如图(部分生成物已经省略)。
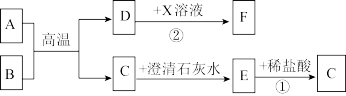
请回答以下问题:
(1)写出 A 物质的化学式______ 。
(2)气体 C 的用途是______ 。
(3)写出反应②的化学方程式______ 。
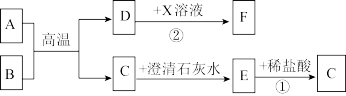
请回答以下问题:
(1)写出 A 物质的化学式
(2)气体 C 的用途是
(3)写出反应②的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】生活中处处有化学。
(1)现有下列6种物质,请选择相应字母编号填空:
A、干冰 B、酒精 C、碱式碳酸铜 D、碳酸氢铵 E、一氧化碳 F、镁粉
①实验室最常用的燃料________ ;
②“司母戊”鼎青铜器锈斑主要成分_______ ;
③可用于制造舞台云雾_______ ;
④农业生产中用作化肥________ ;
⑤可用于制造烟花________ ;
⑥与血红蛋白结合的有毒气体________ ;
(2)厨房味精可以增加膳食的美味。其主要成分为“谷氨酸钠”(化学式是C5H8NO4Na),另外还含有少量NaCl(其他成分不考虑)。则味精属于________ (填“混合物”或“纯净物”),味精中至少含有_________ 种元素(填数字)。
(3)请用化学用语填空:
①海水中含量最多的阳离子_______ ;
②地壳中含量最多的金属元素________ ;
③含氧量最高的氧化物________ 。
(4)空气是由多种成分组成的。______ (填字母编号)。
③常压下,液态氮的沸点_______ 液态氧的沸点(填“>”或“<”或“=”)。将燃着的木条置于盛满液态空气的集气瓶口,观察到的现象是_______ 。将该集气瓶放置一段时间后,液态物质剩余约1/10体积,其主要成分是________ 。
III.从科技的角度
④如图为某种分子筛型家用制氧机工作时气体变化的微观示意图,该制氧机的原理是_______ ,该变化属于______ (填“物理”或“化学”)变化。
牛奶中富含钙,是膳食中最容易被吸收的钙的来源。如图是某乳业公司纯牛奶包装标签文字说明。
①标签中“钙含量”中的钙指的是______ (填字母)
A、碳酸钙 B、钙元素 C、钙单质 D、钙原子
②青少年缺钙可能导致______ 。
③若儿童每天至少需要0.6g的钙,假设这些钙有90%来自牛奶,则每人每天要喝______ 盒这种牛奶。(结果取整数)
(1)现有下列6种物质,请选择相应字母编号填空:
A、干冰 B、酒精 C、碱式碳酸铜 D、碳酸氢铵 E、一氧化碳 F、镁粉
①实验室最常用的燃料
②“司母戊”鼎青铜器锈斑主要成分
③可用于制造舞台云雾
④农业生产中用作化肥
⑤可用于制造烟花
⑥与血红蛋白结合的有毒气体
(2)厨房味精可以增加膳食的美味。其主要成分为“谷氨酸钠”(化学式是C5H8NO4Na),另外还含有少量NaCl(其他成分不考虑)。则味精属于
(3)请用化学用语填空:
①海水中含量最多的阳离子
②地壳中含量最多的金属元素
③含氧量最高的氧化物
(4)空气是由多种成分组成的。
I.从微观角度:用 表示氮原子,
表示氮原子, 表示氧原子。
表示氧原子。
①用“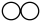 ”表示的微粒是
”表示的微粒是
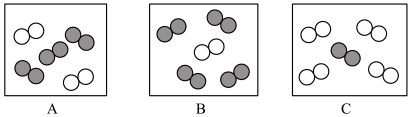
③常压下,液态氮的沸点
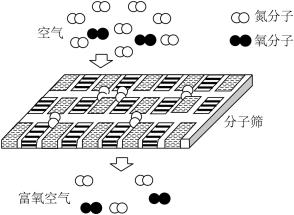
III.从科技的角度
④如图为某种分子筛型家用制氧机工作时气体变化的微观示意图,该制氧机的原理是
牛奶中富含钙,是膳食中最容易被吸收的钙的来源。如图是某乳业公司纯牛奶包装标签文字说明。
| 纯牛奶 配料:鲜牛奶 保质期:6个月(4℃) 净含量:230mL/盒 钙含量:(每100mL) 钙≥0.11g |
A、碳酸钙 B、钙元素 C、钙单质 D、钙原子
②青少年缺钙可能导致
③若儿童每天至少需要0.6g的钙,假设这些钙有90%来自牛奶,则每人每天要喝
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】煤的清洁利用是目前全球热门的研究课题,其中的关键是如何处理煤燃烧后产生的二氧化碳。某研究小组研究开发利用煤直接化学循环技术,成功使煤释放热量的同时,捕获了反应过程中产生的99%的二氧化碳。该方法的流程如图所示:
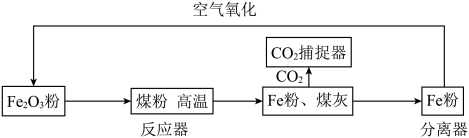
(1)捕捉二氧化碳的目的是____________ 。
(2)将煤、氧化铁磨成粉末的目的是___________ 。
(3)写出反应器中主要的化学方程式_______________________________ 。
(4)该流程中可以循环利用的物质是________________ 。

(1)捕捉二氧化碳的目的是
(2)将煤、氧化铁磨成粉末的目的是
(3)写出反应器中主要的化学方程式
(4)该流程中可以循环利用的物质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
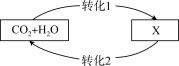
【推荐2】2010年6月5日,世界环境日中国主题为“低碳减排,绿色生活”,旨在传递低碳生活理念,提高公众环保意识.该主题倡导减少二氧化碳的排放,低能量、低消耗的生活方式,从而减少对大气的污染,减缓生态恶化.
(1)自然界中消耗二氧化碳的主要途径是_____
(2)下列措施中,有利于降低大气中CO2浓度的有:_____ .(填字母)
a.减少化石燃料的使用 b.植树造林,增大植被面积
c.采用节能技术 d.利用太阳能、风能
(3)下列做法不符合“低碳经济”理念的是(填序号)_____ ;
①改造或淘汰高能耗、高污染产业;②大力发展火力发电;③研制和开发新能源替代传统能源;④优化建筑设计,增强室内自然采光,减少照明用电;⑤将二氧化碳变废为宝,循环利用.
(4)将CO2转化成有机物可有效实现碳循环.CO2转化成有机物的例子很多,如:
a.6CO2+6H2O C6H12O6+6O2 b.CO2+3H2
C6H12O6+6O2 b.CO2+3H2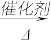 CH3OH+H2O
CH3OH+H2O
c.CO2+CH4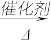 CH3COOH d.2CO2+6H2
CH3COOH d.2CO2+6H2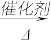 CH2═CH2+4H2O
CH2═CH2+4H2O
以上反应中,最节能的是_____ ,原子利用率最高的是_____ .
(5)“绿色化学”的特点之一是“零排放”(即:只生成一种产物).一定条件下,二氧化碳和氢气可以按照不同比例反应,生成下列有机物,若该生产过程符合“绿色化学”的要求,则这种产物是_____ (填字母序号).
A 甲醇(CH4O) B 甲酸(CH2O2) C 乙醇(C2H6O) D 乙酸(C2H4O2)
(1)自然界中消耗二氧化碳的主要途径是
(2)下列措施中,有利于降低大气中CO2浓度的有:
a.减少化石燃料的使用 b.植树造林,增大植被面积
c.采用节能技术 d.利用太阳能、风能
(3)下列做法不符合“低碳经济”理念的是(填序号)
①改造或淘汰高能耗、高污染产业;②大力发展火力发电;③研制和开发新能源替代传统能源;④优化建筑设计,增强室内自然采光,减少照明用电;⑤将二氧化碳变废为宝,循环利用.
(4)将CO2转化成有机物可有效实现碳循环.CO2转化成有机物的例子很多,如:
a.6CO2+6H2O
 C6H12O6+6O2 b.CO2+3H2
C6H12O6+6O2 b.CO2+3H2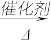 CH3OH+H2O
CH3OH+H2Oc.CO2+CH4
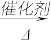 CH3COOH d.2CO2+6H2
CH3COOH d.2CO2+6H2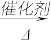 CH2═CH2+4H2O
CH2═CH2+4H2O以上反应中,最节能的是
(5)“绿色化学”的特点之一是“零排放”(即:只生成一种产物).一定条件下,二氧化碳和氢气可以按照不同比例反应,生成下列有机物,若该生产过程符合“绿色化学”的要求,则这种产物是
A 甲醇(CH4O) B 甲酸(CH2O2) C 乙醇(C2H6O) D 乙酸(C2H4O2)
您最近一年使用:0次