为探究酸碱盐之间的反应,小红同学做了以下实验,在稀硫酸中加入了一定量的碳酸钡粉末。请回答:
(1)发生反应的化学方程式是________ ;溶液中减少的离子是_______ (写化学符号)。
(2)若要配制98g质量分数为10%的稀硫酸,需要质量分数为98%的浓硫酸(密度为1.84g/cm3)_____ mL,需要水______ mL(计算结果精确到0.1)。在实验室用浓硫酸配制稀硫酸的主要步骤有:计算、_____ 、混匀、冷却至室温装瓶,并贴上标签。
(1)发生反应的化学方程式是
(2)若要配制98g质量分数为10%的稀硫酸,需要质量分数为98%的浓硫酸(密度为1.84g/cm3)
更新时间:2020-09-09 13:18:53
|
相似题推荐
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐1】阅读下面科普短文,回答下列问题。
对付新型冠状病毒的消毒制
国家卫健委修订印发的《新型冠状病面肺炎防控方案》(第四版)中记录:新型冠状病毒对紫外线和热敏感;含氯消毒制、过氧乙酸和75%酒精等均可有效灭活病毒。
84消毒液是以次氯酸钠(NaClO)为主要有效成分的消毒液,是无色或淡黄色的液体,且具有刺默性气味,有效氯含量为1.1%—1.3%,其主要作用是杀灭肠道致病菌,化脓性球菌和细菌芽孢。84消毒液适用于一般物体表面,白色衣物、医院污染物品的消毒,84消毒液有一定的刺激性与腐蚀性。必须稀释以后才能使用,一般稀程浓度为千分之二到千分之五,即1000mL里面放2—5mL84消毒液。
过氧乙酸又名过醋酸(C2H4O3),无色透明液体,易挥发,有刺激性气味,可溶于水或乙醇等有机溶制。过氧乙酸为强氧化剂,腐蚀性强,有漂白作用。过氧乙酸的性质不稳定,易分解,遇热、强碱,有机物或重金属离子等分解加速。过氧乙酸完全燃烧能生成二氧化碳和水,具有酸的通性,可分解为乙酸和氧气,过氧乙酸属于高效消毒剂,气态过氧乙酸和溶液都具有很强的杀菌能力。它能杀灭细菌繁殖体、分枝杆菌、细菌芽孢、真菌、藻类及病毒,也可以破坏细菌毒素。
75%的酒精可用于消毒,这是因为该浓度的酒精渗透力很强,可穿透细菌表面,进入细菌内部,使组成细菌的蛋白质凝固,导数细菌失去活性。过高浓度的酒精会在细菌表面形成一层保护膜,阻止其进入细菌体内,难以将细菌彻底杀死,若酒精浓度过低,虽可进入细菌,但不能将其体内的蛋白质凝固,同样也下能将细菌彻底杀死,乙醇闪点为12.78℃。火灾危险性属于甲类,75%酒精闪点大约在22℃,火灾危险性还是属于甲类,因此在使用75%酒精进行消毒时,室内禁止采用喷洒式消毒,应采取擦拭方法进行消毒且在消毒过程中避免洒漏酒精,空气中酒精浓度不能超过3%,为防止火灾发生,应保持室内通风。室外采取喷洒式消毒必须禁止明火,防止局部喷洒浓度过大,造成遇明火引发火灾的风险。
阅读上述内容,回答下列问题:
(1)写出84消毒液的一条物理性质:________ ;使用84消毒液时,需要稀释的原因是_________ 。
(2)过氧乙酸完全燃烧的文字表达式:________ ;正确保存过氧乙酸的方法是_________ 。
(3)在药店买到的酒精有75%和95%两种浓度,若用95%酒精配制一定量75%酒精,若要量取95%酒精50mL,用到的玻璃仪器有:量筒和________ 。
对付新型冠状病毒的消毒制
国家卫健委修订印发的《新型冠状病面肺炎防控方案》(第四版)中记录:新型冠状病毒对紫外线和热敏感;含氯消毒制、过氧乙酸和75%酒精等均可有效灭活病毒。
84消毒液是以次氯酸钠(NaClO)为主要有效成分的消毒液,是无色或淡黄色的液体,且具有刺默性气味,有效氯含量为1.1%—1.3%,其主要作用是杀灭肠道致病菌,化脓性球菌和细菌芽孢。84消毒液适用于一般物体表面,白色衣物、医院污染物品的消毒,84消毒液有一定的刺激性与腐蚀性。必须稀释以后才能使用,一般稀程浓度为千分之二到千分之五,即1000mL里面放2—5mL84消毒液。
过氧乙酸又名过醋酸(C2H4O3),无色透明液体,易挥发,有刺激性气味,可溶于水或乙醇等有机溶制。过氧乙酸为强氧化剂,腐蚀性强,有漂白作用。过氧乙酸的性质不稳定,易分解,遇热、强碱,有机物或重金属离子等分解加速。过氧乙酸完全燃烧能生成二氧化碳和水,具有酸的通性,可分解为乙酸和氧气,过氧乙酸属于高效消毒剂,气态过氧乙酸和溶液都具有很强的杀菌能力。它能杀灭细菌繁殖体、分枝杆菌、细菌芽孢、真菌、藻类及病毒,也可以破坏细菌毒素。
75%的酒精可用于消毒,这是因为该浓度的酒精渗透力很强,可穿透细菌表面,进入细菌内部,使组成细菌的蛋白质凝固,导数细菌失去活性。过高浓度的酒精会在细菌表面形成一层保护膜,阻止其进入细菌体内,难以将细菌彻底杀死,若酒精浓度过低,虽可进入细菌,但不能将其体内的蛋白质凝固,同样也下能将细菌彻底杀死,乙醇闪点为12.78℃。火灾危险性属于甲类,75%酒精闪点大约在22℃,火灾危险性还是属于甲类,因此在使用75%酒精进行消毒时,室内禁止采用喷洒式消毒,应采取擦拭方法进行消毒且在消毒过程中避免洒漏酒精,空气中酒精浓度不能超过3%,为防止火灾发生,应保持室内通风。室外采取喷洒式消毒必须禁止明火,防止局部喷洒浓度过大,造成遇明火引发火灾的风险。
阅读上述内容,回答下列问题:
(1)写出84消毒液的一条物理性质:
(2)过氧乙酸完全燃烧的文字表达式:
(3)在药店买到的酒精有75%和95%两种浓度,若用95%酒精配制一定量75%酒精,若要量取95%酒精50mL,用到的玻璃仪器有:量筒和
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】“二十四节气”与农耕生产息息相关。
(1)“春分”:莺飞草长,菜花飘香。从微观的角度分析闻到菜花香的可能原因为_____ 。
(2)“谷雨”:一颗红薯一把灰。其中的“灰”指草木灰(含碳酸钾),碳酸钾溶液显碱性,不能和含_____ (写离子符号)的肥料混合施用。
(3)“白露”:白露满地,割谷拾棉。古人用实心钢管敲打成“薄如叶”的镰刀割谷,说明铁具有良好的_____ 性。谷物秸秆用作土灶燃薪,为使“薪”完全燃烧,可采取的措施为_____ (写一条)。博物馆中陈列的镰刀上锈迹斑斑,请提出一条有利于铁制文物保护的措施_____ 。
(4)“秋分”:一粒好种,万担好粮。农业上用溶质质量分数为16%的氯化钠溶液来选种,现用100g溶质质量分数为20%的氯化钠溶液配制上述溶液。步骤:
①计算,需要水_____ g;
②_____ ;
③稀释。配制过程中需要用的仪器为:_____ 、胶头滴管、烧杯、玻璃棒。
(1)“春分”:莺飞草长,菜花飘香。从微观的角度分析闻到菜花香的可能原因为
(2)“谷雨”:一颗红薯一把灰。其中的“灰”指草木灰(含碳酸钾),碳酸钾溶液显碱性,不能和含
(3)“白露”:白露满地,割谷拾棉。古人用实心钢管敲打成“薄如叶”的镰刀割谷,说明铁具有良好的
(4)“秋分”:一粒好种,万担好粮。农业上用溶质质量分数为16%的氯化钠溶液来选种,现用100g溶质质量分数为20%的氯化钠溶液配制上述溶液。步骤:
①计算,需要水
②
③稀释。配制过程中需要用的仪器为:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】现需溶质质量分数为0.5%的过氧乙酸对环境进行消毒,请回答下列问题。
可供选用的实验用品:水、溶质质量分数20%的过氧乙酸、量筒(1000mL)、10L塑料桶、木棍、口罩、眼镜、橡皮手套。
(1)实验(配制)步骤:
①计算配制比例:将200g 20%的过氧乙酸稀释为0.5%的过氧乙酸,需加入水____________ g;若两者密度相等,则20%的过氧乙酸与所加水配制的体积比为_______________ (填最简整数比)。
②配制过程需戴好防护用品,因过氧乙酸有_________________ ;
A 碱性 B 腐蚀性 C 可燃性
③将相应体积的20%的过氧乙酸与水倒入塑料桶中,用_____________ 搅拌 后,盖好桶盖待用。
(2)过氧乙酸不能用铁质器皿盛装,原因是______________ 。
可供选用的实验用品:水、溶质质量分数20%的过氧乙酸、量筒(1000mL)、10L塑料桶、木棍、口罩、眼镜、橡皮手套。
(1)实验(配制)步骤:
①计算配制比例:将200g 20%的过氧乙酸稀释为0.5%的过氧乙酸,需加入水
②配制过程需戴好防护用品,因过氧乙酸有
A 碱性 B 腐蚀性 C 可燃性
③将相应体积的20%的过氧乙酸与水倒入塑料桶中,用
(2)过氧乙酸不能用铁质器皿盛装,原因是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐1】已知A~E为初中化学常见的五种物质。其中D的固体叫做“干冰”;B中只含两种元素,C是世界年产量最高的金属,且C与E不含相同元素。各种物质间的反应和转化关系如右下图所示(“一”表示相连的两种物质之间可以发生反应,“→”表示一种物质可以转化为另一种物质,反应条件、部分反应物和生成物已略去)。请分析后回答:

(1)物质D的名称是________ 。
(2)B-C反应类型为__________ 。
(3)写出下列反应的化学方程式:
①D→A:______________ 。
②C→E:______________ 。

(1)物质D的名称是
(2)B-C反应类型为
(3)写出下列反应的化学方程式:
①D→A:
②C→E:
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
真题
解题方法
【推荐2】利用废镍催化剂(主要成分:Ni,还含有少量的Zn、Fe、CaO等杂质)制备NiCO3的实验流程如下(虚线处部分流程略去):
(1)“酸溶”时,为使废镍充分溶解,可采取的措施有__________ (任写一种)。
(2)“氧化”阶段发生的反应为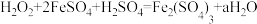 ,则a=
,则a=________ 。
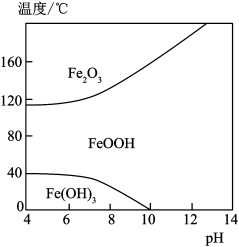
(3)“除铁”的目的是除去溶液中的Fe3+。改变温度、pH,Fe3+转化所得产物可能不同(如图)。80℃、pH=6时,Fe3+转化为________ (填化学式)。_____________ 。 该过程不能将NiSO4溶液滴入Na2CO3溶液中,其原因是____________ 。

(1)“酸溶”时,为使废镍充分溶解,可采取的措施有
(2)“氧化”阶段发生的反应为
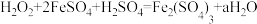 ,则a=
,则a=(3)“除铁”的目的是除去溶液中的Fe3+。改变温度、pH,Fe3+转化所得产物可能不同(如图)。80℃、pH=6时,Fe3+转化为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿空气中易变质。CuCl 的制备流程如下:
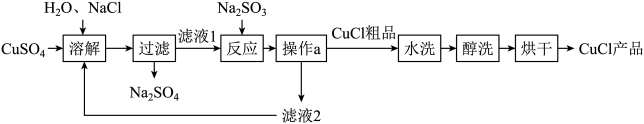
(1)“滤液 1”中除了Na+、SO42-外,还存在较多的离子是_____ 、_____ (写离子符号)。
(2)“反应”中发生的化学变化是 2CuCl2+Na2SO3=2CuCl +2NaCl+SO3
+2NaCl+SO3 ,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为
,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为_____ , 反应的基本类型为_____ 。
(3)“操作 a”的名称是_____ 。本流程中可以循环利用的物质(水除外)是_____ (写化学式)。
(4)可用“水洗”的原因是_________ ,“醇洗”的目的是_____ 。
(5)160g CuSO4与足量NaCl 经上述制备流程,可生成的 CuCl 最多是_____ g。

(1)“滤液 1”中除了Na+、SO42-外,还存在较多的离子是
(2)“反应”中发生的化学变化是 2CuCl2+Na2SO3=2CuCl
 +2NaCl+SO3
+2NaCl+SO3 ,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为
,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为(3)“操作 a”的名称是
(4)可用“水洗”的原因是
(5)160g CuSO4与足量NaCl 经上述制备流程,可生成的 CuCl 最多是
您最近一年使用:0次



