归纳总结是学习化学的一种方法。请结合小明同学对碱的四点化学性质的归纳图完成下列问题。(箭头上方的物质是指与碱反应的物质)
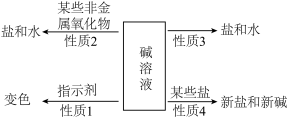
(1)碱溶液能使无色酚酞溶液变____________
(2)根据性质 2可知,NaOH 如果密封不好,久置后会变质,检验 NaOH 是否变质的一种盐溶液是__________
(3)性质 3 的化学反应从离子角度分析,实质是____________ 生成水分子
(4)工业上制备氢氧化钠可以利用性质 4 的反应,写出相关化学方程式____________

(1)碱溶液能使无色酚酞溶液变
(2)根据性质 2可知,NaOH 如果密封不好,久置后会变质,检验 NaOH 是否变质的一种盐溶液是
(3)性质 3 的化学反应从离子角度分析,实质是
(4)工业上制备氢氧化钠可以利用性质 4 的反应,写出相关化学方程式
更新时间:2020-08-17 19:28:46
|
相似题推荐
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】A、B、C、D、E是初中化学常见的物质,A和B发生中和反应,且生成物之一是生活中常见的调味品和防腐剂,C是常见的溶剂,B、E的物质类别相同。它们相互反应及转化关系如图所示,(图中“一”表示相连的两物质间能发生化学反应,“→”表示一种物质能转化为另一物质,部分反应物、生成物及反应条件已略去)
请回答下列问题。

(1)B物质的俗称为___________ 。
(2)C与D反应的基本反应类型是___________ 。
(3)写出E的一点用途___________ 。
(4)D与E反应的化学方程式___________ 。
请回答下列问题。

(1)B物质的俗称为
(2)C与D反应的基本反应类型是
(3)写出E的一点用途
(4)D与E反应的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】如图A~E分别是铁、硫酸、氢氧化钡、硫酸铜和碳酸钠五种物质之一,横线相连的物质之间能发生化学反应,其中C物质的溶液呈蓝色,A与E作用产生的气体是光合作用的原料之一。
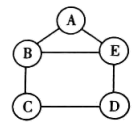
(1)A物质的俗称是____________ ,E物质的用途是____________ 。
(2)B与C作用的化学方程式为____________ 。

(1)A物质的俗称是
(2)B与C作用的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】烧碱是一种重要的工业原料。在工业上可以用纯碱和石灰石为原料制备氢氧化钠,主要流程如图所示:

(1)上述流程中,步骤②所涉及的反应类型为______ 反应(填“化合”、“分解”、“置换”、“复分解”之一)。
(2)步骤④中,分离烧碱溶液和碳酸钙沉淀应采用______ 操作。
(3)氢氧化钠有很强的腐蚀性,如果不小心沾到皮肤上,要立即用大量的水冲洗,然后涂上______ (填下列选项字母)。
A.硼酸溶液 B.3%~5%的碳酸氢钠溶液 C.石灰水
(4)室温下,某实验小组的同学将5.3%的Na2CO3溶液,逐滴加入到3000g澄清石灰水中,产生沉淀的质量与滴入Na2CO3溶液的质量关系如下图所示。试回答:

①当滴入Na2CO3溶液150g时(至图中B点),烧杯中溶液里一定大量存在的金属阳离子是______ (写离子符号)。
②当滴入Na2CO3溶液 100 g 时(至图中A点),恰好完全反应。试计算,此时所得NaOH溶液的质量是多少?______ (写出计算过程)

(1)上述流程中,步骤②所涉及的反应类型为
(2)步骤④中,分离烧碱溶液和碳酸钙沉淀应采用
(3)氢氧化钠有很强的腐蚀性,如果不小心沾到皮肤上,要立即用大量的水冲洗,然后涂上
A.硼酸溶液 B.3%~5%的碳酸氢钠溶液 C.石灰水
(4)室温下,某实验小组的同学将5.3%的Na2CO3溶液,逐滴加入到3000g澄清石灰水中,产生沉淀的质量与滴入Na2CO3溶液的质量关系如下图所示。试回答:

①当滴入Na2CO3溶液150g时(至图中B点),烧杯中溶液里一定大量存在的金属阳离子是
②当滴入Na2CO3溶液 100 g 时(至图中A点),恰好完全反应。试计算,此时所得NaOH溶液的质量是多少?
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】归纳总结是学习化学的重要方法,某化学兴趣小组学习碱的性质后,通过实验对氢氧化钙的化学性质进行了验证和总结,如图所示“一”表示物质两两之间能发生化学反应。请根据如图,回答问题。(已知:CaCl2,溶液呈中性)

(1)甲同学将酚酞试液滴入氢氧化钙溶液中,观察到溶液变红,得出结论:氢氧化钙溶液呈_____ (填“酸性”、“碱性”或“中性”);
(2)乙同学将过量的稀盐酸加入到甲同学所得溶液中,观察到的现象是_____ ,此时所得溶液中含有的溶质有_____ (酸碱指示剂除外);
(3)丙同学将碳酸钠溶液加入氢氧化钙溶液中,充分反应后,与乙同学所得溶液混合,静置后发现;上层为无色透明的溶液,底部有白色沉淀。则上层溶液中一定含有的溶质是_____ (酸碱指示剂除外);上层溶液中还可能含有氯化钙,为验证可能含有的溶质,应如何操作,该反应的化学方程式为:_____ 。

(1)甲同学将酚酞试液滴入氢氧化钙溶液中,观察到溶液变红,得出结论:氢氧化钙溶液呈
(2)乙同学将过量的稀盐酸加入到甲同学所得溶液中,观察到的现象是
(3)丙同学将碳酸钠溶液加入氢氧化钙溶液中,充分反应后,与乙同学所得溶液混合,静置后发现;上层为无色透明的溶液,底部有白色沉淀。则上层溶液中一定含有的溶质是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】实验室中有两瓶失去标签的无色溶液,已知是碳酸钠溶液和硫酸钠溶液中的各一种,小雪和小童同学想用化学方法确定各是哪种溶液,并进行了实验探究。
(1)①小雪各取两种无色溶液少许,分别加入A、B两支试管中,分别向两支试管中的溶液里滴加无色酚酞试液,观察到A试管中的液体变红,B试管中无明显现象。则可判断A试管中加入的是______ 溶液(填化学式)。
②小童从下列四种试剂中选取了一种试剂,进行鉴别实验,根据明显现象也成功鉴别了上述两种无色溶液。则小童所选的这种试剂是______ (填选项序号之一)。
A.Ba(NO3)2溶液 B.稀盐酸 C.K2SO4溶液 D.CaCO3固体
(2)化学小组的同学欲探究某固体混合物A的成分,已知A中可能含有(NH4)2SO4、K2CO3、BaCl2、Na2SO4四种物质中的两种或多种,如图所示进行探究实验,出现的现象如图中所述。(设过程中所有发生的反应都恰好完全反应)

试根据实验过程和和图示提供的信息,进行分析推理,回答下列问题:
①无色气体B的化学式为______ ,白色沉淀G的化学式为______ 。
②无色滤液D中一定大量存在的阳离子为______ 。
③写出步骤Ⅱ中一定发生反应的化学方程式______ 。
④根据上述实验现象判断,在固体混合物A里,上述四种物质中,还不能确定存在的物质是______ (填化学式)。得此结论的理由是______ 。
(1)①小雪各取两种无色溶液少许,分别加入A、B两支试管中,分别向两支试管中的溶液里滴加无色酚酞试液,观察到A试管中的液体变红,B试管中无明显现象。则可判断A试管中加入的是
②小童从下列四种试剂中选取了一种试剂,进行鉴别实验,根据明显现象也成功鉴别了上述两种无色溶液。则小童所选的这种试剂是
A.Ba(NO3)2溶液 B.稀盐酸 C.K2SO4溶液 D.CaCO3固体
(2)化学小组的同学欲探究某固体混合物A的成分,已知A中可能含有(NH4)2SO4、K2CO3、BaCl2、Na2SO4四种物质中的两种或多种,如图所示进行探究实验,出现的现象如图中所述。(设过程中所有发生的反应都恰好完全反应)

试根据实验过程和和图示提供的信息,进行分析推理,回答下列问题:
①无色气体B的化学式为
②无色滤液D中一定大量存在的阳离子为
③写出步骤Ⅱ中一定发生反应的化学方程式
④根据上述实验现象判断,在固体混合物A里,上述四种物质中,还不能确定存在的物质是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】A、B、C、D均为初中化学常见的纯净物,它们分别属于不同物质类别,A可用于纺织、印染、造纸等,它们之间的关系如下图所示。“→”表示一种物质经一步反应即可生成另一种物质,“一”表示两种物质可直接发生反应。部分反应物、生成物已省略。

请回答下列问题。
(1)A与FeCl3反应的化学方程式是_______ 。
(2)A与B反应的微观实质是________ 。
(3)C与D反应的现象是______ 。
(4)B与D反应的化学方程式是_____ 。

请回答下列问题。
(1)A与FeCl3反应的化学方程式是
(2)A与B反应的微观实质是
(3)C与D反应的现象是
(4)B与D反应的化学方程式是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】常见的酸、碱、盐在初中化学学习中占有非常重要地位,回答下列问题。
(1)将浓盐酸敞口放在空气中一段时间,浓盐酸的质量有何变化?_____ 。
(2)KCl是一种重要的盐,写出有KCl生成的中和反应方程式_____ 。
(3)实验室有失去标签的五瓶溶液:稀盐酸、石蕊溶液、Ca(OH)2溶液、NaOH溶液、Na2CO3溶液。根据观察溶液的颜色和分别取样两两混合,首先被鉴别出来的试剂是石蕊溶液,然后是_____ 。
(4)根据常温下部分酸、碱和盐的溶解性表,能获取那些信息?_____ 。(选序号)
①Ag2CO3在水中的溶解性
②浓HNO3在实验室里要密封保存;
③常温下Mg(OH)2能使酚酞溶液变红;
④在化合物中碳酸根离子显示的化合价;
⑤不能用水来鉴别NaCl和Na2SO4两种白色粉末;
⑥判断Na2CO3溶液与Ba(OH)2溶液能否发生复分解反应
(1)将浓盐酸敞口放在空气中一段时间,浓盐酸的质量有何变化?
(2)KCl是一种重要的盐,写出有KCl生成的中和反应方程式
(3)实验室有失去标签的五瓶溶液:稀盐酸、石蕊溶液、Ca(OH)2溶液、NaOH溶液、Na2CO3溶液。根据观察溶液的颜色和分别取样两两混合,首先被鉴别出来的试剂是石蕊溶液,然后是
(4)根据常温下部分酸、碱和盐的溶解性表,能获取那些信息?
部分酸、碱和盐的溶解性表(室温)
| H+ | K+ | NH4+ | Na+ | Ca2+ | Ba2+ | Mg2+ | Fe2+ | Cu2+ | Ag+ | |
| OH- | 溶 | 溶、挥 | 溶 | 微 | 溶 | 不 | 不 | 不 | 一 | |
| Cl- | 溶、挥 | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 | 不 |
| NO3- | 溶、挥 | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 |
| SO42- | 溶 | 溶 | 溶 | 溶 | 微 | 不 | 溶 | 溶 | 溶 | 微 |
| CO32- | 溶、挥 | 溶 | 溶 | 溶 | 不 | 不 | 微 | 不 | 一 | 不 |
①Ag2CO3在水中的溶解性
②浓HNO3在实验室里要密封保存;
③常温下Mg(OH)2能使酚酞溶液变红;
④在化合物中碳酸根离子显示的化合价;
⑤不能用水来鉴别NaCl和Na2SO4两种白色粉末;
⑥判断Na2CO3溶液与Ba(OH)2溶液能否发生复分解反应
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
【推荐3】在氢氧化钠溶液中加入 X 溶液并插入温度计,逐滴加入硫酸溶液,观察到红色褪去,温度计示数上升。证明碱与酸能发生反应,且放出热量。
(1)加入的 X 溶液应该是_____ 溶液;
(2)甲同学提出滴入的硫酸不能用浓硫酸,他的理由是_____ ;
(3)乙同学提出红色褪去不能说明酸和碱恰好反应完全,为了证明是否恰好反应,可取上述反应后的无色溶液少许加入_____ 即可(填序号)。
①铜 ②镁 ③氧化铜 ④BaCl2 溶液 ⑤Na2CO3 溶液
(4)若取10%的氢氧化钠溶液100g和10%的硫酸溶液100g混合后,加入紫色石蕊,则此时溶液呈_____ 色(填序号)。
①紫 ②红 ③蓝
(1)加入的 X 溶液应该是
(2)甲同学提出滴入的硫酸不能用浓硫酸,他的理由是
(3)乙同学提出红色褪去不能说明酸和碱恰好反应完全,为了证明是否恰好反应,可取上述反应后的无色溶液少许加入
①铜 ②镁 ③氧化铜 ④BaCl2 溶液 ⑤Na2CO3 溶液
(4)若取10%的氢氧化钠溶液100g和10%的硫酸溶液100g混合后,加入紫色石蕊,则此时溶液呈
①紫 ②红 ③蓝
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】有一包白色固体粉末可能由NH4C1、 、
、 、
、 、
、 、NaCl中的一种或几种组成。为了确定其组成,小东做了以下实验:(提示:AgCl、BaSO4不溶于稀硝酸)。
、NaCl中的一种或几种组成。为了确定其组成,小东做了以下实验:(提示:AgCl、BaSO4不溶于稀硝酸)。
①取少量白色粉末于研钵中,加入少量的熟石灰粉末混合,研磨,没有闻到氨味;
②另取少量白色粉末加入适量的水中,出现白色浑浊,过滤,得到白色滤渣和无色滤液;
③向②所得滤渣中加入足量稀硝酸,滤渣完全溶解,并有无色无味的气体产生。
④向②所得滤液中先加入过量硝酸钡溶液,充分反应后静置,取上层清液加入硝酸银溶液,有白色沉淀生成,再滴加稀硝酸,沉淀不溶解。由以上实验可推断:
(1)由①②③实验现象可以推测肯定不存在___________ ;
(2)由②③的现象可以确定这包固体中肯定含有___________ 。
(3)写出④中“生成不溶于稀硝酸的白色沉淀”的化学方程式___________ 。
 、
、 、
、 、
、 、NaCl中的一种或几种组成。为了确定其组成,小东做了以下实验:(提示:AgCl、BaSO4不溶于稀硝酸)。
、NaCl中的一种或几种组成。为了确定其组成,小东做了以下实验:(提示:AgCl、BaSO4不溶于稀硝酸)。①取少量白色粉末于研钵中,加入少量的熟石灰粉末混合,研磨,没有闻到氨味;
②另取少量白色粉末加入适量的水中,出现白色浑浊,过滤,得到白色滤渣和无色滤液;
③向②所得滤渣中加入足量稀硝酸,滤渣完全溶解,并有无色无味的气体产生。
④向②所得滤液中先加入过量硝酸钡溶液,充分反应后静置,取上层清液加入硝酸银溶液,有白色沉淀生成,再滴加稀硝酸,沉淀不溶解。由以上实验可推断:
(1)由①②③实验现象可以推测肯定不存在
(2)由②③的现象可以确定这包固体中肯定含有
(3)写出④中“生成不溶于稀硝酸的白色沉淀”的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐2】下列框图中的物质均为初中化学常见的物质,其中A是建筑材料的主要成分,B黑色固体,下图是它们之间的相互转化关系。请回答:

(1)写出下列物质的化学式:A_____________ B__________________ 。
(2)得到F溶液的操作Ⅰ的名称为:________________ 。
(3)请写出E →F的化学方程式:______________________________________ 。
(4)请写出G →I的化学方程式:______________________________________ 。

(1)写出下列物质的化学式:A
(2)得到F溶液的操作Ⅰ的名称为:
(3)请写出E →F的化学方程式:
(4)请写出G →I的化学方程式:
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
解题方法
【推荐3】某学习小组探究干冰与NaOH的反应。
实验1探究干冰与NaOH溶液是否反应
如图1,在试管中放入几小块干冰,将产生的气体通入NaOH溶液中。

(1)干冰易升华利用了干冰的__________ 性质(填“物理”或“化学”)。
(2)将上述反应后的溶液分成2份,一份滴加足量Ca(OH)2溶液,如果观察到__________ ,另一份滴入足量盐酸,如果观察到__________ ,说明CO2与NaOH发生反应,反应的化学方程式为__________ 。
实验2探究干冰与不同浓度NaOH溶液反应过程中的pH变化情况
取150mL蒸馏水和150mL溶质质量分数为3%、2%、1%的氢氧化钠溶液于4个烧杯中,分别加入20g干冰,通过传感器测其pH,且pH变化如图2所示。

(3)用NaOH固体配制一定溶质质量分数的溶液,无需用到的仪器有 (填标号)。
(4)蒸馏水中加入干冰后,溶液呈__________ (填“酸”或“碱”)性,该实验目的是__________ 。
(5)与干冰混合后,碱性最弱的一组对应的原氢氧化钠溶液的浓度为__________ 。
实验3探究干冰与NaOH溶液反应的产物成分
(6)在密闭体系中,分别往等体积、等浓度的Na2CO3溶液和NaHCO3溶液逐滴加入等浓度的稀硫酸,压强变化曲线如图3所示。

0~50s,压强无明显变化的体系中,反应生成的含碳元素的盐类物质M是___________ (填化学式)。
(7)受上述结论启发,分别取20mL实验2反应后的溶液,逐滴滴加5.3%的稀硫酸,获得的相关数据如下表所示。
①结合表中数据分析,2%NaOH与干冰反应后溶液中的溶质是__________ 。
②所取的20mL溶液中,Na2CO3质量分数最大的是__________ (填实验编号)。
实验1探究干冰与NaOH溶液是否反应
如图1,在试管中放入几小块干冰,将产生的气体通入NaOH溶液中。

(1)干冰易升华利用了干冰的
(2)将上述反应后的溶液分成2份,一份滴加足量Ca(OH)2溶液,如果观察到
实验2探究干冰与不同浓度NaOH溶液反应过程中的pH变化情况
取150mL蒸馏水和150mL溶质质量分数为3%、2%、1%的氢氧化钠溶液于4个烧杯中,分别加入20g干冰,通过传感器测其pH,且pH变化如图2所示。

(3)用NaOH固体配制一定溶质质量分数的溶液,无需用到的仪器有 (填标号)。
| A.胶头滴管 | B.酒精灯 | C.量筒 | D.烧杯 | E.玻璃棒 |
(4)蒸馏水中加入干冰后,溶液呈
(5)与干冰混合后,碱性最弱的一组对应的原氢氧化钠溶液的浓度为
实验3探究干冰与NaOH溶液反应的产物成分
(6)在密闭体系中,分别往等体积、等浓度的Na2CO3溶液和NaHCO3溶液逐滴加入等浓度的稀硫酸,压强变化曲线如图3所示。

0~50s,压强无明显变化的体系中,反应生成的含碳元素的盐类物质M是
(7)受上述结论启发,分别取20mL实验2反应后的溶液,逐滴滴加5.3%的稀硫酸,获得的相关数据如下表所示。
| 实验编号 | A | B | C |
| 取20mL对应溶液 | 3%NaOH与干冰反应后的溶液 | 2%NaOH与干冰反应后的溶液 | 1%NaOH与干冰反应后的溶液 |
| 完全生成M时消耗硫酸体积V1/mL | 4.14 | 1.43 | 0.36 |
| M完全转化成CO2时消耗硫酸体积V2/mL | 4.55 | 2.46 | 1.60 |
②所取的20mL溶液中,Na2CO3质量分数最大的是
您最近一年使用:0次




