硫铁矿【主要成分是二硫化亚铁(FeS2)】,其他成分不含铁,硫元素是一种重要的化工原料,常用来制备硫酸和氯化铁,工业生产流程如图所示。
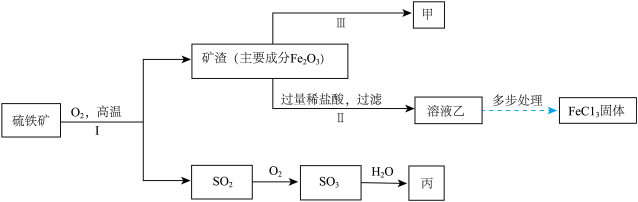
(1)过滤中玻璃棒的作用是___________ ;
(2)步骤二中主要反应的化学方程式为_______________ ;
(3)溶液乙中一定有的阳离子______________________ ;
(4)上述流程中所涉及的含硫的物质中,硫元素的化合价共有_________ 种。
(5)若硫铁矿中的硫元素可完全转化为硫酸,则300t含80%的硫铁矿可制得硫酸的质量为________ 吨。

(1)过滤中玻璃棒的作用是
(2)步骤二中主要反应的化学方程式为
(3)溶液乙中一定有的阳离子
(4)上述流程中所涉及的含硫的物质中,硫元素的化合价共有
(5)若硫铁矿中的硫元素可完全转化为硫酸,则300t含80%的硫铁矿可制得硫酸的质量为
更新时间:2020-09-15 09:38:37
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】水是生命之源,请回答下列问题:
(1)小明同学想知道买的“中梁山”牌矿泉水是硬水还是软水,可用_______ 来检验。生活中常用_______ 的方法降低水的硬度,并起到消毒杀菌的作用。
(2)直饮水机的水处理过程如图所示。
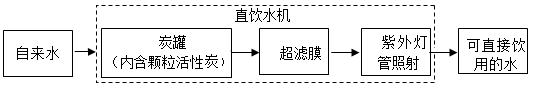
①图中“可直接饮用的水”属于_______ (填“混合物”或“纯净物”)。
②图中炭罐的主要作用是_______ (填标号)。
A 过滤 B.脱色除味 C.消毒杀菌 D.降低水的硬度
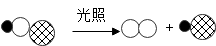
(3)目前不少自来水厂用液氯(Cl2)作为消毒剂,液氯注入水后发生反应生成的次氯酸(HClO有消毒、杀菌的作用。用白来水养金鱼,在将水注入鱼缸之前,常须把水在阳光下明晒一段时间,使水中的次氯酸分解,次氯酸在光照条件下发生分解的示意图如下:
 (“
(“ ”代表氢原子、“
”代表氢原子、“ ”代表氧原子,“
”代表氧原子,“ ”代表氯原子)次氧酸在光照条件下发生分解的化学方程式为
”代表氯原子)次氧酸在光照条件下发生分解的化学方程式为_______ 。
(1)小明同学想知道买的“中梁山”牌矿泉水是硬水还是软水,可用
(2)直饮水机的水处理过程如图所示。

①图中“可直接饮用的水”属于
②图中炭罐的主要作用是
A 过滤 B.脱色除味 C.消毒杀菌 D.降低水的硬度
(3)目前不少自来水厂用液氯(Cl2)作为消毒剂,液氯注入水后发生反应生成的次氯酸(HClO有消毒、杀菌的作用。用白来水养金鱼,在将水注入鱼缸之前,常须把水在阳光下明晒一段时间,使水中的次氯酸分解,次氯酸在光照条件下发生分解的示意图如下:
 (“
(“ ”代表氢原子、“
”代表氢原子、“ ”代表氧原子,“
”代表氧原子,“ ”代表氯原子)次氧酸在光照条件下发生分解的化学方程式为
”代表氯原子)次氧酸在光照条件下发生分解的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】我国提出2060年前实现碳中和,彰显了负责任大国的作为与担当。
(1)现阶段的能源结构仍以化石燃料为主,化石燃料包括煤、__________ 和天然气。写出天然气完全燃烧的化学方程式:_______ 。
(2)捕集、利用和封存CO2是实现碳中和的一种途径
Ⅰ.矿物质碳化封存的反应之一是氧化镁与CO2反应生成碳酸镁,碳酸镁的化学式为________ 。
Ⅱ.CO2的“捕集”,如图是一种利用NaOH溶液“捕集”CO2的主要技术流程。
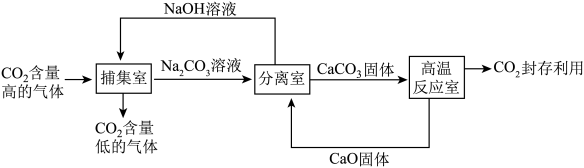
①“捕集室”中发生反应的化学方程式是_______ 。“捕集室”中采用喷淋方式加入NaOH溶液,其优点是______ 。
②整个设计流程中,可以循环利用的物质是CO2和___________ (填化学式)。
(3)CO2的利用在高温高压下,CO2和NH3可以合成尿素【CO(NH2)2】,同时生成水,该反应中参加反应的CO2与NH3的分子个数比是__________ 。
(4)从环境保护的角度考虑,___________ 被认为是理想的清洁、高能燃料。
(1)现阶段的能源结构仍以化石燃料为主,化石燃料包括煤、
(2)捕集、利用和封存CO2是实现碳中和的一种途径
Ⅰ.矿物质碳化封存的反应之一是氧化镁与CO2反应生成碳酸镁,碳酸镁的化学式为
Ⅱ.CO2的“捕集”,如图是一种利用NaOH溶液“捕集”CO2的主要技术流程。

①“捕集室”中发生反应的化学方程式是
②整个设计流程中,可以循环利用的物质是CO2和
(3)CO2的利用在高温高压下,CO2和NH3可以合成尿素【CO(NH2)2】,同时生成水,该反应中参加反应的CO2与NH3的分子个数比是
(4)从环境保护的角度考虑,
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐3】阅读下列科普短文,回答问题。
新能源汽车已经走进了我们的生活。与传统汽车使用化石燃料不同,新能源汽车的能量来源更加多元化。电动汽车:电池能为电动汽车提供动力,几类电池的部分性能指标如图1所示。其中能量密度表示单位体积的电池所具有的能量;氢内燃车:氢内燃车以氢气为燃料,不排放任何污染物。氢气可通过电解水(原理如图2)等多种方式获得。据测算,1kg氢气完全燃烧可释放14.3×104kJ的热量,1kg汽油完全燃烧可释放4.6×104kJ的热量;乙醇汽车:乙醇汽车以乙醇为燃料,乙醇是可再生能源,可以通过发酵甘蔗、玉米等农作物,或发酵粮食收割后剩余的秸秆大量提取;太阳能汽车:以太阳能电池驱动,低碳环保,真正实现了零排放。我国新能源汽车发展迅速,未来可期。
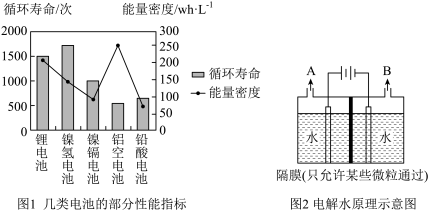
(1)依据图1,锂电池优于镍氢电池的性能指标是________ 。
(2)依据测算数据可知,氢内燃车与汽油车相比的优势是___________ 。
(3)乙醇燃烧的化学方程式_____________ 。
(4)下列说法正确的是 (填序号)。
新能源汽车已经走进了我们的生活。与传统汽车使用化石燃料不同,新能源汽车的能量来源更加多元化。电动汽车:电池能为电动汽车提供动力,几类电池的部分性能指标如图1所示。其中能量密度表示单位体积的电池所具有的能量;氢内燃车:氢内燃车以氢气为燃料,不排放任何污染物。氢气可通过电解水(原理如图2)等多种方式获得。据测算,1kg氢气完全燃烧可释放14.3×104kJ的热量,1kg汽油完全燃烧可释放4.6×104kJ的热量;乙醇汽车:乙醇汽车以乙醇为燃料,乙醇是可再生能源,可以通过发酵甘蔗、玉米等农作物,或发酵粮食收割后剩余的秸秆大量提取;太阳能汽车:以太阳能电池驱动,低碳环保,真正实现了零排放。我国新能源汽车发展迅速,未来可期。

(1)依据图1,锂电池优于镍氢电池的性能指标是
(2)依据测算数据可知,氢内燃车与汽油车相比的优势是
(3)乙醇燃烧的化学方程式
(4)下列说法正确的是 (填序号)。
| A.依据图1可知,提供相同能量时,铝空电池的体积最小 |
| B.图2中,A口产生的气体为氢气 |
| C.农业大国盛产甘蔗和玉米,有利于推广乙醇汽车 |
| D.报废的电动汽车电池,要及时用土进行掩埋处理 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在点燃条件下,一定质量的C2H2与7.2gO2恰好完全反应,生成6.6gCO2、1.8gH2O和xgCO。则x=_____ ;化学方程式为_____ 。要让这一定量的C2H2充分燃烧还需氧气的质量为_____ g。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】铝和氢氧化钠、水反应生成偏铝酸钠(化学式为NaA1O2)和氢气,其反应的化学方程式___________ ;将一定量的铝放入80g氢氧化钠溶液中,恰好完全反应,测得反应前后溶液中钠元素的质量分数之比为28:25,则生成的氢气质量为___________ g。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】用化学符号或文字按要求填空:
(1)3个氢分子_______ 。
(2)构成氧化镁的微粒_______ 。
(3)标出氢氧化铝中铝元素的化合价_______ 。
(4)P2O5右下角数字“5”的含义_______ 。
(1)3个氢分子
(2)构成氧化镁的微粒
(3)标出氢氧化铝中铝元素的化合价
(4)P2O5右下角数字“5”的含义
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】请按下列要求写出化学符号
(1)氧化铁________
(2)2个铵根离子_________
(3)3个钡离子_____________
(4)过氧化氢中氧元素的化合价______
(1)氧化铁
(2)2个铵根离子
(3)3个钡离子
(4)过氧化氢中氧元素的化合价
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐1】如图,A、B、C、D、E是初中化学中常见的不同类别的物质。已知A是单质;C是红棕色固体;D可做干燥剂;E俗称纯碱。图中“-”表示相连的物质两两之间可以发生反应,“ ”表示由某一物质可制得另一物质(部分反应物、生成物及反应条件已略去)。回答下列问题:
”表示由某一物质可制得另一物质(部分反应物、生成物及反应条件已略去)。回答下列问题:
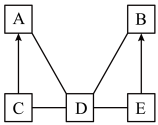
(1)写化学式:D______ ;
(2)由E转化为B的化学方程式为______ ;
(3)由C转化为A的原理在工业上常用于______ 。
 ”表示由某一物质可制得另一物质(部分反应物、生成物及反应条件已略去)。回答下列问题:
”表示由某一物质可制得另一物质(部分反应物、生成物及反应条件已略去)。回答下列问题:
(1)写化学式:D
(2)由E转化为B的化学方程式为
(3)由C转化为A的原理在工业上常用于
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】稀土金属因其独特的性能而被誉为“新材料之母”。稀土金属钇的氧化物(Y2O3)广泛应用于航空航天涂层材料,其颗粒大小决定了产品的质量。利用富钇稀土(含Y2O3约70%,含Fe2O3、CuO、SiO2等约30%)生产大颗粒氧化钇的一种工艺如图:
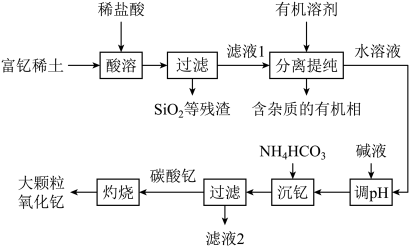
(1)氧化纪(Y2O3)中,Y元素的化合价为______________ 。
(2)“酸溶”过程中,氧化钇与盐酸反应的化学方程式是_________________ 。
(3)“分离提纯”是为了除去滤液1中的______________ (填化学式)。
(4)碳酸钇灼烧分解的化学方程式____________________ 。
(5)为了获得大颗粒氧化钇,某小组研究了条件对产品直径的影响,相关数据如下(D50表示颗粒直径):
分析上表数据,其他条件不变时,若将灼烧温度均升高至1400℃,预期所得氧化钇D50最大的是_______ (填实验编号)。

(1)氧化纪(Y2O3)中,Y元素的化合价为
(2)“酸溶”过程中,氧化钇与盐酸反应的化学方程式是
(3)“分离提纯”是为了除去滤液1中的
(4)碳酸钇灼烧分解的化学方程式
(5)为了获得大颗粒氧化钇,某小组研究了条件对产品直径的影响,相关数据如下(D50表示颗粒直径):
| 实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 沉淀反应温度/℃ | 60 | 80 | 85 | 93 | 93 | 93 |
| 料液浓度/(g/L) | 30 | 30 | 30 | 30 | 40 | 40 |
| 灼烧温度/℃ | 1100 | 1100 | 1100 | 1100 | 1100 | 1400 |
| 氧化钇D50/um | 6.00 | 21.65 | 35.99 | 38.56 | 35.99 | 61.54 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】构建模型和构建知识网络是化学学习中重要的学习方法,小雷同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:
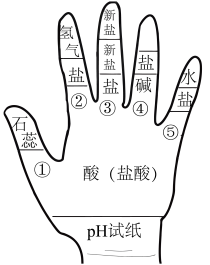
(1)为了验证性质①,小雷将紫色石蕊试液滴加到稀盐酸中,观察到______ 。
(2)小雷将一枚生锈的铁钉放入足量的稀盐酸中,他首先观察到的现象是铁锈( )溶解,溶液由无色变成黄色,过一会儿,他又观察到有气泡产生。发生以上反应现象的化学方程式为
)溶解,溶液由无色变成黄色,过一会儿,他又观察到有气泡产生。发生以上反应现象的化学方程式为______ (任写一个)。
(3)图中性质④属于______ (填基本反应类型)。

(1)为了验证性质①,小雷将紫色石蕊试液滴加到稀盐酸中,观察到
(2)小雷将一枚生锈的铁钉放入足量的稀盐酸中,他首先观察到的现象是铁锈(
 )溶解,溶液由无色变成黄色,过一会儿,他又观察到有气泡产生。发生以上反应现象的化学方程式为
)溶解,溶液由无色变成黄色,过一会儿,他又观察到有气泡产生。发生以上反应现象的化学方程式为(3)图中性质④属于
您最近一年使用:0次



